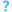التركيب الجيني H5N1
فيروس الإنفلونزا أ H5N1 (A / H5N1) | |
|---|---|
| تصنيف الفيروسات | |
| المجموعة: | نعم |
| المملكة: | الفيروسات |
| الشعبة: | Negarnaviricota |
| الطائفة: | Insthoviricetes |
| الرتبة: | Articulavirales |
| الفصيلة: | فيروس الإنفلونزا |
| الجنس: | فيروس إنفلونزا أ |
| الجنيس: | فيروس الإنفلونزا أ H5N1 (A / H5N1) |
| النوع: | فيروس إنفلونزا أ |
| تعديل مصدري - تعديل | |
 |
التركيب الجيني هو التركيب الجزيئي للحمض النووي الريبي لفيروس H5N1.
H5N1 هو نوع فرعي من فيروس الإنفلونزا أ. يعتقد الخبراء أنه قد يتحول إلى شكل ينتقل بسهولة من شخص لآخر. إذا حدثت مثل هذه الطفرة، فقد تظل من النوع الفرعي H5N1 أو يمكن أن تغير الأنواع الفرعية كما حدث في H2N2 عندما تطورت إلى سلالة H3N2 من إنفلونزا هونج كونج.
تحور H5N1[1] خلال انجراف المستضدات إلى عشرة أصناف شديدة الإمراض، ولكن جميعها تنتمي حاليًا إلى النمط الجيني Z لفيروس إنفلونزا الطيور H5N1. ظهر النمط الجيني Z من خلال إعادة التصنيف في عام 2002 من الأنماط الجينية المسببة للأمراض الشديدة H5N1 التي ظهرت لأول مرة في الصين في عام 1996 في الطيور وفي هونغ كونغ في عام 1997 في البشر.[2] «تم عزل فيروسات H5N1 المسببة للعدوى البشرية المرتبطة ارتباطًا وثيقًا بفيروسات الطيور في عامي 2004 و 2005 إلى نمط جيني واحد، يشار إليه غالبًا باسم النمط الجيني Z».[1]
هذه العدوى على البشر تزامنت مع الوبائية (و باء في غير البشر) من أنفلونزا H5N1 في عدد السكان الدواجن في هونغ كونغ. تم إيقاف تفشي هذا المرض (المرض الذي يصيب الحيوانات من العديد من الأنواع خاصة على مساحة واسعة) من خلال قتل جميع الدواجن المحلية داخل الإقليم. يشير الاسم H5N1 إلى الأنواع الفرعية للمستضدات السطحية الموجودة على الفيروس:
- الراصة الدموية من النوع الـ 5 (Hemagglutinin).
- وأنزيم نورامينيداز من النوع الـ 1 (Neuraminidase).
النمط الجيني Z لـ H5N1 هو الآن النمط الجيني المهيمن لـ H5N1. النمط الجيني Z مستوطن في الطيور في جنوب شرق آسيا ويمثل تهديدًا وبائيًا طويل المدى.
تحتوي فيروسات الإنفلونزا A على 11 جينًا في ثمانية جزيئات منفصلة من الرنا[1]:
- PB2 (البلمرة الأساسية 2).
- PB1 (البلمرة الأساسية 1).
- PB1-F2 (alternate open reading frame near the 5' end of the PB1 gene).
- PB (البلمرة الحمضية).
- الراصة الدموية (Hemagglutinin).
- NP (بروتين نووي).
- NA (نيورامينيداز).
- M1 وM2 (مصفوفة).
- NS1 (غير بنيوي).
- NEP / NS2 (التصدير النووي من vRNPs).
اثنان من أهم جزيئات RNA هما HA و PB1. يخلق HA مستضد سطحي مهم بشكل خاص في قابلية الانتقال. يخلق PB1 جزيء بوليميراز فيروسي مهم بشكل خاص في الضراوة.
يحتوي جزيء HA RNA على جين HA، الذي يرمز لـ hemagglutinin ، وهو بروتين سكري مستضدي موجود على سطح فيروسات الإنفلونزا وهو مسؤول عن ربط الفيروس بالخلية المصابة. يشكل Hemagglutinin طفرات على سطح فيروسات الإنفلونزا التي تعمل على التصاق الفيروسات بالخلايا. هذا المرفق مطلوب من أجل النقل الفعال لجينات فيروس الإنفلونزا إلى الخلايا، وهي عملية يمكن أن تسدها الأجسام المضادة التي ترتبط ببروتينات الهيماجلوتينين.
أحد العوامل الوراثية في التمييز بين فيروسات الإنفلونزا البشرية وفيروسات إنفلونزا الطيور هو أن أنفلونزا الطيور HA تربط مستقبلات حمض ألفا 2-3 في حين أن أنفلونزا HA البشرية تربط مستقبلات حمض ألفا 2-6. فيروسات إنفلونزا الخنازير لديها القدرة على ربط نوعي مستقبلات حمض السياليك. لدى البشر مستقبلات من نوع الطيور بكثافات منخفضة للغاية ولدى الدجاج مستقبلات من النوع البشري بكثافات منخفضة للغاية. وقد لوحظ أن بعض العينات المعزولة المأخوذة من إنسان مصاب بفيروس H5N1 بها طفرات HA في المواضع 182، 192، 223، 226 أو 228 وقد ثبت أن هذه الطفرات تؤثر على الارتباط الانتقائي للفيروس إلى أولئك الذين سبق ذكرهم من حمض السياليك و / أو مستقبلات سطح الخلية البشرية. هذه هي أنواع الطفرات التي يمكن أن تحول فيروس إنفلونزا الطيور إلى جائحة إنفلونزا.
أنتجت دراسة عن حدة الجرثوم في عام 2008 في أحد المختبرات تزاوجت فيروس إنفلونزا الطيور H5N1 الذي تم تداوله في تايلاند عام 2004 وفيروس إنفلونزا H3N2 المكتشف في وايومنغ عام 2003، أنتجت 63 فيروسًا تمثل مجموعات مختلفة محتملة من جينات فيروس إنفلونزا الطيور والبشر. كان واحد من كل خمسة مميتًا للفئران بجرعات منخفضة. كان الفيروس الذي كان أقرب ما يكون إلى فيروس H5N1 من حيث الضراوة هو الذي يحتوي على hemagglutinin (HA)، وneuraminidase (NA) وجزيئات RNA لفيروس إنفلونزا الطيور PB1 مع جيناتها مقترنة بجزيئات RNA الخمسة المتبقية (PB2 ، PA ، NP ، M ، و NS) مع جيناتهم من فيروس الإنفلونزا البشرية. تحمل كل من فيروسات جائحة 1957 و1968 وباء إنفلونزا الطيور جين PB1. يقترح المؤلفون أن التقاط جين PB1 لفيروس إنفلونزا الطيور قد يكون خطوة في فيروس الإنفلونزا المحتملة الناشئة عن إعادة تشكل الفيروس."[3]
رموز PB1 لبروتين PB1 وبروتين PB1-F2. بروتين PB1 هو مكون حاسم من البلمرة الفيروسية. يتم تشفير بروتين PB1-F2 بواسطة إطار قراءة مفتوح بديل للجزء PB1 RNA و «يتفاعل مع مكونين من مسام نفاذية الميتوكوندريا ANT3 و VDCA1، [تحس] الخلايا إلى موت الخلايا. يساهم PB1-F2 على الأرجح في الإمراضية الفيروسية وقد يكون له دور مهم في تحديد شدة جائحة الأنفلونزا.»[4] تم اكتشاف هذا من قبل "Chen et al". وذكرت في مجلة الطبيعة.[5] «بعد مقارنة الفيروسات من فاشية H5N1 بهونج كونج 1997، تم العثور على تغير واحد في الأحماض الأمينية (N66S) في تسلسل PB1-F2 في الموضع 66 والذي ارتبط بالإمراض. تم العثور على نفس هذا التغيير في الأحماض الأمينية (N66S) أيضًا في بروتين PB1-F2 لفيروس A / Brevig Mission / 18 الوبائي لعام 1918».[6]
المصطلح[عدل]
تتكون عائلة فيروس الإنفلونزا "Orthomyxoviridae" من 5 أجناس: فيروس إنفلونزا أ، فيروس إنفلونزا ب، فيروس إنفلونزا ج، فقر الدم السلمون المعدية وفيروس الغدة الدرقية.
تتضمن «فيروسات RNA» «فيروسات sRRNA السلبية» التي تتضمن عائلة "Orthomyxoviridae" التي تحتوي على خمسة أجناس، مصنفة حسب التباينات في مستضدات البروتين النووي (NP و M). أحد هذه الأنواع هو فيروس "Influenzavirus A" الذي يتكون من نوع واحد يسمى «فيروس إنفلونزا أ»؛ أحد أنواعه الفرعية هو H5N1.
H5N1 (مثل فيروسات إنفلونزا الطيور الأخرى) لديها سلالات تسمى «شديدة الإمراض» (HP) و «منخفضة الإمراض» (LP). إن فيروسات إنفلونزا الطيور التي تسبب أنفلونزا الطيور عالية الإمراض شديدة الضراوة، ومعدلات الوفيات في قطعان الطيور المصابة تقترب من 100٪. عادة ما تكون فيروسات LPAI أقل ضراوة، ولكن يمكن أن تكون هذه الفيروسات بمثابة أسلاف لفيروسات HPAI. السلالة الحالية من فيروس H5N1 المسؤول عن نفوق الطيور الداجنة في آسيا هي سلالة HPAI؛ سلالات أخرى من H5N1 تحدث في أماكن أخرى من العالم أقل ضراوة، وبالتالي، تصنف على أنها سلالات LPAI. جميع سلالات HPAI التي تم تحديدها حتى الآن اشتملت على أنواع فرعية H5 و H7. التمييز يتعلق بالإمراض في الدواجن، وليس البشر. عادة ما يكون فيروس الطيور شديد الإمراض ليس شديد الإمراض للبشر أو الطيور غير الداجنة. هذه السلالة الحالية من H5N1 غير عادية في كونها مميتة للعديد من الأنواع.
يمكن استخدام كل من «الإنفلونزا» (التي تعني الإنفلونزا) و «أ» (أي النوع «أ») كصفات لـ «فيروس» الذي ينتج عنه الاسم «فيروس الإنفلونزا أ»؛ الذي عندما يتم تكبيره هو الاسم المناسب لفيروس إنفلونزا أ وهو اسم النوع الذي تشير إليه عبارة الاسم أيضًا.
السياق[عدل]
الفيروس
الفيروس هو أحد أنواع الطفيليات المجهرية التي تصيب الخلايا في الكائنات الحية.
Orthomyxoviridae
Orthomyxoviridae هي عائلة من فيروسات RNA التي تصيب الفقاريات. ويشمل تلك الفيروسات التي تسبب الأنفلونزا. تحتوي فيروسات هذه العائلة على 7 إلى 8 أجزاء من الحمض النووي الريبي الخطي ذي الحزم السلبية الأحادية.
فيروس الإنفلونزا
يشير «فيروس الإنفلونزا» إلى مجموعة فرعية من Orthomyxoviridae التي تخلق الأنفلونزا. لا تعتمد هذه الفئة التصنيفية على علم الوراثة.
فيروس الإنفلونزا أ
تحتوي فيروسات الإنفلونزا A على 10 جينات في ثمانية جزيئات RNA منفصلة، والتي، للأسباب المذكورة أعلاه، تسمى PB2 و PB1 و PA و HA و NP و NA و M و NS. تحدد HA و NA و M بنية البروتينات الأكثر صلة من الناحية الطبية كأهداف للعقاقير المضادة للفيروسات والأجسام المضادة. (الجين الحادي عشر المكتشف مؤخرًا يسمى PB1-F2 ينتج أحيانًا بروتينًا ولكنه غائب عن بعض عزلات فيروس الإنفلونزا.[5]) هذا التقسيم لجينوم الإنفلونزا يسهل إعادة التركيب الجيني عن طريق إعادة ترتيب المقطع في العوائل المصابة بفيروسين مختلفين للأنفلونزا في نفس الوقت.[1] فيروس الإنفلونزا هو النوع الوحيد في الأنفلونزا A جنس من عائلة فيروسات مخاطية قويمة وهي بالمعنى السلبي، واحد الذين تقطعت بهم السبل، مجزأة فيروسات RNA.
«إن فيروس الأنفلونزا RNA polymerase هو مركب متعدد الوظائف يتكون من البروتينات الفيروسية الثلاثة PB1 و PB2 و PA، والتي تشكل، مع البروتين النووي الفيروسي NP، الحد الأدنى من المكمل المطلوب لتوليف mRNA الفيروسي وتكراره.»[7]
الترميز الجيني للسطح[عدل]
- شرائح الجين المشفر للمستضد السطحي (جزيء RNA): (HA، NA).
- يرمز HA إلى hemagglutinin وهو بروتين سكري مستضدي موجود على سطح فيروسات الإنفلونزا وهو مسؤول عن ربط الفيروس بالخلية المصابة. يشكل Hemagglutinin طفرات على سطح فيروسات الإنفلونزا التي تعمل على إرفاق الفيروسات بالخلايا. هذا المرفق مطلوب من أجل النقل الفعال لجينات فيروس الإنفلونزا إلى الخلايا، وهي عملية يمكن أن تسدها الأجسام المضادة التي ترتبط ببروتينات الهيماجلوتينين. أحد العوامل الوراثية في التمييز بين فيروسات إنفلونزا الطيور وفيروسات إنفلونزا الطيور هو أن «HA1 تربط مستقبلات حمض سياليك ألفا في حين أن HA يربط مستقبلات حمض ألفا 2-6 ألفا. إن فيروسات إنفلونزا الخنازير لديها القدرة على ربط نوعي مستقبلات حمض السياليك».[8] الطفرة الموجودة في تركيا في عام 2006 «تنطوي على استبدال في عينة واحدة من حمض أميني في الموضع 223 من بروتين مستقبلات الهيموغلوتينين. يسمح هذا البروتين لفيروس الإنفلونزا بالارتباط بالمستقبلات على سطح خلايا مضيفه. وقد لوحظ هذا التحور مرتين من قبل - في الأب والابن في هونغ كونغ في عام 2003، وفي حالة مميتة في فيتنام العام الماضي. إنه يزيد من قدرة الفيروس على الارتباط بمستقبلات الإنسان، ويقلل من ارتباطه بمستقبلات الدواجن، مما يجعل السلالات مع هذه الطفرة تتكيف بشكل أفضل مع إصابة البشر». طفرة أخرى في نفس العينة في الموضع 153 لها آثار غير معروفة حتى الآن.[9] «يبدو أن بقايا الأحماض الأمينية في الموضع 226 و 228 من جيب ربط المستقبلات لـ HA تحدد تقارب الارتباط لمستقبلات سطح الخلية والتأثير على الارتباط الانتقائي للفيروس إلى الطيور (حمض السياليك -2,3-NeuAcGal) أو الإنسان (سياليك) حمض -2,6-NeuAcGal) مستقبلات سطح الخلية. تحتفظ عزلات الإنسان A / HK / 212/03 و A / HK / 213/03 بالتوقيع المرتبط بربط مستقبلات الطيور، ولكن لديهم استبدال فريد للأحماض الأمينية (Ser227Ile) داخل جيب ربط المستقبلات لم يكن موجودًا حتى في فيروس A / Gs / HK / 739.2 / 02 وثيق الصلة (النمط الجيني Z +)».[10] تكشف الأبحاث الحديثة أن البشر لديهم مستقبلات من نوع الطيور بكثافات منخفضة جدًا وأن الدجاج لديه مستقبلات من النوع البشري بكثافات منخفضة جدًا.[11] وجد الباحثون أن الطفرات في مكانين في الجين، التي تم تحديدها باسم 182 و 192، تسمح للفيروس بالارتباط بمستقبلات الطيور والبشر.[12][13]
- يرمز NA إلى إنزيم النيورامينيداز وهو إنزيم بروتين سكري مستضد موجود على سطح فيروسات الإنفلونزا. يساعد على إطلاق فيروسات النسل من الخلايا المصابة. تعمل عقاقير الإنفلونزا تاميفلو وريلينزا عن طريق تثبيط بعض سلالات النورامينيداز. تم تطويرها على أساس N2 و N9. «في شكل N1 من البروتين، يتم عكس جزء صغير يسمى 150 حلقة، مما يخلق جيبًا مجوفًا غير موجود في بروتينات N2 و N9. عندما نظر الباحثون في كيفية تفاعل الأدوية الموجودة مع بروتين N1، وجدوا أنه في وجود مثبطات النيورامينيداز، غيرت الحلقة تشكيلها إلى واحدة مماثلة لتلك الموجودة في بروتينات N2 و N9».[14]
الترميز الجيني الداخلي[عدل]
- الأجزاء الجينية لترميز البروتين الفيروسي الداخلي (جزيء RNA): (M ، NP ، NS ، PA ، PB1 ، PB2).[15]
مصفوفة الترميز الجينية[عدل]
- رموز M لبروتينات المصفوفة (M1 و M2) التي تشكل إلى جانب البروتينين السطحيين (hemagglutinin وneuraminidase)، كبسولة (طبقة واقية) للفيروس. يتم ترميزه باستخدام إطارات قراءة مختلفة من نفس شريحة RNA.
- M1 هو بروتين يرتبط بالرنا الفيروسي.
- M2 هو بروتين يزيل الفيروس، وبالتالي يعرض محتوياته (شرائح RNA الثمانية) إلى سيتوبلازم الخلية المضيفة. بروتين الغشاء M2 هو قناة أيونية مطلوبة للعدوى الفعالة.[16] يرتبط استبدال الأحماض الأمينية (Ser31Asn) في M2 ببعض الأنماط الجينية H5N1 بمقاومة الأمانتادين.[17]
الترميز الجيني للبروتين النووي[عدل]
- رموز NP للبروتين النووي.
- NS: رموز NS لاثنين من البروتينات غير الهيكلية (NS1 و NS2 - كانت تسمى سابقًا NEP). «كانت الإمراض المسببة لفيروس الإنفلونزا مرتبطة بالجين غير البنيوي لفيروس H5N1 / 97».[18]
- NS1: غير بنيوي: نواة؛ الآثار على النقل الخلوي للـ RNA، الربط، الترجمة. بروتين مضاد للانترفيرون.[19] قد تكون "NS1 لفيروسات H5N1 المسببة للأمراض الشديدة الانتشار المنتشرة في الدواجن والطيور المائية في جنوب شرق آسيا مسؤولة عن استجابة محسنة للالتهاب الخلوي (خاصة TNFa) التي تسببها هذه الفيروسات في البلاعم البشرية".[4] يتميز H5N1 NS1 بتغيير حمض أميني واحد في الموضع 92. من خلال تغيير الحمض الأميني من حمض الجلوتاميك إلى حمض الأسبارتيك، تمكن الباحثون من إلغاء تأثير H5N1 NS1. أدى تغير الأحماض الأمينية الفردية في جين NS1 إلى زيادة الإمراضية لفيروس إنفلونزا H5N1 بشكل كبير."[20]
- NEP: «بروتين التصدير النووي (NEP، الذي كان يشار إليه سابقًا باسم بروتين NS2) يتوسط تصدير vRNPs».[21]
الترميز الجيني للبوليميراز[عدل]
- رموز PA لبروتين PA الذي هو مكون حاسم من البلمرة الفيروسية.
- رموز PB1 لبروتين PB1 وبروتين PB1-F2.
- بروتين PB1 هو مكون حاسم من البلمرة الفيروسية.
- يتم تشفير بروتين PB1-F2 بواسطة إطار قراءة مفتوح بديل للجزء PB1 RNA و «يتفاعل مع مكونين من مركب مسام انتقال نفاذية الميتوكوندريا، ANT3 و VDCA1 ، [تحس] الخلايا إلى موت الخلايا. يساهم PB1-F2 على الأرجح في الإمراضية الفيروسية وقد يكون له دور مهم في تحديد شدة جائحة الأنفلونزا.»[4] تم اكتشاف هذا من قبل "Chen et al". وذكرت في مجلة الطبيعة.[5] «بعد مقارنة الفيروسات من فاشية H5N1 بهونج كونج 1997، تم العثور على تغير واحد في الأحماض الأمينية (N66S) في تسلسل PB1-F2 في الموضع 66 والذي ارتبط بالإمراض. تم العثور على نفس هذا التغيير في الأحماض الأمينية (N66S) أيضًا في بروتين PB1-F2 لفيروس A / Brevig Mission / 18 الوبائي لعام 1918».[6]
- رموز PB2 لبروتين PB2 وهو مكون حاسم من البلمرة الفيروسية. اعتبارًا من عام 2005، كان 75 ٪ من فيروس H5N1 البشري المعزول من فيتنام بها طفرة تتكون من Lysine في المادة المتبقية 627 في بروتين PB2؛ والذي يعتقد أنه يسبب مستويات عالية من الضراوة.[22] حتى H5N1، كان لجميع فيروسات إنفلونزا الطيور المعروفة Glu في الموضع 627، في حين أن جميع فيروسات الإنفلونزا البشرية كانت تحتوي على ليسين. اعتبارًا من عام 2007، «يمثل ظهور 3 (أو أكثر) من العوائق من EMA [EMA = E urope ، M iddle East ، A frica] فرصًا جديدة متعددة لأنفلونزا الطيور (H5N1) لتتطور إلى سلالة وبائية بشرية. على عكس السلالات المنتشرة في جنوب شرق آسيا، تُشتق فيروسات EMA من سلف لديه طفرة PB2 627K. من المتوقع أن يكون لهذه الفيروسات خصائص تكاثر محسنة في الثدييات، وفي الواقع تزامن انتشار EMA مع الظهور السريع للحالات في الثدييات - بما في ذلك البشر في تركيا ومصر والعراق وجيبوتي والقطط في ألمانيا والنمسا والعراق. لسوء الحظ، تبدو الفيروسات من نوع EMA خبيثة مثل السلالات الآسيوية الخالصة: من بين 34 إصابة بشرية خارج آسيا حتى منتصف عام 2006، كانت 15 حالة مميتة.»[23] يُعتقد أن Lys عند PB2-627 يمنح فيروسات H5N1 المسببة للطيور ميزة النمو الفعال في الجهاز التنفسي العلوي والسفلي للثدييات.[24]
طفره[عدل]
تتميز فيروسات الإنفلونزا بمعدل تحور مرتفع نسبيًا يميز فيروسات الرنا. إن تجزيء جينوم الإنفلونزا يسهل إعادة التركيب الجيني عن طريق إعادة ترتيب المقطع في العوائل المصابة بفيروسين مختلفين للأنفلونزا في نفس الوقت. يمكن لفيروسات H5N1 إعادة تصنيف الجينات مع سلالات أخرى تشارك في إصابة كائن مضيف، مثل الخنازير أو الطيور أو الإنسان، وتتحول إلى شكل يمكن أن ينتقل بسهولة بين البشر. هذا هو واحد من العديد من المسارات الممكنة للوباء.
تعود قدرة سلالات الإنفلونزا المختلفة على إظهار انتقائية الأنواع إلى حد كبير إلى الاختلاف في جينات هيماجلوتينين. يمكن أن تؤدي الطفرات الجينية في جين hemagglutinin الذي يسبب استبدال الأحماض الأمينية المفردة إلى تغيير قدرة بروتينات hemagglutinin الفيروسية بشكل كبير على الارتباط بالمستقبلات على سطح الخلايا المضيفة. يمكن لهذه الطفرات في فيروسات إنفلونزا الطيور H5N1 أن تغير سلالات الفيروس من كونها غير فعالة في إصابة الخلايا البشرية إلى أن تكون فعالة في التسبب في العدوى البشرية مثل أنواع فيروسات الإنفلونزا البشرية الأكثر شيوعًا.[25] هذا لا يعني أن إحلال الأحماض الأمينية يمكن أن يسبب جائحة، ولكنه يعني أن إحلال الأحماض الأمينية يمكن أن يتسبب في أن يصبح فيروس إنفلونزا الطيور غير الممرض لدى البشر ممرضًا لدى البشر.
H3N2 («إنفلونزا الخنازير») متوطن في الخنازير في الصين، وقد تم اكتشافه في الخنازير في فيتنام، مما يزيد من المخاوف من ظهور سلالات جديدة. كانت السلالة السائدة لفيروس الإنفلونزا السنوي في يناير 2006 هي H3N2، وهي الآن مقاومة للأدوية القياسية المضادة للفيروسات أمانتادين وريمانتادين. إن إمكانية تبادل الجينات H5N1 و H3N2 من خلال إعادة التصنيف هي مصدر قلق كبير. في حالة حدوث إعادة فرز في H5N1 ، فقد تظل نوعًا فرعيًا H5N1، أو يمكن أن تغير الأنواع الفرعية، كما حدث H2N2 عندما تطورت إلى سلالة H3N2 من إنفلونزا هونج كونج.
احتوت سلالات جائحة H2N2 وH3N2 على أجزاء من الحمض النووي الريبي لفيروس إنفلونزا الطيور. «في حين أن فيروسات الإنفلونزا البشرية الوبائية لعام 1957 (H2N2) و 1968 (H3N2) نشأت بوضوح من خلال إعادة التصنيف بين فيروسات الإنسان وفيروس الطيور، يبدو أن فيروس الإنفلونزا الذي تسبب في» الإنفلونزا الإسبانية «في عام 1918 مشتق بالكامل من مصدر الطيور».[26]
في يوليو 2004، باحثون بقيادة H.Deng من معهد Harbin للأبحاث البيطرية، Harbin، الصين والأستاذ روبرت G. Webster من مستشفى سانت جود لأبحاث الأطفال، ممفيس، تينيسي، أبلغوا عن نتائج التجارب التي تعرضت فيها الفئران تم الحصول على 21 عزلة من سلالات H5N1 المؤكدة من البط في الصين بين عامي 1999 و 2002. ووجدوا «نمطًا زمنيًا واضحًا لزيادة الإمراض تدريجيًا».[27] النتائج التي أبلغ عنها دكتور ويبستر في يوليو 2005 تكشف عن مزيد من التقدم نحو المسببة للأمراض في الفئران وسفك الفيروس الأطول من البط.
سلالة آسيوية ينقسم إنفلونزا الطيور (H5N1) في اثنين من المستضدات. "يتضمن Clade 1 عزلة بشرية وطيور من فيتنام وتايلاند وكمبوديا وعزلات طيور من لاوس وماليزيا. تم تحديد فيروسات Clade 2 لأول مرة في عزلات الطيور من الصين وإندونيسيا واليابان وكوريا الجنوبية قبل انتشارها غربًا إلى الشرق الأوسط وأوروبا وأفريقيا. ووفقاً لمنظمة الصحة العالمية، كانت فيروسات Clade 2 مسؤولة بشكل أساسي عن عدوى H5N1 البشرية التي حدثت خلال أواخر 2005 و 2006. حدد التحليل الوراثي ستة تفرعات فرعية من Clade 2، ثلاثة منها لها توزيع جغرافي متميز وتورطت في إصابات بشرية: الخريطة
- الطبقة الفرعية 1، إندونيسيا.
- الطبقة الفرعية 2، أوروبا والشرق الأوسط وأفريقيا (تسمى EMA).
- الطبقة الفرعية 3، الصين".[28][29][30]
وقد ألقت دراسة عام 2007 التي ركزت على الكود الفرعي EMA مزيدًا من الضوء على طفرات EMA. «العزلات الجديدة الـ 36 المبلغ عنها هنا تزيد بشكل كبير من كمية بيانات تسلسل الجينوم الكامل المتاحة من عزلات إنفلونزا الطيور الأخيرة (H5N1). قبل مشروعنا، احتوى GenBank على 5 جينومات كاملة أخرى من أوروبا للفترة 2004-2006، ولم يكن يحتوي على جينومات كاملة من الشرق الأوسط أو شمال إفريقيا. أظهر تحليلنا عدة نتائج جديدة. أولاً، تقع جميع العينات الأوروبية والشرق أوسطية والأفريقية في كليد متميز عن الكتل الآسيوية المعاصرة الأخرى، وجميعها تشترك في أصل مشترك مع سلالة هونغ كونغ الأصلية لعام 1997. تُظهر أشجار السلالة المبنية على كل من الأجزاء الثمانية صورة متسقة لثلاث سلالات، كما هو موضح في شجرة HA الموضحة في الشكل 1. يحتوي اثنان من الكتل على فيروسات فيتنامية معزولة؛ الأصغر منها، مع 5 فيروسات معزولة، نسمي V1؛ أما الجزء الأكبر، مع 9 فيروسات معزولة، فهو V2. تقع الفيروسات المعزولة الـ 22 المتبقية في طبقة ثالثة مميزة بشكل واضح، تسمى EMA، والتي تضم عينات من أوروبا والشرق الأوسط وأفريقيا. تعرض الأشجار للقطاعات السبعة الأخرى طوبولوجيا متشابهة، مع فصل Clades V1 و V2 و EMA بوضوح في كل حالة. وضعت التحليلات لجميع جينومات الأنفلونزا الكاملة (H5N1) و 589 تسلسل HA Clade EMA متميزًا عن الكتل الرئيسية المتداولة في جمهورية الصين الشعبية وإندونيسيا وجنوب شرق آسيا.»[23]
انظر أيضا[عدل]
قراءة متعمقة[عدل]
- Influenza Report 2006 Online book.
- Ghedin E، Sengamalay NA، Shumway M، Zaborsky J، Feldblyum T، Subbu V، Spiro DJ (نوفمبر 2005). "Large-scale sequencing of human influenza reveals the dynamic nature of viral genome evolution". Nature. ج. 437 ع. 7062: 1162–1166. Bibcode:2005Natur.437.1162G. DOI:10.1038/nature04239. PMID:16208317. presents a summary of what has been discovered in the Influenza Genome Sequencing Project.
- Links and descriptions to abstracts and full texts This bibliography of avian influenza publications was compiled through the cooperative effort of the USGS National Wildlife Health Center and the Wildlife Disease Information Node.
- Search for research publications about H5N1: Entez PubMed
- Beigel JH, Farrar J, Han AM, et al.; Writing Committee of the World Health Organization (WHO) Consultation on Human Influenza A/H5. (سبتمبر 2005). "Avian influenza A (H5N1) infection in humans". N. Engl. J. Med. ج. 353 ع. 13: 1374–85. DOI:10.1056/NEJMra052211. hdl:10722/45195. PMID:16192482.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء عددية: قائمة المؤلفين (link) صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - Evolutionary "Tree of Life" for H5N1:
- Here is the phylogenetic tree of the influenza virus hemagglutinin gene segment. Amino acid changes in three lineages (bird, pig, human) of the influenza virus hemagglutinin protein segment HA1.
- Here is the tree showing the evolution by reassortment of H5N1 from 1999 to 2004 that created the Z genotype in 2002.
- Here is the tree showing evolution by antigenic drift since 2002 that created dozens of highly pathogenic varieties of the Z genotype of avian flu virus H5N1, some of which are increasingly adapted to mammals.
- WHO (PDF) contains latest Evolutionary "Tree of Life" for H5N1 article Antigenic and genetic characteristics of H5N1 viruses and candidate H5N1 vaccine viruses developed for potential use as pre-pandemic vaccines published August 18, 2006
- Hiromoto Y، Yamazaki Y، Fukushima T، وآخرون (مايو 2000). "Evolutionary characterization of the six internal genes of H5N1 human influenza A virus". J. Gen. Virol. ج. 81 ع. Pt 5: 1293–303. DOI:10.1099/0022-1317-81-5-1293. PMID:10769072. مؤرشف من الأصل في 2007-12-19. اطلع عليه بتاريخ 2006-04-10.
- Genome database Page links to the complete sequence of the Influenza A virus (A/Goose/Guangdong/1/96(H5N1)) genome.
روابط خارجية[عدل]
- Influenza Research Database – Database of influenza genomic sequences and related information.
المراجع[عدل]
- ^ ا ب ج The World Health Organization Global Influenza Program Surveillance Network (2005). "Evolution of H5N1 viruses in Asia". Emerging Infectious Diseases. ج. 11 ع. 10: 1515–1526. DOI:10.3201/eid1110.050644. PMC:3366754. PMID:16318689. مؤرشف من الأصل في 2020-04-21.
- ^ WHO (October 28, 2005). "H5N1 avian influenza: timeline" (PDF). مؤرشف من الأصل (PDF) في July 27, 2011. اطلع عليه بتاريخ أكتوبر 2020.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ Canadian Press article Study shows hybrids of bird flu and human flu viruses fit well, could occur published June 1, 2008 نسخة محفوظة يونيو 5, 2008 في Wayback Machine [وصلة مكسورة]
- ^ ا ب ج García-Sastre A (يناير 2006). "Antiviral response in pandemic influenza viruses". Emerging Infect. Dis. ج. 12 ع. 1: 44–7. DOI:10.3201/eid1201.051186. PMC:3291409. PMID:16494716. مؤرشف من الأصل في 2011-04-24.
- ^ ا ب ج Weisan Chen؛ Paul A. Calvo؛ وآخرون (2001). "A novel influenza A virus mitochondrial protein that induces cell death". Nature Medicine. ج. 7 ع. 12: 1306–12. DOI:10.1038/nm1201-1306. PMID:11726970.
- ^ ا ب Scientist Live نسخة محفوظة 2007-10-20 في Wayback Machine article A Single Mutation in the PB1-F2 of H5N1 (HK/97) and 1918 Influenza A Viruses Contributes to Increased Virulence published October 18, 2007
- ^ M. T. Michael Lee, Konrad Bishop, Liz Medcalf, Debra Elton, Paul Digard, and Laurence Tiley (15 يناير 2002). "Definition of the minimal viral components required for the initiation of unprimed RNA synthesis by influenza virus RNA polymerase". Nucleic Acids Research. ج. 30 ع. 2: 429–438. DOI:10.1093/nar/30.2.429. PMC:99831. PMID:11788704.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Alex Greninger (16 يوليو 2004). "The Definition and Measurement of Dangerous Research" (PDF). CISSM Working Paper. مؤرشف من الأصل (PDF) في 2006-11-08. اطلع عليه بتاريخ 2006-12-09.
- ^ Butler D (يناير 2006). "Alarms ring over bird flu mutations". Nature. ج. 439 ع. 7074: 248–9. Bibcode:2006Natur.439..248B. DOI:10.1038/439248a. PMID:16421529.
- ^ H5N1 influenza: A protean pandemic threat نسخة محفوظة 2008-05-13 في Wayback Machine
- ^ Influenza Report 2006 Online book page 51 نسخة محفوظة 2020-04-01 في Wayback Machine
- ^ CIDRAP article Study finds 2 mutations that help H5N1 infect humans published November 21, 2006 نسخة محفوظة 2013-05-03 في Wayback Machine
- ^ Bloomberg News articles Two Bird Flu Gene Mutations Might Lead to Faster Human Spread published November 15, 2006 "نسخة مؤرشفة". مؤرشف من الأصل في 2007-10-09. اطلع عليه بتاريخ 2020-04-21.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ Scidev.net News article Bird flu protein's 'pocket' could inspire better drugs published August 16, 2006 نسخة محفوظة 2008-02-05 في Wayback Machine
- ^ The Threat of Pandemic Influenza: Are We Ready? Page 118 نسخة محفوظة 2020-05-20 في Wayback Machine
- ^ Influenza virus replication in Medical Microbiology, 4th edition edited by Samuel Baron. 1996 Chapter 58. (ردمك 0-9631172-1-1). نسخة محفوظة 2009-05-03 في Wayback Machine
- ^ "H5N1 influenza: a protean pandemic threat". Proc. Natl. Acad. Sci. U.S.A. ج. 101 ع. 21: 8156–61. مايو 2004. Bibcode:2004PNAS..101.8156G. DOI:10.1073/pnas.0402443101. PMC:419573. PMID:15148370. مؤرشف من الأصل في 2008-05-13.
- ^ "Characterization of highly pathogenic H5N1 avian influenza A viruses isolated from South Korea". J. Virol. ج. 79 ع. 6: 3692–702. مارس 2005. DOI:10.1128/JVI.79.6.3692-3702.2005. PMC:1075707. PMID:15731263. مؤرشف من الأصل في 2009-12-03.Also, Pandemic Influenza نسخة محفوظة 2010-01-06 في Wayback Machine Center for Infectious Disease Research & Policy Academic Health Center -- University of Minnesota
- ^ NS1 described in Inhibition by the NS1 protein - Enhanced virulence/viral pathogenesis by enabling the virus to disarm the host cell type IFN defense system Pathobiologics International نسخة محفوظة 2020-05-31 في Wayback Machine
- ^ "The Definition and Measurement of Dangerous Research by Alex Greninger" (PDF). مؤرشف من الأصل (PDF) في 2006-03-06. اطلع عليه بتاريخ 2006-04-10.
- ^ "Influenza B and C virus NEP (NS2) proteins possess nuclear export activities". J. Virol. ج. 75 ع. 16: 7375–83. أغسطس 2001. DOI:10.1128/JVI.75.16.7375-7383.2001. PMC:114972. PMID:11462009.
- ^ The Threat of Pandemic Influenza: Are We Ready? Page 126 نسخة محفوظة 2008-10-11 في Wayback Machine
- ^ ا ب "Genome analysis linking recent European and African influenza (H5N1) viruses". Emerging Infect. Dis. ج. 13 ع. 5: 713–8. مايو 2007. DOI:10.3201/eid1305.070013. PMC:2432181. PMID:17553249.
- ^ Scientist Live نسخة محفوظة 2007-10-18 في Wayback Machine article Growth of H5N1 Influenza A Viruses in the Upper Respiratory Tracts of Mice published October 18, 2007
- ^ "Fatal Evolution of the receptor binding phenotype of influenza A (H5) viruses". Virology. ج. 344 ع. 2: 432–438. 2006. DOI:10.1016/j.virol.2005.08.035. PMID:16226289.
- ^ Harder, T. C.؛ Werner, O. (2006). "Avian Influenza". في Kamps, B. S.؛ Hoffman, C.؛ Preiser, W. (المحررون). Influenza Report 2006. Paris, France: Flying Publisher. ISBN:3-924774-51-X. مؤرشف من الأصل في 2016-05-10. اطلع عليه بتاريخ 2006-04-18.This e-book is under constant revision and is an excellent guide to Avian Influenza
- ^ "The evolution of H5N1 influenza viruses in ducks in southern China". Proc. Natl. Acad. Sci. U.S.A. ج. 101 ع. 28: 10452–7. يوليو 2004. Bibcode:2004PNAS..10110452C. DOI:10.1073/pnas.0403212101. PMC:478602. PMID:15235128.
- ^ "H5N1 Influenza — Continuing Evolution and Spread". N. Engl. J. Med. ج. 355 ع. 21: 2174–7. نوفمبر 2006. DOI:10.1056/NEJMp068205. PMID:17124014.
- ^ "WHO changes H5N1 strains for pandemic vaccines, raising concern over virus evolution". CIDRAP. 18 أغسطس 2006. مؤرشف من الأصل في 2013-05-03.
- ^ "Antigenic and genetic characteristics of H5N1 viruses and candidate H5N1 vaccine viruses developed for potential use as pre-pandemic vaccines" (PDF). WHO. August 18, 2006. مؤرشف من الأصل (PDF) في August 24, 2006. اطلع عليه بتاريخ أكتوبر 2020.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة)