ثنائي ببتيد
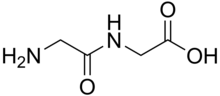
ثنائي الببتيد مركب عضوي مشتق من اثنين من الأحماض الأمينية . يمكن أن تكون الأحماض الأمينية المكونة هي نفسها أو مختلفة. عندما يكون هناك اختلاف ، يمكن أن يكون هناك إيزومرين من ثنائي الببتيد ، اعتمادًا على التسلسل. العديد من ثنائي الببتيدات مهمة من الناحية الفسيولوجية ، وبعضها مهم من الناحية الفسيولوجية والتجارية. من المعروف أن ثنائي الببتيد هو الأسبارتام ، وهو مُحلي صناعي.[1]
ثنائي الببتيدات هي مواد صلبة بيضاء. كثير منها أكثر قابلية للذوبان في الماء من الأحماض الأمينية الأصلية. على سبيل المثال ، يحتوي ثنائي الببتيد Ala-Gln على قابلية ذوبان تبلغ ٥٨٦ جم / لتر أكثر من ١٠ أضعاف قابلية ذوبان Gln (٣٥ جم / لتر). يمكن أن تظهر أيضًا ثباتات مختلفة ، على سبيل المثال فيما يتعلق بالتحلل المائي. Gln لا يتحمل إجراءات التعقيم ، في حين أن هذا ثنائي الببتيد لا يتحمل. نظرًا لأن الببتيدات عرضة للتحلل المائي ، يتم استغلال قابلية الذوبان العالية في الحقن ، أي لتوفير التغذية.
أمثلة[عدل]

قيمة تجارية[عدل]
حوالي ستة ديبيبتيدات ذات أهمية تجارية.[1]
- الأسبارتام ( N - L -α-aspartyl- L -phenylalanine 1-methyl ester) هو مُحلي صناعي.
- كارنوزين (بيتا -alanyl- L -histidine) و الوزي (بيتا -alanyl- N -methyl الحامض الاميني) تتركز بشكل كبير في العضلات والدماغ الأنسجة . يتم استخدامها في الأدوية الرياضية.
- أسيتيل كارنوزين ، منع إعتام عدسة العين
- Ala-Gln and Gly-Tyr ، تسريب [2]
- فال صور ، خافضة للضغط
الببتيدات الأخرى[عدل]
- Homoanserine ( N - (4-aminobutyryl) - L -histidine) هو ثنائي ببتيد آخر تم تحديده في دماغ وعضلات الثدييات.
- Kyotorphin ( L -tyrosyl- L -arginine) هو ثنائي ببتيد نشط عصبي يلعب دورًا في تنظيم الألم في الدماغ.
- Balenine [バレニン] (أو الأفيدين) ( بيتا- ألانيل- N تاو- ميثيل هيستيدين) في عضلات عدة أنواع من الثدييات (بما في ذلك الإنسان) والدجاج .
- Glorin ( N -propionyl-γ- L -glutamyl- L -ornithine-δ-lac ethyl ester) هو ثنائي ببتيد كيميائي لعفن الوحل Polysphondylium violaceum .
- Barettin (cyclo - [(6-bromo-8-en-tryptophan) -arginine]) هو ثنائي ببتيد دوري من الإسفنج البحري Geodia barretti .
- بسودوبرولين
- يشيع استخدام الديالانين كنموذج في الديناميكيات الجزيئية .
إنتاج[عدل]
ثنائي الببتيدات الاصطناعية[عدل]
يتم إنتاج الببتيدات عن طريق اقتران الأحماض الأمينية. يتم تحويل المجموعة الأمينية الموجودة في حمض أميني واحد إلى مادة غير محبة للنواة ويتم إلغاء تنشيط مجموعة الأحماض الكربوكسيلية في الحمض الأميني الثاني باعتبارها إستر الميثيل الخاص بها. يتم بعد ذلك دمج الأحماض الأمينية المعدلة في وجود عامل اقتران ، مما يسهل تكوين رابطة الأميد:
- RCH (NHP) CO 2 H + R'CH (NH 2 ) CO 2 CH 3 → RCH (NHP) C (O) NH (CHR ') CO 2 CH 3 + H 2 O
بعد تفاعل الاقتران هذا ، يتم تحويل مجموعة حماية الأمين P والإستر إلى الأمين الحر وحمض الكربوكسيل ، على التوالي.[3]
بالنسبة للعديد من الأحماض الأمينية ، تكون المجموعات الوظيفية المساعدة محمية . يستخدم تكثيف الأمين والحمض الكربوكسيل لتكوين رابطة الببتيد عمومًا عوامل اقتران لتنشيط حمض الكربوكسيل.[4]
إن تخليق ببتيد بيرجمان أزلاكتون هو تخليق عضوي كلاسيكي لتحضير ثنائي الببتيدات.[1]
التخليق الحيوي[عدل]
يتم إنتاج الببتيدات من عديد الببتيدات عن طريق عمل إنزيم هيدرولاز dipeptidyl peptidase .[5] يتم هضم البروتينات الغذائية إلى ثنائي الببتيدات والأحماض الأمينية ، ويتم امتصاص ثنائي الببتيدات بسرعة أكبر من الأحماض الأمينية ، لأن امتصاصها ينطوي على آلية منفصلة. تنشط الببتيدات الخلايا G الموجودة في المعدة لإفراز الجاسترين .
ديكيتوبيبرازين (ثنائي ببتيدات دورية)[عدل]

Diketopiperazines هي فئة خاصة من ثنائي الببتيدات ، وهي دورية. أنها تشكل منتجات جانبية في تخليق الببتيد. تم إنتاج العديد من الأحماض الأمينية غير المتعارف عليها.[7]
طالع أيضاً[عدل]
المراجع[عدل]
- ^ ا ب ج Yagasaki, Makoto؛ Hashimoto, Shin-ichi (2008). "Synthesis and application of dipeptides; current status and perspectives". From Applied Microbiology and Biotechnology. ج. 81 ع. 1: 13–22. DOI:10.1007/s00253-008-1590-3. PMID:18795289.
- ^ Furst, Peter؛ Pogan, Karin؛ Stehle, Peter (1997). "Glutamine dipeptides in clinical nutrition". Nutrition. ج. 13 ع. 7–8: 731–7. DOI:10.1016/S0899-9007(97)83035-3. PMID:9263278.
- ^ Subirós-Funosas, Ayman El-Faham؛ Fernando Albericio (2013). "Low-epimerization Peptide Bond Formation with Oxyma Pure: Preparation of Z-L-Phg-Val-OMe". Org. Synth. ج. 90: 306. DOI:10.15227/orgsyn.090.0306.
- ^ Jean-Simon Suppo؛ Renata Marcia de Figueiredo؛ Jean-Marc Campagne (2015). "Dipeptide Syntheses via Activated α-Aminoesters". Org. Synth. ج. 92: 296–308. DOI:10.15227/orgsyn.092.0296.
- ^ Steane، Richard. "Hydrolysis of a dipeptide". BioTopics. مؤرشف من الأصل في 2020-11-14. اطلع عليه بتاريخ 2014-07-28.
- ^ Domling A، المحرر (يناير 2013). "Retosiban and Epelsiban: Potent and Selective Orally available Oxytocin Antagonists". Methods and Principles in Medicinal Chemistry: Protein-Protein Interactions in Drug Discovery. Weinheim: Wiley-VCH. ص. 225–256. ISBN:978-3-527-33107-9.
- ^ Borthwick، A. D. (2012). "2,5-Diketopiperazines: Synthesis, Reactions, Medicinal Chemistry, and Bioactive Natural Products". Chem. Rev. ج. 112 ع. 7: 3641–716. DOI:10.1021/cr200398y. PMID:22575049. مؤرشف من الأصل في 2022-04-05.
روابط خارجية[عدل]
- مقدمة عن ثنائي الببتيدات في PeptideGuide.
| ثنائي ببتيد في المشاريع الشقيقة: | |
| |