ثنائي ميثيل فورماميد
| ثنائي ميثيل فورماميد | |
|---|---|
 |
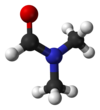 |
| الاسم النظامي (IUPAC) | |
N,N-ثنائي أميد الميثان |
|
| المعرفات | |
| الاختصارات | DMF |
| رقم CAS | 68-12-2 |
| بوب كيم (PubChem) | 6228 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | C3H7NO |
| الكتلة المولية | 73.09 غ/مول |
| المظهر | سائل عديم اللون |
| الكثافة | 0.94 غ/سم3 |
| نقطة الانصهار | - 61 °س |
| نقطة الغليان | 153 °س |
| الذوبانية في الماء | مزوج |
| اللزوجة | 0.92 cP عند 20 °س |
| المخاطر | |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| نقطة الوميض | 58 °س |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
ثنائي ميثيل فورماميد هو مركب عضوي صيغته الكيميائية C3H7NO. ويطلق عليه عادة بشكل مختصر (DMF)، وهو سائل عديم اللون مزوج مع الماء وغالبية السوائل العضوية. يستخدم DMF بشكل شائع كمذيب في التفاعلات الكيميائية. إن ثنائي ميثيل فورماميد النقي عديم الرائحة في حين أن المنتج التجاري أو المتفكك يكون له رائحة السمك بسبب الشوائب من ثنائي ميثيل أمين. واسم DMF مشتق من فورمالدهيد، وأميد حمض فورميك.
ثنائي الميثيل فورماميد هو مذيب قطبي (محب للماء) لا بروتوني ذو نقطة غليان مرتفعة. فهو يسهّل التفاعلات التي تتبع آليات قطبية، مثل تفاعلات SN2. يمكن اصطناع DMF من فورمات الميثيل وثنائي ميثيل أمين أو تفاعل ثنائي ميثيل أمين وأول أكسيد الكربون.[3] يعتبر DMF غير مستقر في وجود مواد قلوية قوية مثل هيدروكسيد الصوديوم أو الحموض القوية مثل حمض هيدروكلوريك أو حمض كبريتيك ويتحلل عائدًا إلى حمض فورميك وثنائي ميثيل أمين، وخاصة في درجات الحرارة المرتفعة.
المراجع
[عدل]- ^ ا ب N,N-DIMETHYLFORMAMIDE (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ Klaus Weissermel, Hans-Jürgen Arpe. Industrial Organic Chemistry: Important Raw Materials and Intermediates. ص. 45–46.
{{استشهاد بكتاب}}: الوسيط غير المعروف|publischer=تم تجاهله (مساعدة)
