داء الأسكارس
| داء الصَفَر | |
|---|---|
| معلومات عامة | |
| الاختصاص | أمراض معدية، وعالم بالديدان الطفيلية |
| من أنواع | داء الأسكاريدا المعدي ، ومرض أنثروبونيوتيك ، والتهاب الديدان الطفيلية المنقولة بالتربة، وداء ديداني[1][2]، ومرض |
| الأسباب | |
| الأسباب | صفر خراطيني |
| طريقة انتقال العامل المسبب للمرض | طريق فموي شرجي |
| المظهر السريري | |
| الأعراض | مغص بطني [2]، وتقيؤ[2]، وغثيان[2]، وألم البطن، وإسهال، وتوعك، وحمى منخفضة ، وشرى، وسعال |
| الإدارة | |
| أدوية | |
| التاريخ | |
| وصفها المصدر | الموسوعة السوفيتية الأرمينية، المجلد الأول |
| تعديل مصدري - تعديل | |
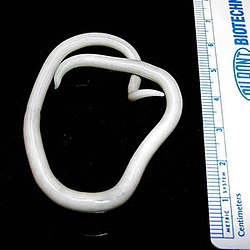
الأَسْكَارِيّة [4] أو دَاءُ الأسْكارِس أو داء الصَفَر هو مرض يصيب الإنسان وينتج عن الديدان الممسودة الطفيلية وهي ما تعرف باسم الصَفَر الخراطيني أو ديدان الأسكارس أو حيات البطن من جنس الصَفَر. ذلك، حيث يرتفع عدد المصابين به وربما يصل إلى ربع سكان العالم[5]، وخاصةً أنه يعد أكثر انتشاراً في المناطق الاستوائية والمناطق التي تعاني من انعدام الاهتمام بالنظافة والصحة العامة. وعلاوةً على ذلك، فهناك نوع آخر طفيلي من جنس دودة الصَفَر يمكن أن يصيب الحيوانات الأليفة التي تربى في المنازل بالمرض.
أسباب العدوى
[عدل]تحدث عدوى الصَفر عن طريق تناول طعام ملوث يحتوي على براز تختبئ به بويضات دودة الصَفر. فبعد ابتلاع تلك البويضات، فإنها تفقس وتخرج منها اليرقات التي تعيش داخل الأمعاء الدقيقة والتي تخترقها بعد ذلك وتسير في الدم لتصل إلى الرئتين وأخيراً تهاجر إلى الجهاز التنفسي. ذلك، حيث يتم ابتلاعها مرة ثانية بعد ذلك لتهبط مرة أخرى إلى الأمعاء لكي تنمو وتتطور حتى يصل طولها 30 سم (12 بوصة) وعندها تستقر بجدار الأمعاء، ومن هنا تبدأ دورة حياتها من جديد.
وعادةً ما تحدث عدوى الصَفر وتتم الإصابة بها دون ظهور أي أعراض دالة على ذلك، ولا سيما إذا كان عدد الديدان قليلاً. ومع ذلك، فإنه قد يصاحبها أعراض مثل التهاب الأمعاء والرئتين والحمى والإسهال ومشكلات أخرى خطيرة قد تتطور إذا اخترقت الديدان أجزاء أخرى في الجسم.
علامات وأعراض الإصابة
[عدل]من الممكن أن يظل مرضى الصَفر فترات زمنية طويلة جداً دون أن تبدو عليهم أعراض الإصابة بها ودون أن يشعروا بذلك. ومع ذلك، فإن هجرة اليرقات خلال مراحل انتقالها داخل جسم الإنسان قد تؤدي إلى التهاب الأحشاء والتهاب الصفاق والتهابات أخرى وتضخم الكبد أو الطحال وتسمم الجسم والالتهاب الرئوي. كما أن كثرة الديدان بشكل كبير قد ينتج عنها الإصابة بسوء التغذية وعدة مضاعفات أخرى - قد تكون خطيرة ومهلكة في بعض الأحيان - منها انسداد الأمعاء بسبب تجمع الديدان في صورة كتل (ويُلاحَظ ذلك خاصةً لدى الأطفال) وانسداد القناة الصفراوية أو قناة البنكرياس. هذا، حيث قد تم اكتشاف وجود ما يزيد عن 796 دودة صَفر خراطيني تزن 550 جرام (19 أوقية) عندما تم تشريح جثة طفلة يبلغ عمرها سنتين من جنوب أفريقيا. وكانت الديدان قد تسببت في التواء المعي اللفائفي وإصابته بالغرغرينا، الأمر الذي فسره الأطباء بأنه السبب الذي أفضى إلى وفاة الطفلة.[6]
هذا، وتعتمد الصَفَرة في معظم غذائها على الطعام المهضوم بشكل جزئي في أمعاء الفرد العائل لها. ومن المعروف إلى حد ما أنها عندما تخترق الغشاء المخاطي للأمعاء يسيل منه الدم الذي تتغذى عليه، ولكن هذا لا يعد مصدر غذائها الرئيسي.[7]
في كندا في عام 1970، قام طالب دراسات عليا بتلويث طعام زملائه بديدان الصَفر الخراطيني. وأصبح أربعة أفراد من الضحايا في حالة صحية خطيرة بينما عانى اثنان آخران منهم من قصور حاد في التنفس.[8][9]
آلية تطور الصَفَرة
[عدل]دورة حياة الصَفَرة
[عدل]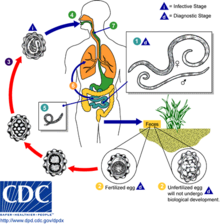
إن أول ظهور لبويضات الاسكارس في البراز يكون خلال فترة تتراوح من 60-70 يومًا. وبالنسبة ليرقات الاسكارس، تبدأ أعراض الإصابة بها في الظهور خلال فترة تتراوح من 4-16 يومًا إثر انتقال العدوى والإصابة بها. وهناك أعراض أخرى تشمل حدوث اضطراب في الجهاز الهضمي وآلام في المعدة والأمعاء ومغص بالبطن وقيء وحمى ورؤية ديدان حية تخرج من الجسم في البراز. وقد يعاني بعض المرضى من أعراض الالتهاب الرئوي أو الاضطرابات العصبية أثناء رحلة اليرقات وانتقالها داخل الجسم. ومع ذلك، فعلى وجه العموم قد يكون هناك عدد قليل من الأعراض الدالة على الإصابة بالاسكارس أو لا يوجد أي أعراض. إن تجمع الديدان في صورة كتل من الممكن أن يؤدي إلى انسداد الأمعاء، كما أن رحلة اليرقات داخل الجسم قد تسبب الالتهاب الرئوي وكثرة اليوزينيات في الدم (ارتفاع عدد كريات الدم البيضاء الحامضية).
مصدر الإصابة بالاسكارس
[عدل]تنتقل عدوى الاسكارس عن طريق ملامسة سطح أو تربة ملوثة ببراز - أو تناول أي منتجات فاكهة أو خضراوات قد نبتت بتلك التربة - يحتوي على بويضات الاسكارس. كما أن تناول تلك البويضات الناقلة للعدوى والتي يرجع مصدرها إلى تربة ملوثة ببراز البشر أو انتقالها من خلال تناول الخضراوات والمياه الملوثة يعد السبب الرئيسي للإصابة بالاسكارس. وعلاوةً على ذلك، فإن الملامسة المباشرة للحيوانات الأليفة التي كانت تعيش من قبل في بيئة ملوثة قد تؤدي إلى انتشار العدوى، بينما تؤدي الحيوانات الأليفة التي تعد معقلاً لنوع آخر من الديدان المستديرة إلى عدوى الإصابة بنوع آخر من الديدان (مثل السهمية الكلبية أو ما تعرف بدودة الكلب، وغير ذلك) كما يحدث أحيانًا مع مروضي الخيول.
وإضافةً إلى ذلك، فقد ينتقل المرض أيضًا من خلال إعادة تدوير مياه الصرف الصحي على المستوى المحلي لري حقول المحاصيل الزراعية. ويعد هذا أمرًا شائعًا إلى حد بعيد في الاقتصاديات الصناعية الناشئة، مما ينطوي على مخاطر جمة لا تهدد مبيعات المحاصيل المحلية فحسب ولكن تهدد أيضًا الصادرات من الخضراوات الملوثة. لقد بدا أن ظهور تفشي مرض الاسكارس في إيطاليا في عام 1986 كان يرجع إلى إعادة تدوير مياه الصرف الصحي بطريقة غير مسئولة واستخدامها في ري وزراعة صادرات منطقة البلقان من الخضراوات.[10]
وتجدر الإشارة إلى أنه من المستحيل انتقال عدوى الاسكارس بين البشر من شخص إلى آخر عن طريق الملامسة أو الاتصال المباشر.[11]
التشخيص
[عدل]عادةً ما يتم تشخيص الإصابة بالاسكارس مصادفةً وذلك عند رؤية الفرد المصاب مرور بعض الديدان في البراز أو القيء. كما يمكن تشخيص الاسكارس من خلال فحص عينات البراز التي يتم أخذها لإجراء فحص معملي للبويضات والطفيليات والتي ستظهر وجود بويضات الاسكارس. وقد توجد اليرقات في إفرازات المعدة أو إفرازات الجهاز التنفسي في حالة الإصابة بمرض الالتهاب الرئوي. هذا، وتبين تحاليل الدم كثرة اليوزينيات في الدم المحيطي. كذلك يمكن تشخيص الاسكارس من خلال عمل أشعة إكس التي توضح أن طول الدودة قد يبلغ من 15-35 سم حيث تملأ الأمعاء وأحيانًا ما تكون في صورة ملتوية (أي تجَمُّع الديدان في صورة كتل).
كيفية الوقاية من الإصابة بالاسكارس
[عدل]تشمل الأساليب التي يمكننا من خلالها وقاية أنفسنا من الإصابة بديدان الاسكارس استخدام الحمامات ودورات المياه للتبرز والتخلص من الفضلات بطريقة آمنة والحفاظ على الأطعمة وتغطيتها منعًا من تلوثها بالأتربة والقاذورات وغسل الفواكه والخضراوات جيدًا بالماء النقي قبل أكلها وغسل اليدين باستمرار قبل الأكل وبعده.
ولا ينبغي تناول الأطعمة إذا سقطت على سطح الأرض دون غسلها أو طهيها ولا سيما في المناطق الموبوءة والحاملة للعدوى. كما ينبغي دائمًا غسل الفواكه والخضراوات جيدًا بالماء النقي قبل تناولها.
طرق العلاج
[عدل]نورد فيما يلي الأدوية الصيدلية التي تستخدم لقتل الديدان المستديرة ويُطلق عليها الأدوية الطاردة للديدان:
- دواء ميبيندازول (فيرموكس) (C16H13N3O2). يعمل هذا الدواء على تثبيت الديدان وشل حركتها وقتلها من خلال منع امتصاص الجلوكوز والعناصر الغذائية الأخرى في أمعاء البالغين المتأثرين بها حيث تستقر هذه الديدان. ويتم تناول هذا الدواء عن طريق الفم على أن تكون الجرعة 100 ملجم كل 12 ساعة لمدة 3 أيام.
- دواء بيبيرازين (C4H10N2.C6H10O4). يسبب هذا الدواء حدوث شلل رخو للاسكارس نتيجة إحصاره للأستيل كولين في عضلاتها، الأمر الذي يؤدي بدوره إلى تثبيط نشاطها.
كما أن التأثير المخدر للدواء يشل حركة الاسكارس مما يمنع هجرتها داخل الجسم عندما يتم تناول أدوية أخرى ذات تأثير ضعيف مثل دواء ثيابندازول. وعلاوةً على ذلك، فإن استخدام هذا الدواء الطارد للديدان يؤدي إلى خروج الاسكارس في البراز. وذلك شريطة أن يتم تناول 75 ملجم لكل واحد كجم (بحد أقصى 3.5 جرام) كجرعة واحدة تؤخذ عن طريق الفم.
- دواء بيرانتيل باموات (Antiminth, Pin-Rid, Pin-X) وهو مضاد للديدان (C11H14N2S.C23H16O6) يزيل استقطاب الوصل العصبي العضلي لحمض النيكوتينيك مما يؤدي إلى حدوث شلل تشنجي لدودة الاسكارس. كما أن العوامل التي تؤدي إلى الشلل التشنجي (تشنج عضلات العنق والفك)، ولا سيما بيرانتيل باموات، قد ينتج عنها الإصابة بانسداد الأمعاء الكلي في حالة كثرة الديدان وتجمعها بالأمعاء. يتم تناول 11 ملجم لكل كجم من هذا الدواء كجرعة واحدة، على ألا تتجاوز الجرعة جرامًا واحدًا.
- دواء ألبيندازول (C12H15N3O2S) هو دواء طارد للديدان وواسع المفعول حيث أنه يقلل من إنتاج مادة ATP (مختصر ثلاثي فوسفات الأدينوزين) في الديدان مما يسبب استنزاف طاقتها وشل حركتها وموتها في النهاية. يؤخذ هذا الدواء جرعة واحدة عن طريق الفم بحيث يبلغ مقدارها 400 ملجم (ولا يُستعمل في فترة الحمل وكذلك مع الأطفال دون العامين).
- دواء ثيابندازول. يؤدي هذا الدواء إلى هجرة دودة الاسكارس إلى المريء، لذلك فإنه عادةً ما يُعْطَى مع دواء بيبيرازين.
- دواء هيكسيل ريزورسينول ذو التأثير الفعال بعد تناول جرعة واحدة منه، كما ورد في: Holt, Jr Emmett L, McIntosh Rustin: Holt's Diseases of Infancy and Childhood: A Textbook for the Use of Students and Practitioners. Appleton and Co, New York,11th edition.
- مادة سانتونين (خلاصة نباتية تستخدم في تركيب الأدوية الطاردة للديدان) تعد أكثر سمًا من دواء هيكسيل ريزورسينول، كما ورد في: Holt, Jr Emmett L, McIntosh Rustin: Holt's Diseases of Infancy and Childhood: A Textbook for the Use of Students and Practitioners. Appleton and Co, New York,, 11th edition.
- زيوت الكينوبوديوم (زيوت السرمق أو نبات رجل الإوز) تعد أكثر سمًا من دواء هيكسيل ريزورسينول، كما ورد في: Holt, Jr Emmett L, McIntosh Rustin: Holt's Diseases of Infancy and Childhood: A Textbook for the Use of Students and Practitioners. Appleton and Co, New York, 11th edition.
هذا، ويمكن أيضًا استخدام أدوية الستيرويدات القشرية في علاج بعض الأعراض، مثل الالتهابات.
لقد استخدم الأمريكيون الأصليون بصورة تقليدية النبات الطبي epazote (الذي ينتمي لفصيلة السرمقيات والمسمى العلمي له Chenopodium ambrisioides) في علاج الديدان، ولكنه لم يكن ذا تأثير قوي مثل المركبات الدوائية.
كيف يتم تشخيص الإسكارس
[عدل]سيطلب الطبيب منك عيّنة براز ترسل إلى المختبر لاختبارها، بعض الأشخاص يلاحظون إصابتهم بالعدوى عند خروج الدودة مع الفضلات أو عندما تخرج عند السعال، وعندها تؤخذ للطبيب للتشخيص. ولا يتم التشخيص بفحص الدم.
ما علاج عدوى الإسكارس
[عدل]تعالج الإصابة بعدوى الإسكارس بتناول عقاقير يصفها الطبيب لمدة يوم إلى ثلاثة أيام، وهي فاعلة، ولكن لها بعض الآثار الجانبية. الطبيب المعالج سيطلب فحصا إضافيا لعيّنات براز بعد 1-2 (أسبوع) من العلاج، إذا كانت العدوى مازالت مستمرة فإن المعالجة ستتكرر.
هل يمكن علاج المرأة الحامل المصابة بعدوى الإسكارس
[عدل]العدوى بديدان الإسكارس خفيفة عموما، ولا تعد من الطوارئ، ويمكن تأجيل علاجها لبعد الولادة إذا لم تكن الإصابة شديدة.
كيف تتجنب عدوى الإسكارس
[عدل]يمكن تجنب عدوى الإسكارس بالأمور التالية:
1. تجنب ملامسة التربة الملوّثة بفضلات الإنسان.
2. عدم التغوط في الأماكن الخارجية العامة.
3. التخلص من حفاظات الأطفال بشكل صحيح.
4. غسل اليدين بالماء والصابون قبل تجهيز الغذاء.
معدل انتشار الإصابة بديدان الاسكارس
[عدل]
لقد وُجد أن ما يقرب من 1.5 مليار فرد مصاب بديدان الاسكارس وخاصةً في قارتي أفريقيا وآسيا.[12][1] كما تعد الإصابة بديدان الاسكارس أحد الأمراض المستوطنة في الولايات المتحدة الأمريكية، بما في ذلك ساحل الخليج الأمريكي، ونيجيريا وجنوب شرق آسيا. ذلك، حيث أشارت إحدى الدراسات إلى أن معدل انتشار الإصابة بديدان الاسكارس في الولايات المتحدة الأمريكية بلغ حوالي 4 ملايين فرد (%2) [8]. وفي إحدى الدراسات الشاملة لإحدى المناطق الريفية التابعة لمقاطعة نوفا سكوتيا الكندية، وُجِد أن %28.1 من بين 431 فرد خضعوا لتحاليل طبية كانت النتيجة إيجابية مؤكدةً إصابتهم بديدان الاسكارس ، وكان جميعهم دون العشرين من العمر، في حين أن 276 فرد من أبناء العاصمة هاليفاكس قد تم إجراء تحاليل لهم وكانت النتيجة سلبية.[13] وعلاوةً على ذلك، يشير ترسب بويضات الاسكارس في مياه الصرف الصحي إلى معدل حدوث الإصابة بديدان الاسكارس. وأظهرت دراسة أُجريت في عام 1978 أن حوالي %75 من جميع عينات الرواسب الطينية الناتجة عن مخلفات مياه الصرف الصحي والتي أُخذت من المناطق الحضرية بالولايات المتحدة الأمريكية كانت تحتوي على بويضات الاسكارس ، وأن معدلات تلك البويضات كانت مرتفعة للغاية حيث كان يتراوح عددها من 5 إلى 100 بويضة في كل لتر. أما في مدينة فرانكفورت بولاية إنديانا، فكانت نتيجة %87.5 من العينات التي أُخذت من الرواسب الطينية لمياه الصرف إيجابية مؤكدةً أنها تحتوي على ديدان الاسكارس والديدان السهمية (التوكسوكارا) والديدان السوطية والديدان الشصية. وفي مدينة ماكون بولاية جورجيا، فكانت نتجية عينة واحدة من بين 13 عينة أخرى من العينات التي أُخذت من التربة إيجابية حيث أنها كانت تحمل الاسكارس. وبالنسبة لمياه الصرف الصحي المحلية بمدينة الرياض في المملكة العربية السعودية، فقد تم الكشف عن وجود ما يزيد عن 100 بويضة في كل لتر من مياه الصرف [14]، أما في جمهورية تشيكوسلوفاكيا فكانت النتيجة مرتفعة للغاية حيث تراوح عدد البويضات ما بين 240 و1050 بويضة في لتر مياه الصرف الواحد.[15]
وجدير بالذكر أنه يمكن غالبًا تشخيص الإصابة بديدان الاسكارس من خلال الفحص المعملي لعينات الطعام للتأكد من وجود بويضات الديدان. وفي إحدى الدراسات الميدانية بالعاصمة مراكش في المغرب حيث تُستخدم مياه الصرف الصحي غير المعالجة في تسميد أراضي المحاصيل الزراعية، تم اكتشاف وجود بويضات الاسكارس بمعدل 0.18 بويضة في كل كيلوجرام من البطاطس و0.27 بويضة في كل كيلوجرام من اللفت و4.63 بويضة في كل كيلوجرام من النعناع و0.7 بويضة في كل كيلوجرام من الجزر و1.64 بويضة في كل كيلوجرام من الفجل.[16] وأظهرت دراسة أخرى مماثلة أُجريت على المنطقة نفسها أن هناك %73 من الأطفال العاملين في هذه المزارع كانوا يعانون من الديدان الطفيلية، ولا سيما ديدان الاسكارس ، ومن المحتمل أن يرجع ذلك إلى تعرضهم لمياه الصرف الصحي غير المعالجة.
المجتمع والثقافة
[عدل]نقاط أخرى مهمة
[عدل]- قد تؤدي الإصابة بديدان الاسكارس إلى المعاناة من بعض أنواع الحساسية مثل الحساسية من الجمبري والحساسية من عثة الغبار وينتج ذلك عن المستضد المشترك؛ ألا وهو بروتين التروبوميوزين.
- تتمتع ديدان الاسكارس بكراهيتها الشديدة لبعض مواد التخدير العامة مما يؤدي إلى خروجها من الجسم، أحيانًا عن طريق الفم.[17]
| الجنس والنوع | اسكارس لمبريكويدس |
|---|---|
| الاسم الشائع | أكبر أنواع الديدان المستديرة المعوية |
| العامل المسبب للإصابة: | الإصابة بديدان الاسكارس |
| مرحلة الإصابة | البويضات الملقحة |
| العائل النهائي | الإنسان |
| بوابة الدخول | الفم |
| طريقة الانتقال | تناول البويضات الملقحة عن طريق تناول الأطعمة أو المياه الملوثة |
| الموطن | الأمعاء الدقيقة |
| المرحلة الممرضة | الديدان اليافعة واليرقات |
| طريقة الالتصاق | الالتصاق في ثنيات الغشاء المخاطي للأمعاء عن طريق الضغط |
| مصدر الغذاء | تتغذى على الكيموس (مادة شبه سائلة وسميكة القوام ناتجة عن عملية الهضم الجزئي للغذاء في المعدة.) |
| أعراض المرض ومضاعفاته | مرور اليرقات إلى الرئة مسببة الالتهاب الرئوي، ومتلازمة لوفلر؛ أما الديدان اليافعة فتسبب انسداد الأمعاء وخراج الكبد والتهاب الزائدة الدودية. وتتشابه في مرحلة مرورها في الدم إلى الرئة مع الديدان الشصية (الصنارية) والديدان الاسطوانية البرازية. |
| التشخيص المعملي | أساليب التركيز والفحص المباشر لمسحة البراز: طريقة كاتوكاتز |
| الأدوية المستخدمة في العلاج | ألبيندازول أو ميبيندازول أو بيرانتيل باموات |
| وصف تشخيصي لدودة الاسكارس اليافعة | أنثى الاسكارس يكون لديها فتحة تناسلية واضحة |
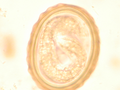
| وصف تشخيصي لبويضة الاسكارس | بويضة لها قشرة خارجية متعرجة وزلالية |
الأبحاث
[عدل]هناك نموذجان من الحيوانات التي أصيبت بديدان الاسكارس وخضعت للدراسة والبحث:
- Howes HL (يونيو 1971). "Anthelmintic studies with pyrantel. II. Prophylactic activity in a mouse-[[ascaris suum]] test model". J. Parasitol. The Journal of Parasitology, Vol. 57, No. 3. ج. 57 ع. 3: 487–93. DOI:10.2307/3277899. PMID:5090955. مؤرشف من الأصل في 2016-04-09.
{{استشهاد بدورية محكمة}}: تعارض مسار مع وصلة (مساعدة) - Lichtensteiger CA, DiPietro JA, Paul AJ, Neumann EJ, Thompson L (أبريل 1999). "Persistent activity of doramectin and ivermectin against Ascaris suum in experimentally infected pigs". Vet. Parasitol. ج. 82 ع. 3: 235–41. DOI:10.1016/S0304-4017(99)00018-7. PMID:10348103. مؤرشف من الأصل في 2019-12-18.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link)
معرض صور
[عدل]انظر أيضًا
[عدل]- أسكارس
- الإصابة بالدودة الشريطية.
- الإصابة بالديدان السهمية .
- حادث التسمم الناتج عن الإصابة بديدان الاسكارس في عام 1970 .
المراجع
[عدل]- ^ Monarch Disease Ontology release 2018-06-29 (ط. 2018-06-29)، 29 يونيو 2018، QID:Q55345445
- ^ ا ب Disease Ontology (بالإنجليزية), 27 May 2016, QID:Q5282129
- ^ WikiSkripta (بالتشيكية والسلوفاكية), ISSN:1804-6517, QID:Q9049250
- ^ المعجم الكبير لمجمع اللغة العربية في مصر حرف الهمزة ص 292
- ^ Williams-Blangero S, VandeBerg JL, Subedi J؛ وآخرون (أبريل 2002). "Genes on chromosomes 1 and 13 have significant effects on Ascaris infection". Proc. Natl. Acad. Sci. U.S.A. ج. 99 ع. 8: 5533–8. DOI:10.1073/pnas.082115999. PMC:122804. PMID:11960011. مؤرشف من الأصل في 2019-12-18.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Baird JK, Mistrey M, Pimsler M, Connor DH (مارس 1986). "Fatal human ascariasis following secondary massive infection". Am. J. Trop. Med. Hyg. ج. 35 ع. 2: 314–8. PMID:3953945. مؤرشف من الأصل في 2019-12-18.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Ascaris lumbricoides". مؤرشف من الأصل في 2008-06-01.
- ^ James A. Phills et al., Pulmonary Infiltrates, Asthma and Eosinophilia due to Ascaris Suum Infestation in Man, 286 New England Journal of Medicine 965-70 (1972)
- ^ FDA/CFSAN Risk Assessment for Food Terrorism and Other Food Safety Concerns نسخة محفوظة 13 مايو 2009 على موقع واي باك مشين.
- ^ Pawlowski، ZS (1986). "Ascariasis and sewage in Europe". في Block JC (المحرر). Epidemiological Studies of Risks Associated With the Agricultural Use of Sewage Sludge: Knowledge and Needs (EUR). Elsevier Science Pub Co. ص. 83–93. ISBN:1-85166-035-6.
{{استشهاد بكتاب}}: الوسيط author-name-list parameters تكرر أكثر من مرة (مساعدة) - ^ "Ascaris Infection Fact Sheet". مؤرشف من الأصل في 2010-05-31.
- ^ Crompton DW (يونيو 1999). "How much human helminthiasis is there in the world?". J. Parasitol. The Journal of Parasitology, Vol. 85, No. 3. ج. 85 ع. 3: 397–403. DOI:10.2307/3285768. PMID:10386428. مؤرشف من الأصل في 2019-04-27.
- ^ Embil JA, Pereira LH, White FM, Garner JB, Manuel FR (يوليو 1984). "Prevalence of Ascaris lumbricoides infection in a small Nova Scotian community". Am. J. Trop. Med. Hyg. ج. 33 ع. 4: 595–8. PMID:6476203. مؤرشف من الأصل في 2019-12-18.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Bolbol AS (1992). "Risk of contamination of human and agricultural environment with parasites through reuse of treated municipal wastewater in Riyadh, Saudi Arabia". J Hyg Epidemiol Microbiol Immunol. ج. 36 ع. 4: 330–7. PMID:1300348.
- ^ Horák P (1992). "Helminth eggs in the sludge from three sewage treatment plants in Czechoslovakia". Folia Parasitol. ج. 39 ع. 2: 153–7. PMID:1644362.
- ^ Habbari K, Tifnouti A, Bitton G, Mandil A (سبتمبر 1999). "Helminthic infections associated with the use of raw wastewater for agricultural purposes in Beni Mellal, Morocco". East. Mediterr. Health J. ج. 5 ع. 5: 912–21. PMID:10983530.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Wu ML, Jones VA (يناير 2000). "Ascaris lumbricoides". Arch. Pathol. Lab. Med. ج. 124 ع. 1: 174–5. PMID:10629158. مؤرشف من الأصل في 2020-03-04.
وصلات خارجية
[عدل]- Video يعرض كيفية التخلص من ديدان اسكارس لمبريكويدس بواسطة منظار
- صور (تحذير: مليئة بالرسوم التوضيحية): [2] و [3]
- مراكز مكافحة الأمراض والوقاية منها DPDx Parasitology Diagnostic Web Site
- داء الاسكارس: Radiology and color pathology pictures from MedPix