داساتينيب
| داساتينيب | |
|---|---|
| الاسم النظامي | |
| N-(2-chloro-6-methylphenyl)-2-[[6-[4-(2-hydroxyethyl)- 1-piperazinyl]-2-methyl-4-pyrimidinyl]amino]-5-thiazole carboxamide monohydrate |
|
| اعتبارات علاجية | |
| اسم تجاري | Sprycel |
| ASHPDrugs.com | أفرودة |
| مدلاين بلس | a607063 |
| الوضع القانوني | وكالة الأدوية الأوروبية:وصلة، إدارة الغذاء والدواء:وصلة |
| فئة السلامة أثناء الحمل | D (أستراليا) D (الولايات المتحدة) |
| طرق إعطاء الدواء | By mouth (مضغوط (دواء)) |
| بيانات دوائية | |
| ربط بروتيني | 96% |
| استقلاب (أيض) الدواء | كبد |
| عمر النصف الحيوي | 1.3 to 5 hours |
| الإخراج | Faecal (85%), كلية (4%) |
| معرّفات | |
| CAS | 302962-49-8 |
| ك ع ت | L01L01XE06 XE06 |
| بوب كيم | CID 3062316 |
| IUPHAR | 5678 |
| ECHA InfoCard ID | 100.228.321 |
| درغ بنك | DB01254 |
| كيم سبايدر | 2323020 |
| المكون الفريد | X78UG0A0RN |
| كيوتو | D03658 |
| ChEBI | CHEBI:49375 |
| ChEMBL | CHEMBL1421 |
| بيانات كيميائية | |
| الصيغة الكيميائية | C22H26ClN7O2S |
| الكتلة الجزيئية | 488.01 g/mol |
| تعديل مصدري - تعديل | |
داساتينيب ، يباع تحت اسم العلامة التجارية سبريسل، وهو العلاج الكيميائي الذي يستخدم لعلاج حالات معينة من سرطان الدم النقوي المزمن وسرطان الدم الليمفاوي الحاد .[1] على وجه التحديد يتم استخدامه لعلاج حالات ايجابية كروموسوم فيلادلفيا.[1] يؤخذ عن طريق الفم .[1] وتشمل الآثار الجانبية الشائعة انخفاص خلايا الدم البيضاء، وانخفاض الصفائح الدموية، وفقر الدم، والتورم، والطفح الجلدي، والإسهال.[1] الآثار الجانبية الشديدة قد تشمل النزيف، وذبحة رئوية، وفشل القلب، ومتلازمة عدم انتظام ضربات القلب.[1] الاستخدام أثناء الحمل قد يؤدي إلى إلحاق الضرر بالطفل.[1] وهو مثبط كيناز التيروزين .[1] تمت الموافقة على داساتينيب للاستخدام الطبي في الولايات المتحدة في عام 2006.[1] وهو مدرج في قائمة الأدوية الأساسية لمنظمة الصحة العالمية، وهي الأدوية الأكثر فعالية وآمنة اللازمة في النظام الصحي.[2] في المملكة المتحدة، اعتبارا من عام 2015، كانت تكاليف الدواء حوالي 2,505.00 جنيه شهريا من العلاج.[3] وقالت شركة هندية أنها يمكن أن تجعل نسخة عامة بقيمة 4 دولار للجرعة الواحدة .[4]
الاستخدامات الطبية
[عدل]يستخدم داساتينيب لعلاج الناس الذين يعانون من سرطان الدم النخاعي المزمن والأشخاص الذين يعانون من سرطان الدم الليمفاوي الحاد وللاشخاص إيجابيوا الكروموسوم فيلادلفيا .[5]
الآثار السلبية
[عدل]كان لانخفاض عدد كريات الدم البيضاء و لوكيميا الدم النخاعي آثارا سامة شائعة . خمسة عشر شخصا (من أصل 84، أي 18٪) في الدراسة المذكورة أعلاه قاموا بتصوير الانضباب الجنبي، والذي كان أحد الآثار الجانبية المشتبه بها لداساتينيب . بعض من هؤلاء الناس يتطلب استخدامهم لثوراسنتيسيس أو بليورودسيس لعلاج الانجرافات. وتشمل الأحداث السلبية الأخرى الإسهال من خفيف إلى معتدل، والصداع . وهناك عدد قليل من الناس اظهرت الاختبارات حدوث مشاكل في وظائف الكبد التي عادت إلى وضعها الطبيعي دون تعديلات الجرعة. لوحظ أيضا نقص كلس الدم الخفيف، دون أن يسبب أي مشاكل كبيرة. تم العثور على عدة حالات من ارتفاع ضغط الدم الشرياني الرئوي في الأشخاص الذين عولجوا مع داساتينيب .[6] في 11 تشرين الأول / أكتوبر 2011، أعلنت إدارة الغذاء والدواء الأمريكية أن داساتينيب قد يزيد من خطر وجود حالة نادرة ولكنها خطيرة حيث يكون هناك ارتفاع غير طبيعي في ضغط الدم لشرايين الرئتين (ارتفاع ضغط الدم الرئوي) . قد تشمل أعراض ارتفاع ضغط الدم الرئوي ضيق التنفس، والتعب، وتورم الجسم (مثل الكاحلين والساقين).وقد أضيفت معلومات حول هذا الخطر إلى قسم التحذيرات والاحتياطات .[7]
علم الصيدلة
[عدل]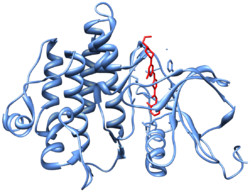
الأهداف الرئيسية لداساتينيب هي («كروموسوم فيلادلفيا»)، مستقبلات إفرين، والعديد من كينازات التيروزين الأخرى.
التاريخ
[عدل]تم تطوير داساتينيب بالتعاون مع بريستول مايرز سكويب وأوتسوكا فارماسيوتيكال Co.[9] ، وتم تسميته لباحث بريستول مايرز سكويب الباحث جاغاباندو داس، الذي يقول أن الدواء لن يكون قد ظهر إلى حيز الوجود، لولا بعض الافتراضات الأساسية للكيميائيين الطبيين في الوقت الذي توقف فيه التقدم في تطوير الجزيء .[10]
التكلفة
[عدل]اعترض الاتحاد لعلاج السرطان بأسعار معقولة على داساتينيب، في رسالة إلى الممثل التجاري للولايات المتحدة. ويبلغ متوسط سعر الجملة في الولايات المتحدة 367 دولارا في اليوم، أي ضعف السعر في البلدان الأخرى ذات الدخل المرتفع. والسعر في الهند، حيث يبلغ متوسط الدخل السنوي للفرد الواحد 570 1 دولارا . عرضت الشركات المصنعة الهندية تقديم إصدارات عامة تكلفتها 4 دولارات في اليوم، ولكن تحت ضغط من الولايات المتحدة، رفضت وزارة السياسة الصناعية والترويج الصناعي إصدار ترخيص إلزامي.[4]
برست بريستول مايرز سكويب ارتفاع أسعار الأدوية السرطانية مع ارتفاع تكاليف البحث والتطوير، ولكن الاتحاد من علاج السرطان بأسعار معقولة وقال ان معظم تكاليف البحث والتطوير جاءت من الحكومة الأمريكية، بما في ذلك المعاهد الوطنية للصحة بتمويل البحوث والتجارب السريرية، و 50٪ الائتمان الضريبي. في انكلترا وويلز، أوصى المعهد الوطني للصحة والتميز الرعاية ضد داساتينيب بسبب ارتفاع نسبة التكلفة والفوائد.[4]
و قال الاتحاد من أجل علاج السرطان بأسعار معقولة أن «النزاع داساتينيب يوضح أوجه القصور في السياسة التجارية الأمريكية وأثرها على مرضى السرطان» .[4]
المراجع
[عدل]- ^ ا ب ج د ه و ز ح "Dasatinib". The American Society of Health-System Pharmacists. مؤرشف من الأصل في 2017-12-10. اطلع عليه بتاريخ 2017-12-08.
- ^ "WHO Model List of Essential Medicines (20th List)" (PDF). World Health Organization. مارس 2017. مؤرشف من الأصل (PDF) في 2017-10-25. اطلع عليه بتاريخ 2017-06-29.
- ^ British national formulary : BNF 69 (ط. 69). British Medical Association. 2015. ص. 614. ISBN:9780857111562. مؤرشف من الأصل في 2022-06-14.
- ^ ا ب ج د Cohen، D (4 نوفمبر 2014). "US trade rep is pressing Indian government to forbid production of generic cancer drug, consortium says". BMJ (Clinical research ed.). ج. 349: g6593. PMID:25370846.
- ^ Keating، GM (يناير 2017). "Dasatinib: A Review in Chronic Myeloid Leukaemia and Ph+ Acute Lymphoblastic Leukaemia". Drugs. ج. 77 ع. 1: 85–96. DOI:10.1007/s40265-016-0677-x. PMID:28032244.
- ^ "NHS - Healthcare News". مؤرشف من الأصل في 2013-05-05. اطلع عليه بتاريخ 2018-01-27.
- ^ FDA: Sprycel (dasatinib): Drug Safety Communication - Risk of Pulmonary Arterial Hypertension, 10/11/2011. نسخة محفوظة 12 مارس 2017 على موقع واي باك مشين. [وصلة مكسورة]
- ^ Tokarski، J. S.؛ Newitt، J. A.؛ Chang، C. Y.؛ Cheng، J. D.؛ Wittekind، M.؛ Kiefer، S. E.؛ Kish، K.؛ Lee، F. Y.؛ Borzillerri، R.؛ Lombardo، L. J.؛ Xie، D.؛ Zhang، Y.؛ Klei، H. E. (2006). "The Structure of Dasatinib (BMS-354825) Bound to Activated ABL Kinase Domain Elucidates Its Inhibitory Activity against Imatinib-Resistant ABL Mutants". Cancer Research. ج. 66 ع. 11: 5790–5797. DOI:10.1158/0008-5472.CAN-05-4187. PMID:16740718.
- ^ https://www.otsuka.co.jp/en/company/release/2015/0302_01.html, http://news.bms.com/press-release/rd-news/fda-approves-us-product-labeling-update-sprycel-dasatinib-include-three-year-f نسخة محفوظة 20 سبتمبر 2018 على موقع واي باك مشين., http://news.bms.com/press-release/financial-news/bristol-myers-squibb-announces-extension-us-agreement-abilify-and-estab نسخة محفوظة 20 سبتمبر 2018 على موقع واي باك مشين.
- ^ Drahl، Carmen (16 يناير 2012). "How Jagabandhu Das made dasatinib possible". The Safety Zone blog. مجلة أخبار الكيمياء والهندسة. مؤرشف من الأصل في 2017-12-10. اطلع عليه بتاريخ 2016-08-29.
روابط خارجية
[عدل]- Sprycel (dasatinib) Official Site
- Prescribing information from Bristol-Myers Squibb
- Summary Basis for Approval from the U.S. Food and Drug Administration Freedom of Information Homepage
- Sprycel Summary of Product Characteristics (from the European Medicines Agency Website)
- Discovery of N-(2-Chloro-6-methyl-phenyl)-2-(6-(4-(2-hydroxyethyl)-piperazin-1-yl)-2-methylpyrimidin-4-ylamino)thiazole-5-carboxamide (BMS-354825), a Dual Src/Abl Kinase Inhibitor with Potent Antitumor Activity in Preclinical Assays

