غاز نبيل
| صنف فرعي من | |
|---|---|
| جزء من | |
| ممثلة بـ | |
| له جزء أو أجزاء |
| Noble gases | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ↓ دورة (جدول دوري) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 | title="Helium: noble gases
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 | title="Neon: noble gases
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 | title="Argon: noble gases
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 | title="Krypton: noble gases
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 | title="Xenon: noble gases
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6 | title="Radon: noble gases
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Legend
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
الغازات النبيلة (تُعرف أيضاً باسم الغازات الخاملة) مجموعة من العناصر الكيميائية ذات خصائص متماثلة، تكون في الظروف القياسية جميعها عديمة الرائحة وعديمة اللون وذات ذرات وحيدة، بالإضافة إلى أن فعاليتها الكيميائية منخفضة جداً. تشمل الغازات النبيلة الهيليوم والنيون والأرغون والكريبتون والزينون والرادون المشع. يُتوقع أيضاً أن يُضمَّ الأوغانيسون إلى الغازات النبيلة، إلا أن كيميائيته لم تُفهَم بَعْد.
الغازات النبيلة تشكل المجموعة 18 من الجدول الدوري، حتى الدورة السادسة. الغازات النبيلة ذات فاعلية كيميائية منخفضة إلى حدٍ كبير، باستثناء ظروف قاسية محددة. يتم استثمار خمول الغازات النبيلة في التطبيقات التي تحتاج إلى عدم حدوث تفاعل، على سبيل المثال يتم استخدام الأرغون في المصابيح الكهربائية لمنع خيوط التنغستن الساخنة من التأكسد، كما يُستخدم الهيليوم في غازات التنفس الغواصين في أعماق البحار لمنع تسمم الأوكسجين والنيتروجين وثنائي أوكسيد الكربون.
يمكن تفسير خصائص الغازات النبيلة بشكل جيد من خلال النظريات الحديثة في البنية الذرية، حيث تحتوي طبقتها الخارجية على عدد «كامل» من الإلكترونات، مما يقلل من ميلها للمشاركة في التفاعلات الكيميائية، لذا من الممكن إعداد بضع مئات من مركبات الغازات النبيلة فقط. تتقارب درجة انصهار ودرجة الغليان في الغازات النبيلة، بحيث أن الفرق بينهما لا يتجاوز 10 درجات مئوية (18 درجة فهرنهايت)، هذا يعني أن تواجدها بشكل سائل يكون ضمن مدى حراري صغير جداً.
يمكن الحصول على النيون والأرغون والكريبتون والزينون من الهواء في وحدة فصل الهواء باستخدام أساليب تسييل الغازات والتقطير بالتجزئة. يمكن الحصول على الهيليوم من حقول الغاز الطبيعي، التي تحتوي على تراكيز عالية من غاز الهيليوم، وذلك باستخدام تقنيات فصل الغاز بالتبريد العميق. أما الرادون فيتم عزله عادةً أثناء التحلل الإشعاعي لمركبات الراديوم أوالثوريوم أواليورانيوم المتحللة. للغازات النبيلة تطبيقات في الصناعات مثل الإضاءة واللحام واكتشاف الفضاء، يستخدم غواصو البحار غاز التنفس هيليوكس عند أعماق أكثر من 55 متر (180 قدم) لحماية الغواص من التسمم بالأوكسجين والأثر المميت للأوكسجين عالي الضغط، وتخدير الأعماق والأثر المشتت المخدّر للنيتروجين في الهواء عند الابتعاد عن عتبة الضغط الجزيئي، بالإضافة إلى التسمم بثنائي أوكسيد الكربون (فرط ثنائي أوكسيد الكربون في الدم) والتأثير الناجم عن فرط ثنائي أوكسيد الكربون في الدم (وهويتضمن الذعر). اِستُبدل الهيدروجين بالهيليوم في المناطيد والبالونات بسبب خطورة قابلية الهيدروجين للاشتعال.
التاريخ
[عدل]تمت ترجمة Noble gas (الغاز النبيل) من الاسم الألماني Edelgas عام 1898 من قبل العالم هوجوإيردمان[1] للإشارة إلى فعاليتها الكيميائية المنخفضة جداً، يشير هذا الاسم كذلك إلى المعادن النبيلة اذات التفاعلية المنخفضة. تمت الإشارة إلى الغازات النبيلة بـالغازات الخاملة إلا أنه تم إهمال هذه التسمية بسبب اكتشاف الكثير من مركبات الغازت النبيلة.[2] اِستُخدِمَ أيضاً مصطلح الغازات النادرة للإشارة إلى الغازات النبيلة[3] إلا أن هذه التسمية غير دقيقة لأن الأرغون يشكل جزءاً ملحوظاً (0.94% من الحجم، و1.3% من الكتلة) من غازات الغلاف الجوي للأرض وذلك يعود إلى تحلل نظير البوتاسيوم 40 المشعّ.[4]
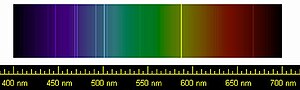
اكتشف الكيميائي والفيزيائي الإنجليزي هنري كافنديش عام 1784 أن الهواء يحتوي على نسبة صغيرة من مادة أقل تفاعلاً من النيتروجين.[5] فيما بعد، اكتشف بيير جانسين وجوزيف نورمان لوكير عنصراً جديداً في 18 أغسطس/آب عام 1868 بينما كانا ينظران إلى طيف إصدار الغلاف اللوني للشمس، وسُمِّي فيما بعد ἥλιος (هيليوس) وتعني الشمس بالإغريقية، ثم سُمي helium (هيليوم) فيما بعد.[6] لم يكن التحليل الكيميائي ممكناً آنذاك، إلا أن الهيليوم اِعتُبِر لاحقاً غازاً نبيلاً. وبعد قرنٍ من ملاحظة هنري كافانديش، اكتشف اللورد ريليه جون ويليام ستروت أن عينات النيتروجين من الهواء كانت ذات كثافة مختلفة عن النتروجين الناتج عن التفاعلات الكيميائية. إلى جانب العالم الإسكتلندي ويليام رامزي في كلية لندن الجامعية افترض اللورد ريليه أن النتروجين المستخرج من الهواء مختلط بغاز آخر، مما أدى إلى إجراء تجربة لفصل هذا الغاز الجديد، نجحت التجربة وأدّت إلى عزل العنصر الجديد وهوالأرغون، الذي سُمِّي نسبة إلى الكلمة الإغريقية ἀργός (أرجوس، وهي تعني «الخمول» أو«الكسول»).[5] أدرك العلماء بهذا الاكتشاف فئة كاملة من الغازات المفقودة من الجدول الدوري. تمكّن رامزي خلال بحثه حول الأرغون من عزل الهيليوم للمرة الأولى أثناء تسخين معدن الكليفيت. تم قبول الهيليوم والأرغون كعناصر عام 1902، وقام ديميتري مندلييف بضمها إلى جدوله كمجموعة رقم 0 في ترتيبه للعناصر، والتي ستصبح فيما بعد الجدول الدوري.[7]
أكمل رامزي البحث عن هذه الغازات باستخدام التقطير بالتجزئة لفصل الهواء السائل إلى مكوناته العديدة. اكتشف رامزي عام 1898 العناصر الكريبتون والنيون والزينون وسماها اشتقاقاً من الكلمات اليوناينة، κρυπτός (كريبتوس، وتعني «المختفي») وνέος (نيوس، وتعني «الجديد») وξένος (كسينوس، وتعني «الغريب») على الترتيب. أما الرادون فقد تم اكتشافه للمرة الأولى عام 1898 على يد فريدريش ارنست درون [8] وسُمِّيَ انبعاث الراديوم، ولم يتم اعتباره غازاً نبيلاً حتى عام 1904 حين تم اكتشاف أن خصائصه شبيهة بخصائص الغازات النبيلة الأخرى.[9] حصل اللورد ريليه على جائزة نوبل في الفيزياء وويليام رامزي على نوبل في الكيمياء عام 1904 لاكتشافهما الغازات النبيلة[10][11] وقد وصف جي. إي. سيدربلوم الذي ترأس فيما بعد الأكاديمية السويدية الملكية للعلوم، وصفه بقوله:«اكتشاف مجموعة جديدة تماماً من العناصر، التي لم تُعرف أي مقدمات لها على وجه اليقين، لهوشيء فريد من نوعه تماماً في تاريخ الكيمياء، كونه في جوهَرِه تقدُّم في علم ذودلالةٍ غريبة».[11]
ساعد اكتشاف الغازات النبيلة على تطوير الفهم العام للبنية الذرية. حاول الكيميائي الفرنسي هنري مواسان عام 1895، تشكيل تفاعل كيميائي بين الأرغون، وهوأحد الغازات النبيلة والفلور، وهوأكثر العناصر كهرسلبية، إلا أن محاولته فشلت. بقي العلماء غير قادرين على تحضير مركبات كيميائية من الأرغون حتى نهاية القرن العشرين، إلا أن هذه المحاولات ساعدت العلماء على تطوير نظريات جديدة في البنية الذرية. استفاد الفيزيائي الدنماركي نيلز بور من هذه التجارب في افتراضه لتوضع الإلكترونات الذي طرحه عام 1913، حيث اقترح بور أن الإلكترونات في الذرات تصطف في طبقات أوأغلفة محيطة بالنواة، وأن جميع الغازت النبيلة باستثناء الهيليوم تحتوي في طبقتها الخارجية أوغلافها الخارجي على ثمانية إلكترونات.[9] وضع جيلبرت نيوتن لويس عام 1916 قاعدة الثمانيات، والتي تقول أن الذرات التي تحوي في طبقتها الخارجي على ثمانية إلكترونات أكثر استقراراً من أي ذرة أخرى للعنصر ذاته، حيث أن وجود ثمانية إلكترونات في الطبقة الخارجية لذرة العنصر يجعلها غير متفاعلة مع عنصر آخر لأنها لا تحتاج المزيد من الإلكترونات لتكمل طبقتها الخارجية.[12]
اكتشف نيل بارتلت عام 1962 أول مركب كيميائي من غاز نبيل وهوسداسي فلوروبلاتينات الزينون.[13] أما مركبات الغازات النبيلة الأخرى اِكتشفت بعد فترة وجيزة، حيث اكتشف أول مركب للرادون عام 1962 وهوثنائي فلوريد الرادون (RnF2) [14] والذي تم التعرف عليه بواسطة تقنيات الاقتفاء الراديوي، وفي عام 1963 اِكتُشِفَ أول مركب لغاز الكريبتون وهوثنائي فلوريد الكريبتون (KrF2) [15] تم الإبلاغ عن أول مركب مستقر للأرغون عام 2000 عندما تم تشكيل فلوروهيدريد الأرغون (HArF) عند درجة الحرارة 40 ك (−233.2 °م؛ −387.7 °ف).[16]
قام العلماء في ديسمبر/كانون الأول عام 1998 في المعهد المشترك للبحوث النووية في دوبنا في روسيا بقصف البلوتونيوم بالكالسيوم لإنتاج ذرة واحدة من العنصر 114[17] الفليروفيوم.[18] وقد بيّنت التجارب الكيميائية الأولية أن هذا العنصر قد يكون أول عنصر فوق ثقيل لإظهاره خصائص شاذة عن تلك خصائص الغاز النبيل، على الرغم من أنه عنصر من المجموعة 14 في الجدول الدوري.[19] ونجح العلماء من المعهد المشترك للبحوث النووية ومختبر لورانس ليفرمور الوطني في أكتوبر/تشرين الأول من العام 2006 بخلق الأوغانيسون الصناعي وهوالعنصر السابع في المجموعة 18[20] وذلك عبر قصف الكاليفورنيوم والكالسيوم.[21]
الخصائص الفيزيائية والذرية
[عدل]| الخاصية[9][22] | هيليوم | نيون | أرغون | كريبتون | زينون | رادون |
|---|---|---|---|---|---|---|
| الكثافة (جرام/دم3) | 0.1786 | 0.9002 | 1.7818 | 3.708 | 5.851 | 9.97 |
| درجة الغليان (كلفن) | 4.4 | 27.3 | 87.4 | 121.5 | 166.6 | 211.5 |
| درجة الذوبان (كلفن) | 0.95 (عند 25 وحدة بار) |
24.7 | 83.6 | 115.8 | 161.7 | 202.2 |
| حرارة التبخر (كيلوجول/مول) | 0.08 | 1.74 | 6.52 | 9.05 | 12.65 | 18.1 |
| الذوبانية في الماء عند 20 سيليزيوس (سم3/كغ) | 8.61 | 10.5 | 33.6 | 59.4 | 108.1 | 230 |
| العدد الذري | 2 | 10 | 18 | 36 | 54 | 86 |
| نصف القطر الذري محسوباً بالبيكومتر | 31 | 38 | 71 | 88 | 108 | 120 |
| طاقة التأين (كيلوجول/مول) | 2372 | 2080 | 1520 | 1351 | 1170 | 1037 |

تمتلك الغازات النبيلة قوى بين جزيئية ضعيفة، لذا فدرجات الانصهار والغليان منخفضة. جميع الغازات النبيلة أحادية الذرات في الظروف القياسية، بما في ذلك العناصر التي كتلتها الذرية أكبر من عناصر صلبة عديدة.[9] للهيليوم صفات مميزة عديدة مقارنةً مع العناصر الأخرى: درجات انصهاره وغليانه أقل من درجات انصهار وغليان أي مادة أخرى معروفة، حيث أن الهيليوم هوالعنصر الوحيد المعروف الذي يظهر ميوعة فائقة (أي تنعدم اللزوجة داخل السائل بشكل كامل)، وكلذلك فإن الهيليوم هوالعنصر الوحيد الذي لا يمكن أن يتصلّب بالتبريد ضمن الظروف القياسية-ضغط جوي يساوي 25 وحدة ضغط جوي (2500 كيلوباسكال، 370 رطل لكل بوصة مربعة) عند درجة حرارة 0.95 كلفن (-272.200 سيليزيوس، -457.960 فهرنهايت) لتحويله إلى الحالة الصلبة.[23] الغازات النبيلة حتى الزينون لها نظائر مستقرة عديدة. الرادون ليس له نظائر مستقرة، حيث أن نظيره طويل الأمد هوالرادون 222 له عمر نصف قُدِّر بـ 3.8 أيام ويتحلل إلى الهيليوم والبولونيوم، ويتحلل في نهاية المطاف إلى رصاص.[9] درجات الانصهار والغليان في الغازات النبيلة تزداد نزولاً في المجموعة.
يزداد نصف القطر الذري لذرات الغاز النبيل بالانتقال من فترة إلى أُخرى بزيادة عدد الإلكترونات كما في بقية مجموعات الجدول الدوري، ويرتبط حجم الذرة بعدة خصائص أخرى، مثلاً تنقص طاقة التأين بازدياد نصف القطر الذري لأن إلكترونات التكافؤ في الغازات النبيلة تكون أبعد عن النواة وبالتالي فالنواة بازدياد القطر الذري تصبح أقل قدرةً على الإمساك بهذه الإلكترونات والحفاظ عليها. للغازات النبيلة أكبر طاقة تأين ضمن عناصر دورها (سطرها)، وهذا يعكس استقرار التركيب الإلكتروني ويرتبط هذا الأمر بنقص فعاليتها الكيميائية.[22] للغازات النبيلة الثقيلة طاقات تأين صغيرة كتلك التي تمتلكها عناصر وجزيئات أخرى، حيث قادت فكرة أن الزينون له طاقة تأين مماثلة لطاقة تأين الأوكسجين قادت بارتلت لمحاولة أكسدة الزينون باستخدام سداسي فلوريد البلاتينوم وهومؤكسد معروف بكونه قوياً كفايةً للتفاعل مع الأوكسجين.[13] لا تتقبل الغازات النبيلة أي إلكترون، أنها لا تأخذ شكل أيون سالب الشحنة (أنيون أوصاعدة)، حيث أن الغازات النبيلة لها ألفة إلكترونية سالبة.[24]
يظهر ضعف قوى فان دير فالس بين الذرات على الخصائص الفيزيائية العيانية للغازات النبيلة بشكل واضح. تزداد القوة الجاذبة بازدياد حجم الذرة نظراً لازدياد قابلية الاستقطاب وانخفاض طاقة التأين، وهذا يؤدي إلى اتجاهات جماعية منتظمة تشمل: نزولاً في المجموعة 18 يزداد نصف القطر الذري وتزداد كذلك القوى بين الجزيئية مما يؤدي لزيادة درجات الانصهار والغليان وحرارة التبخر وتزداد كذلك الانحلالية. ويعود ازدياد الكثافة إلى ازدياد الكتلة الذرية.[22]
تكون الغازات النبيلة غازات مثالية في الظروف القياسية، إلا أن انحرافاتها عن قانون الغاز المثالي تقدم أدلة هامة لدراسة التفاعلات بين الجزيئات. تم استنتاج جهد لينارد-جونز عام 1924، باستخدام البياتات التجريبية للأرغون قبل تطور ميكانيك الكم التي وفَّرت أدوات لفهم القوى بين الجزيئية بمبادئها الأساسية. يستخدم جهد لينارد-جونز عادةً للإشارة إلى نموذج التفاعلات بين الجزيئات.[25] التحليل النظري للتفاعلات بين الجزيئية في الغازات النبيلة مقبول وقابل للتداول لأن الغازات النبيلة أحادية الذرات وذراتها كروية، وهذا يجعلها موحدة الخواص، أي أن التفاعل بين الجزيئات مستقل عن الاتجاه.
الخصائص الكيميائية
[عدل]
الغازات النبيلة عديمة اللون وعديمة الرائحة ولا طعم لها، وغير قابلة للاشتعال في الظروف القياسية. وُصفَت الغازات النبيلة ذات مرة بأنها المجموعة رقم 0 في الجدول الدوري، حيث اِعتُقد بأن تكافؤها صفر، أي أن ذراتها لا تتحد مع ذرات عناصر أخرى لتشكل مركبات. على أي حال، فقد أُهمِلت هذه التسمية لاحقاً بسبب اكتشاف بعض المركبات التي تدخل الغازات النبيلة في تركيبها.[9]
التوزيع
[عدل]كما هوالحال في المجموعات الأخرى، تظهر الغازات النبيلة أنماط من التوزيع الإلكتروني، ولا سيما ذلك الذي في الطبقة الخارجية والذي يتظاهر بسلوك كيميائي
| العدد الذري | العنصر الكيميائي | عدد الإلكترونات في الطبقات |
|---|---|---|
| 2 | هيليوم | 2 |
| 10 | نيون | 2, 8 |
| 18 | أرغون | 2, 8, 8 |
| 36 | كريبتون | 2, 8, 18, 8 |
| 54 | زينون | 2, 8, 18, 18, 8 |
| 86 | رادون | 2, 8, 18, 32, 18, 8 |
تمتلك الغازات النبيلة طبقة إلكترونية ممتلئة بإلكترونات التكافؤ، حيث تمثل إلكترونات التكافؤ إلكترونات الطبقة الخارجية في أي ذرة، وهي الإلكرتونات التي تشارك في الحالة الطبيعية بإنشاء الروابط الكيميائية. تكون الذرات ذات الطبقة الإلكترونية التكافؤية الكاملة أكثر استقراراً، لذا فهي لا تميل إلى تشكيل أي روابط كيميائية، لذا فإن ميلها لكسب أوخسارة إلكترونات يكون ضئيلاً.[26] على الرغم من ذلك، فإن الغازات النبيلة الثقيلة كالرادون مثلاً تتجمع على بعضها بالقوة الكهرطيسية بشكل أقل صلابةً من الغازات النبيلة الخفيفة وذلك يسهّل إزالة الإلكترونات الخارجية من الغازات النبيلة الثقيلة. يمكن استخدام الغازات النبيلة، نظراً لاكتمال طبقتها الخارجية في تدوين التوزيع الإلكتروني للعناصر المختلفة. للقيام بذلك تتم كتابة رمز أقرب غاز نبيل يسبق العنصر المعني، ومن ثم يتم إكمال كتابة التوزيع الإلكتروني لهذا العنصر، على سبيل المثال توزيع الفوسفور هو1s2 2s2 2p6 3s2 3p3، في حين أن تدوين توزيعه الإلكتروني باستخدام الغاز النبيل هو[Ne] 3s2 3p3 هذا النمط من التدوين أقصر من تدوين كامل التوزيع الإلكتروني للعنصر في كل مداراته الذرية.[27]
مركبات الغاز النبيل
[عدل]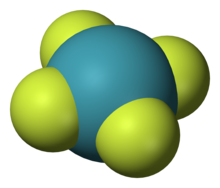
تفاعلية الغازات النبيلة منخفضة جداً، وبالتالي لم يتشكل سوى بضع مئات من مركبات الغازات النبيلة. لم تتشكل المركبات المحايدة التي يشارك الهيليوم والنيون في روابطها الكيميائية (على الرغم من وجود أدلة نظرية على وجود بعض المركبات للهيليوم)، بينما الزينون والكريبتون والأرغون أظهرت تفاعلية ضئيلة.[28] تتبع شدة التفاعلية الترتيب الآتي
Ne < He < Ar < Kr < Xe < Rn.
توقّع لينوس باولينغ عام 1933 أن الغازات النبيلة يمكن لها أن ُتُشَكِّل مركبات كيميائية مع الأوكسجين والفلور، وتوقّع وجود مركب سداسي فلوريد الكريبتون وسداسي فلوريد الزينون، وتوقّع كذلك وجود مركب ثماني فلوريد الزينون كمركب غير مستقر.[29][30] وقد تبين صحة هذه التنبؤات بشكل عام، إلا أن ثماني فلوريد الزينون يُعتقد أنه مركب غير ثابت حرارياً أوحركياً.[31] تُمثِّل مركبات الزينون الأكثر عدداً بين مركبات الغازات النبيلة التي تم تشكيلها حتى الآن.[32] معظمها لها ذرة زينون في حالة الأكسدة +2 أو+4 أو+6 أو+8 مرتبطةً إلى ذرات كهرسلبية مثل الفلور أوالأوكسجين، كما هوالحال في ثنائي فلوريد الزينون XeF2 ورباعي فلوريد الزينون XeF4 وسداسي فلوريد الزينون XeF6 ورباعي أوكسيد الزينونXeO4. يتفاعل الزينون مع الفلور لتشكيل العديد من المركبات تبعاً للمعادلات:
- Xe + F2 → XeF2
- Xe + 2F2 → XeF4
- Xe + 3F2 → XeF6
تستخدم بعض هذه المركبات في الصناعة الكيميائية كعوامل مؤكسدة، مثل ثنائي فلوريد الزينون المتوفر تجارياً، يحث يمكن استخدامه كعامل فلورة.[33] بحلول 2007 تم تحديد حوالي 500 مركب للزينون بما في ذلك مركبات الزينون العضوية (تحتوي المركبات التي يرتبط بها الزينون بذرة كربون)، والزينون المرتبط بالنتروجين والكلور والذهب والزئبق والزينون نفسه.[28][34] كما تم اكتشاف مركبات يرتبط فيها الزينون بالبورون أوالهيدروجين أوالبيريليوم أوالكبريت أوالتيتانيوم أوالنحاس أوالفضة ولكن ضمن دشروط خاصة.[28] من الناحية النظرية، الرادون أكثر تفاعلية من الزينون، فينبغي أن يكون قادراً على تشكيل الروابط الكيميائية بشكل أسهل من الزينون. إلاأنه عملياً بسبب النشاط الإشعاعي العالي وعمر النصف القصير لنظائر الرادون، فإنه من الممكن تركيب مركبات قليلة من أكاسيد وفلوريدات الرادون.[35] الكريبتون أقل تفاعليةً من الزينون، إلا أنه تم الإبلاغ عن عدة مركبات من الكريبتون في حالة الأكسدة +2.[28] يُعبر مركب ثنائي فلوريد الكريبتون الأكثر استقراراً وملاحظةً. يتفاعل الكريبتون مع الفلور تحت الظروف القاسية ليشكّل ثنائي فلوريد الكريبتون تبعاً للتفاعل:
- Kr + F2 → KrF2
تمت ملاحظة المركبات التي يشكل فيها الكريبتون رابطة واحدة مع النيتروجين والأوكسجين[36]، ولكنه ثابت ضمن الظروف - 60 سيليزيوس (-76 فهرنهايت) و-90 سيليزيوس (-130 فهرنهايت) على الترتيب.[28] ترتبط ذرات الكريبتون كيميائياً إلى غير المعادن (الهيدروجين، الكلور، الكربون)، كما يرتبط أيضاً ببعض المعادن الانتقالية المتأخرة كالنحاس والفضة والذهب ولكن لفي درجات حرارة منخفضة أوأوفي قذف فوق الصوتي.[28] تم تطبيق هذه الظروف من أجل الحصول على مركبات للأرغون عام 2000 مثل فلوروهدريد الأرغون (HArF)، وكان بعض مركبات الغازات النبيلة التي ترتبط بها الغازات النبيلة بالمعادن الانتقالية المتأخرة كالفضة أوالذهب أوالنحاس.[28] بحلول عام 2007، لم تُعرف بعد جزيئات محايدة مستقرة بما في ذلك المرتبطة بالنيون أوتساهمياً بالهيليوم.[28] تستطيع الغازات النبيلة-بما في ذلك الهيليوم-تشكيل جزيئات مستقرة بشكل أيونات في الطور الغازي. أبسطها أيون جزيئة هدريد الهيليوم HeH+ الذي اِكتُشِفَ عام 1925.[37] يُعتقد أن هذا التفاعل يحدث طبيعياً في الوسط بين النجمي، على الرغم من أنه لم يتم الجزم بذلك بعد، لأن هذين العنصرين الهيدروجين والهيليوم هما الأكثر وفرةً في الكون.[38] بالإضافة إلى هذه الأيونات، يوجد العديد من الإكسيمرات المحايدة للغازات النبيلة. هذه المركبات كفلوريد الأرغون أوفلوريد الكريبتون مستقرة فقط في الحالة الإلكترونية المُثارة، ولبعضهم تطبيق في ليزرات إكسيمير. إضافةً إلى المركبات التي تشارك فيها ذرة الغاز النبيل برابطة تساهمية، هناك مركبات تشارك فيها الغازات النبيلة برابطة غير تساهمية. وُصفت المركبات القفصية لأول مرة عام 1949،[39] وهي مؤلفة من ذرة غاز نبيل محاصرة ضمن أجواف المشابك البلورية لبعض المواد العضوية وغير العضوية. الشرط المهم لتشكيلها هي أن توافق أحجام ذرات الضيف (الغاز النبيل) تجاويف الشبكة البلورية المُضيفِة. على سبيل المثال، تشكل غازات الأرغون والكريبتون والزينون مركبات قفصية مع الهيدروكينون، لكن الهيليوم والنيون لا تشكل لأنها صغيرة جداً أوقابلية استقطابها غير كافية لترتبط.[40] تستطيع غازات النيون والأرغون والكريبتون والزينون تشكيل هيدرات حيث يتوضع الغاز النبيل ضمن الجليد.[41]
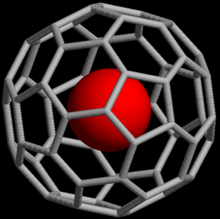
اكتشفت إمكانية تشكيل مركبات داخل فوليرينية من الغازت النبيلة، حيث تكون ذرة الغاز النبيل محاصرة داخل جزيء الفوليرين. عام 1993، اكتشف أنه عند تعريض مركبات C60، وهي مركبات ذات جزيئة كروية الشكل تتألف من 60 ذرة كربون، حين يتم تعريضها للغازات النبيلة في ضغط مرتفع، تتشكل معقدات مثل He@C60 (حيث تشير العلامة @ إلى أن ذرة الغاز النبيل توجد ضمن جزيئة C60 ولكن دون أن ترتبط بها تساهمياً).[42] بحلول عام 2008، تم الحصول على مركبات داخل فوليرينية لغازات الهيليوم والنيون والأرغون والكريبتون والزينون.[43] تم استخدام هذه المركبات في دراسة بنية وتفاعلية الفوليرينات بوسائل الرنين المغناطيسي النووي لذرات الغاز النبيل.[44]
مركبات الغازات النبيلة لثنائي فلوريد الزينون XeF2 شديدة الثبات، لأنها تزيد على قاعدة الثمانية. تم اقتراح نموذج لشرح الارتباط في هذه المركبات لأول مرة عام 1951، حيث اعتبر هذا النموذج ارتباط ثلاث ذرات بشل خطي. على سبيل المثال، تم وصف الارتباط في ثنائي فلوريد الزينون بمجموعة من ثلاثة مدارات جزيئية مشتقة من المدارات P من كل ذرة. الارتباط ناجم عن الجمع بين المدارات P الممتلئة من الزينون مع مدار نصف ممتلئ من المدار P من كل ذرة فلور، مما يؤدي إلى مدار ممتلئ غير رابط ومدار مضاد ترابط فارغ. المدار الجزيئي الأعلى المشغول يتحدد بالذرتين النهائيتين. هذا يقدم موقعاً للشحنة ويتم تسهيله بواسطة الكهرسلبية العالية للفلور.[45] ترسخت كيمياء الغازات النبيلة الثقيلة، بينما ما تزال كيمياء الغازات النبيلة الأخف كالكريبتون والزينون في مرحلة باكرة، بينما لم يتم تحديد عناصر لغاز النيون بعد.
التشكُّل والإنتاج
[عدل]تنخفض وفرة الغازات النبيلة في الكون مع زيادة أعدادها الذرية. الهيليوم وهوالعنصر الأكثر شيوعاً في الكون بعد الهيدروجين يمتلك كسر كتلي حوالي 24%. معظم الهيليوم في الكون تكوّن خلال التكوّن النووي في الانفجار العظيم (وإلى درجة صغيرة من خلال اضمحلال ألفا للعناصر الثقيلة).[46][47] الوفرة على الأرض تتبع اتجاهات مختلفة، على سبيل المثال الهيليوم هوثالث أكثر الغازات النبيلة وفرة في الغلاف الجوي، والسبب لعدم وجود هيليوم بدائي في الغلاف الجوي، ولصغر كتلة الذرة، لا يُمكن أن يُحتفظ بالهيليوم بواسطة مجال الجاذبية الأرضية.[48] الهيليوم على الأرض يأتي من اضمحلال ألفا للعناصر الثقيلة كاليورانيوم والثوريوم الموجودة في قشرة الأرض، ويميل للتراكم في رواسب الغاز الطبيعي.[48] ومن ناحية أخرى، تزداد وفرة الأرغون كنتيجة لاضمحلال بيتا للبوتاسيوم 40، ويمكن أن يُوجد أيضاً في قشرة الأرض بشكل الأرغون 40 وهوالشكل الأكثر وفرة للأرغون على الأرض على الرغم من كونه نادر نسبياً في النظام الشمسي. تعتبر هذه العملية الأساس لطريقة التأريخ البوتاسيوم-الأرغون.[49] على عكس المتوقع فإن الزينون منخفض الوفرة في الغلاف الجوي، وقد دُعيت هذه بمشكلة الزينون المفقود، حيث ظهرت نظرية تفسر فقده بأنه محتبس داخل المعادن في القشرة الأرضية.[50] بعد اكتشاف ثنائي أوكسيد الزينون، أظهرت أبحاث أن الزينون من الممكن أن يحل محل السيليكون في الكوارتز.[51] يتشكّل الرادون في الغلاف الصخري من الراديوم باضمحلال ألفا. يمكن للرادون أن يتسرب إلى المباني من خلال الشقوق في الأساسات، ويتراكم في المناطق ذات التهوية غير الجيدة. يشكل الرادون خطر كبيراً على الصحة بسبب نشاطه الإشعاعي العالي، يُشتبه بكون الرادون سبب في 21.000 وفاة سرطان رئة سنوياً في الولايات المتحدة فقط.[52]
| التوجد | الهيليوم | النيون | الأرغون | الكريبتون | الزينون | الرادون |
|---|---|---|---|---|---|---|
| النظام الشمسي (مقابل كل ذرة سيليكون)[53] | 2343 | 2.148 | 0.1025 | 5.515 × 10?5 | 5.391 × 10?6 | – |
| الغلاف الجوي للأرض (كسر حجمي جزء مقابل مليون)[54] | 5.20 | 18.20 | 9340.00 | 1.10 | 0.09 | (0.06–18) × 10?19[55] |
| الخور الباطنة (كسر كتلي جزء مقابل مليون)[22] | 3 × 10?3 | 7 × 10?5 | 4 × 10?2 | – | – | 1.7 × 10?10 |
| الغاز | سعر عام 2004 (دولار أميركي/متر مكعب)[56] |
|---|---|
| الهيليوم (صناعي) | 4.20–4.90 |
| الهيليوم (مخبري) | 22.30–44.90 |
| الأرغون | 2.70–8.50 |
| النيون | 60–120 |
| الكريبتون | 400–500 |
| الزينون | 4000–5000 |
للاستخدام واسع النطاق يتم استخراج الهيليوم عبر التقطير بالتجزئة من الغاز الطبيعي والذي يمكن أن يحتوي على هيليوم بنسبة 7%.[57] يتم الحصول على النيون والأرغون والكريبتون والزينون من الهواء باستخدام أساليب تسييل الغازات، حيث يتم تحويل الغازت إلى الحالة السائلة ومن ثم تقطير بالتجزئة لفصل الخلائط إلى مكوناتها. يتم إنتاج الهيليوم عاجدةً عبر فصله عن الغاز الطبيعي، والرادون يُعزل عبر النشاط الإشعاعي لمركباته.[9] تتأثر أسعار الغازات الطبيعية بوفرتها، حيث الأرغون أرخصها، والزينون هوالأعلى سعراً. يمثل الجدول المجاور أسعار الكميّات المخبرية للغازات في الولايات المتحدة لعام 2004.
التطبيقات
[عدل]
للغازات النبيلة درجات انصهار وغليان منخفضة جداً، مما يجعلها مفيدة كمبردات مُجمِّدة.[58] على وجه التحديد، الهيليوم السائل الذي يغلي عند الدرجة 4.2 كلفن (-268.95 مئوية، أي -452.11 فهرنهايت)، لذا يُستخدم للمغناطيسات فائقة التوصبل، مثل تلك اللازمة في التصوير بالرنين المغناطيسي والرنين المغناطيسي النووي.[59] يُستخدم أيضاً النيون السائل في التجميد على الرغم من أنه لا يصل إلى درجات الحرارة المنخفضة كالهيليوم السائل، إلا أنه يمتلك سعة تبريد أكبر بأربعين مرة من الهيليوم السائل وأكثر بثلاثة أضعاف من الهيدروجين السائل.[55]
يُستخدم الهيليوم كأحد عناصر غازات التنفس ليحل محل النيتروجين، نظراً لانخفاض قابليته للذوبان في السوائل والدهون.يتم امتصاص الغازات من قبل الدم وأنسجة الجسم في حالات الضغط المنخفض كالغوص، مما يؤدي إلى تأثير مخدر يعرف باسم تخدير النيتروجين أوتخدير الأعماق.[60] بسبب انخفاض ذوبانية الهيليوم فإن الخلايا تأخذ كمية قليلة منه، وعندما يتم استخدام الهيليوم ليحل محل جزء من خليط التنفس، كما هوالحال في التريمكس والهيليوكس، ينخفض التأثير المخدر للغاز عند بلوغ الأعماق.[61] انحلالية الهيليوم المنخفضة توفر مزايا لحالة تدعى مرض انخفاض الضغط أوالتحنّي.[9][62] انخفاض كمية الغاز المُذاب في الجسم تعني تشكل فقاعات أقل خلال انخفاض الضغط خلال الصعود. يعتبر الأرغون الخيار الأفضل لاستخدامه كغاز تضخيم لبدلة الغوص.[63] يُستخدم الهيليوم كذلك لملء الغز في قضبان الوقود النووي للمفاعلات النووية.[64]

حل الهيليوم محل الهيدروجين كغاز رفع في المنحدرات والبالونات، بعد حادثة تحطم هيندنبورغ عام 1937[65]، بسبب خفته على الرغم من حدوث انخفاض في الطفوبنسبة 8.6%.[66] decrease in buoyancy.[9] تُستخدم الغازات النبيلة لتوفير جوخامل في عدة تطبيقات. يستخدم الأرغون في تركيب المركبات حساسة الهواء التي تتحسس لغاز النيتروجين. يُستخدم الأرغون الصلب كذلك لدراسة المركبات غير المستقرة جداً، كوسائط التفاعل، عبر وضعهم في جوخامل في درجات حرارة منخفضة جداً.[67] يُستخدم الهيليوم كوسيط حامل في صبغ الغازات، وكغاز حشولمقاييس الحرارة، وفي أجهزة قياس الإشعاع كعداد غايغر وغرفة الفقاقيع،[56] يُستخدم الهيليوم والأرغون على حدٍ سواء لحماية (لتغليف) أقواس اللحام والمعادن المحيطة (الفلزات الوضيعة) من الغلاف الجوي أثناء اللحام والقطع، وكذلك في العمليات المعدنية الأخرى، وفي إنتاج السيليكون لصناعة أشباه النواقل.[55]

تُستخدم الغازات النبيلة عادةً في الإضاءة بسبب تفاعليتها المنخفضة جداً. يُستخدم الأرغون المختلط مع النيتروجين كغاز حشوللمصابيح المتوهجة.[55] يُستخدم الكريبتون في المصابيح الكهربائية عالية الأداء، ذات درجات الحرارة الأعلى والكفاءة الأكبر، وذلك لأنه يقلل معدل تبخر الخيوط أكثر من الأرغون، وفي مصابيح الهالوجين على وجه الخصوص يُستخدم الكريبتون مختلطاً مع كميات صغيرة من مركبات اليود أوالبروم.[55] تتوهج الغازات النبيلة بألوان مميزة عند استخدامها داخل مصابيح تفريغ الغاز، كأضواء النيون. يستخدم الزينون عادةً في مصابيح قوس الزينون، ولهذه المصابيح تطبيق في أجهزة العرض السينمائي ومصابيح السيارات، نظراً للطيف المستمر تقريباً وهوما يجعلها تشبه ضوء النهار.[55] تُستخدم الغازات النبيلة في ليزرات إكسيمر، والتي تقوم على جزيئات قصيرة الأجل مُثارة إلكترونياً تُعرف بالإكسيمرات. قد تكون الإكسيمرات المستخدمة في الليزرات جزيئات ثنائية الذرة لغازات نبيلة مثل Ar2 أوCr2 أوXe2، أوقد يُجمع الغاز النبيل مع هالوجين في الإكسيمر (وهوالأكثر شيوعاً) مثل كلوريد الزينون XeCl أوفلوريد الزينون XeF أوفلوريد الأرغون ArF. تنتج هذه الليزرات ضوء فوق بنفسجي، يسمح هذا الضوء بالتصوير عالي الدقة نظراً لقصر طول موجته (طول موجة فلوريد الأرغون 193 نانومتر، بينما فلوريد الكريبتون 248 نانومتر). لليزرات الإكسيمر تطبيقات صناعية وطبية وعلمية، حيث تستخدم في جراحة الليزر بما في ذلك رأب الأوعية بالليزر وجراحة العين.[68] لبعض الغات النبيلة تطبيقات مباشرة في الطب، حيث يُستخدم الهيليوم أحياناً لتحسين التنفس لدى مرضى الربو.[55] يُستخدم كذلك الزينون كمُخدِّر بسبب ذوبانيته الشديدة في الدهون، وهذا ما يجعله أكثر فعالية من أوكسيد النيتروز المعتاد، ولأن الجسم يتخلص منه بسهولة، مما يؤدي لانتعاش أسرع.[69] للزينون تطبيق طبي آخر في التصوير الطبي للرئتين من خلال التصوير بالرنين المغناطيسي فائق القطبية.[70] يُستخدم الرادون صاحب النشاط الإشعاعي الكبير في المعالجة بالأشعة.[9]
ألوان التفريغ
[عدل]
|

|

|

|

|

|

|

|

|

|

|

|

|

|

|
| هيليوم | نيون | أرغون | كريبتون | زينون |
يعتمد لون انبعاث تصريف الغاز على عدّة عوامل، منها ما يلي:[71]
- معلمات التفريغ (القيمة المحلية لكثافة التيار والحقل الكهربائي، ودرجة الحرارة...إلخ.-لاحظ تنوع اللون على طول التفريغ في الصف الأعلى.
- نقاء الغاز (يمكن لنسب صغيرة من الغازات الأخرى أن تحدث تأثيراً في اللون)
- المادة التي تغلف أنبوب التفريغ.
المصادر
[عدل]- ^ Renouf، Edward (1901). "Noble gases". ساينس. ج. 13 ع. 320: 268–270. Bibcode:1901Sci....13..268R. DOI:10.1126/science.13.320.268.
- ^ Ozima 2002، صفحة 30
- ^ Ozima 2002، صفحة 4
- ^ "argon". Encyclop?dia Britannica. 2008. مؤرشف من الأصل في 2008-11-18.
- ^ ا ب Ozima 2002، صفحة 1
- ^ Oxford English Dictionary (1989), s.v. "helium". Retrieved December 16, 2006, from Oxford English Dictionary Online. Also, from quotation there: Thomson, W. (1872). Rep. Brit. Assoc. xcix: "Frankland and Lockyer find the yellow prominences to give a very decided bright line not far from D, but hitherto not identified with any terrestrial flame. It seems to indicate a new substance, which they propose to call Helium."
- ^ Mendeleev 1903، صفحة 497
- ^ Partington، J. R. (1957). "Discovery of Radon". نيتشر (مجلة). ج. 179 ع. 4566: 912. Bibcode:1957Natur.179..912P. DOI:10.1038/179912a0.
- ^ ا ب ج د ه و ز ح ط ي "Noble Gas". Encyclop?dia Britannica. 2008. مؤرشف من الأصل في 2008-05-15.
- ^ Cederblom, J. E. (1904). "The Nobel Prize in Physics 1904 Presentation Speech". مؤرشف من الأصل في 2017-07-30.
- ^ ا ب Cederblom, J. E. (1904). "The Nobel Prize in Chemistry 1904 Presentation Speech". مؤرشف من الأصل في 2017-07-31.
- ^ Gillespie, R. J.؛ Robinson, E. A. (2007). "Gilbert N. Lewis and the chemical bond: the electron pair and the octet rule from 1916 to the present day". J Comput Chem. ج. 28 ع. 1: 87–97. DOI:10.1002/jcc.20545. PMID:17109437.
- ^ ا ب Bartlett، N. (1962). "Xenon hexafluoroplatinate Xe+[PtF6]?". Proceedings of the Chemical Society ع. 6: 218. DOI:10.1039/PS9620000197.
- ^ Fields, Paul R.؛ Stein, Lawrence؛ Zirin, Moshe H. (1962). "Radon Fluoride". دورية الجمعية الكيميائية الأمريكية. ج. 84 ع. 21: 4164–4165. DOI:10.1021/ja00880a048.
- ^ Grosse, A. V.؛ Kirschenbaum, A. D.؛ Streng, A. G.؛ Streng, L. V. (1963). "Krypton Tetrafluoride: Preparation and Some Properties". Science. ج. 139 ع. 3559: 1047–1048. Bibcode:1963Sci...139.1047G. DOI:10.1126/science.139.3559.1047. PMID:17812982.
- ^ Khriachtchev, Leonid؛ Pettersson, Mika؛ Runeberg, Nino؛ Lundell, Jan؛ R?s?nen, Markku (2000). "A stable argon compound". نيتشر (مجلة). ج. 406 ع. 6798: 874–876. DOI:10.1038/35022551. PMID:10972285.
- ^ Oganessian, Yu. Ts.؛ Utyonkov، V.؛ Lobanov، Yu.؛ Abdullin، F.؛ Polyakov، A.؛ وآخرون (1999). "Synthesis of Superheavy Nuclei in the 48Ca + 244Pu Reaction". Physical Review Letters. الجمعية الفيزيائية الأمريكية. ج. 83 ع. 16: 3154–3157. Bibcode:1999PhRvL..83.3154O. DOI:10.1103/PhysRevLett.83.3154.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|الأول5=(مساعدة) وExplicit use of et al. in:|مؤلف6=(مساعدة) - ^ Woods، Michael (6 مايو 2003). "Chemical element No. 110 finally gets a name—darmstadtium". Pittsburgh Post-Gazette. مؤرشف من الأصل في 2012-01-24. اطلع عليه بتاريخ 2008-06-26.
- ^ "Gas Phase Chemistry of Superheavy Elements" (PDF). Texas A&M University. مؤرشف من الأصل (PDF) في 2012-02-20. اطلع عليه بتاريخ 2008-05-31.
- ^ Barber, Robert C.؛ Karol, Paul J.؛ Nakahara, Hiromichi؛ Vardaci, Emanuele؛ Vogt, Erich W. (2011). "Discovery of the elements with atomic numbers greater than or equal to 113 (IUPAC Technical Report)*" (PDF). Pure Appl. Chem. IUPAC. ج. 83 ع. 7. DOI:10.1515/ci.2011.33.5.25b. مؤرشف من الأصل (PDF) في 2017-07-31. اطلع عليه بتاريخ 2014-05-30.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|last-author-amp=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Oganessian، Yu. Ts.؛ Utyonkov، V.؛ Lobanov، Yu.؛ Abdullin، F.؛ Polyakov، A.,؛ وآخرون (2006). "Synthesis of the isotopes of elements 118 and 116 in the قالب:SimpleNuclide and قالب:SimpleNuclide + قالب:SimpleNuclide fusion reactions". Physical Review C. ج. 74 ع. 4: 44602. Bibcode:2006PhRvC..74d4602O. DOI:10.1103/PhysRevC.74.044602.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف6=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) صيانة الاستشهاد: علامات ترقيم زائدة (link) - ^ ا ب ج د Greenwood 1997، صفحة 891
- ^ "Solid Helium". University of Alberta. مؤرشف من الأصل في 2008-02-12. اطلع عليه بتاريخ 2008-06-22.
- ^ Wheeler, John C. (1997). "Electron Affinities of the Alkaline Earth Metals and the Sign Convention for Electron Affinity". Journal of Chemical Education. ج. 74: 123–127. Bibcode:1997JChEd..74..123W. DOI:10.1021/ed074p123. مؤرشف من الأصل في 2020-12-02.; Kalcher, Josef؛ Sax, Alexander F. (1994). "Gas Phase Stabilities of Small Anions: Theory and Experiment in Cooperation". Chemical Reviews. ج. 94 ع. 8: 2291–2318. DOI:10.1021/cr00032a004.
{{استشهاد بدورية محكمة}}: الوسيط|مسار أرشيف=بحاجة لـ|مسار=(مساعدة) - ^ Mott، N. F. (1955). "John Edward Lennard-Jones. 1894–1954". Biographical Memoirs of Fellows of the Royal Society. ج. 1: 175–184. DOI:10.1098/rsbm.1955.0013.
- ^ Ozima 2002، صفحة 35
- ^ CliffsNotes 2007، صفحة 15
- ^ ا ب ج د ه و ز ح Grochala، Wojciech (2007). "Atypical compounds of gases, which have been called noble". Chemical Society Reviews. ج. 36 ع. 10: 1632–1655. DOI:10.1039/b702109g. PMID:17721587.
- ^ Pauling، Linus (1933). "The Formulas of Antimonic Acid and the Antimonates". Journal of the American Chemical Society. ج. 55 ع. 5: 1895–1900. DOI:10.1021/ja01332a016.
- ^ Holloway 1968
- ^ Seppelt، Konrad (1979). "Recent developments in the Chemistry of Some Electronegative Elements". Accounts of Chemical Research. ج. 12 ع. 6: 211–216. DOI:10.1021/ar50138a004.
- ^ Moody، G. J. (1974). "A Decade of Xenon Chemistry". Journal of Chemical Education. ج. 51 ع. 10: 628–630. Bibcode:1974JChEd..51..628M. DOI:10.1021/ed051p628. مؤرشف من الأصل في 2010-06-15. اطلع عليه بتاريخ 2007-10-16.
- ^ Zupan, Marko؛ Iskra, Jernej؛ Stavber, Stojan (1998). "Fluorination with XeF2. 44. Effect of Geometry and Heteroatom on the Regioselectivity of Fluorine Introduction into an Aromatic Ring". J. Org. Chem. ج. 63 ع. 3: 878–880. DOI:10.1021/jo971496e. PMID:11672087.
- ^ Harding 2002، صفحات 90–99
- ^ .Avrorin, V. V.؛ Krasikova, R. N.؛ Nefedov, V. D.؛ Toropova, M. A. (1982). "The Chemistry of Radon". Russian Chemical Review. ج. 51 ع. 1: 12–20. Bibcode:1982RuCRv..51...12A. DOI:10.1070/RC1982v051n01ABEH002787.
- ^ Lehmann, J (2002). "The chemistry of krypton". Coordination Chemistry Reviews. 233–234: 1–39. DOI:10.1016/S0010-8545(02)00202-3.
- ^ Hogness, T. R.؛ Lunn, E. G. (1925). "The Ionization of Hydrogen by Electron Impact as Interpreted by Positive Ray Analysis". Physical Review. ج. 26: 44–55. Bibcode:1925PhRv...26...44H. DOI:10.1103/PhysRev.26.44.
- ^ Fernandez, J.؛ Martin, F. (2007). "Photoionization of the HeH2+ molecular ion". J. Phys. B: At. Mol. Opt. Phys. ج. 40 ع. 12: 2471–2480. Bibcode:2007JPhB...40.2471F. DOI:10.1088/0953-4075/40/12/020.
- ^ Powell, H. M.؛ Guter, M. (1949). "An Inert Gas Compound". Nature. ج. 164 ع. 4162: 240–241. Bibcode:1949Natur.164..240P. DOI:10.1038/164240b0.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|lastauthoramp=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Greenwood 1997، صفحة 893
- ^ Dyadin, Yuri A.؛ وآخرون (1999). "Clathrate hydrates of hydrogen and neon". Mendeleev Communications. ج. 9 ع. 5: 209–210. DOI:10.1070/MC1999v009n05ABEH001104.
- ^ Saunders, M.؛ Jiménez-V?zquez, H. A.؛ Cross, R. J.؛ Poreda, R. J. (1993). "Stable compounds of helium and neon. He@C60 and Ne@C60". ساينس. ج. 259 ع. 5100: 1428–1430. Bibcode:1993Sci...259.1428S. DOI:10.1126/science.259.5100.1428. PMID:17801275.
- ^ Saunders, Martin؛ Jimenez-Vazquez, Hugo A.؛ Cross, R. James؛ Mroczkowski, Stanley؛ Gross, Michael L.؛ Giblin, Daryl E.؛ Poreda, Robert J. (1994). "Incorporation of helium, neon, argon, krypton, and xenon into fullerenes using high pressure". J. Am. Chem. Soc. ج. 116 ع. 5: 2193–2194. DOI:10.1021/ja00084a089.
- ^ Frunzi، Michael؛ Cross، R. Jame؛ Saunders، Martin (2007). "Effect of Xenon on Fullerene Reactions". Journal of the American Chemical Society. ج. 129 ع. 43: 13343–6. DOI:10.1021/ja075568n. PMID:17924634.
- ^ Pimentel، G. C. (1951). "The Bonding of Trihalide and Bifluoride Ions by the Molecular Orbital Method". The Journal of Chemical Physics. ج. 19 ع. 4: 446–448. Bibcode:1951JChPh..19..446P. DOI:10.1063/1.1748245.
- ^ Weiss، Achim. "Elements of the past: Big Bang Nucleosynthesis and observation". Max Planck Institute for Gravitational Physics. مؤرشف من الأصل في 2010-05-28. اطلع عليه بتاريخ 2008-06-23.
- ^ Coc, A.؛ وآخرون (2004). "Updated Big Bang Nucleosynthesis confronted to WMAP observations and to the Abundance of Light Elements". المجلة الفيزيائية الفلكية. ج. 600 ع. 2: 544–552. arXiv:astro-ph/0309480. Bibcode:2004ApJ...600..544C. DOI:10.1086/380121.
- ^ ا ب Morrison، P.؛ Pine، J. (1955). "Radiogenic Origin of the Helium Isotopes in Rock". Annals of the New York Academy of Sciences. ج. 62 ع. 3: 71–92. Bibcode:1955NYASA..62...71M. DOI:10.1111/j.1749-6632.1955.tb35366.x.
- ^ Scherer، Alexandra (16 يناير 2007). "40Ar/39Ar dating and errors". Technische Universit?t Bergakademie Freiberg. مؤرشف من الأصل في 2007-10-14. اطلع عليه بتاريخ 2008-06-26.
- ^ Sanloup، Chrystèle؛ Schmidt، Burkhard C.؛ وآخرون (2005). "Retention of Xenon in Quartz and Earth's Missing Xenon". Science. ج. 310 ع. 5751: 1174–1177. Bibcode:2005Sci...310.1174S. DOI:10.1126/science.1119070. PMID:16293758.
- ^ Tyler Irving (مايو 2011). "Xenon Dioxide May Solve One of Earth's Mysteries". L’Actualité chimique canadienne (Canadian Chemical News). مؤرشف من الأصل في 2013-02-09. اطلع عليه بتاريخ 2012-05-18.
- ^ "A Citizen's Guide to Radon". U.S. Environmental Protection Agency. 26 نوفمبر 2007. مؤرشف من الأصل في 2015-09-24. اطلع عليه بتاريخ 2008-06-26.
- ^ Lodders، Katharina (10 يوليو 2003). "Solar System Abundances and Condensation Temperatures of the Elements" (PDF). The Astrophysical Journal. The American Astronomical Society. ج. 591 ع. 2: 1220–1247. Bibcode:2003ApJ...591.1220L. DOI:10.1086/375492. مؤرشف من الأصل (PDF) في 2016-09-10.
{{استشهاد بدورية محكمة}}: الوسيط|ref=harvغير صالح (مساعدة) - ^ "The Atmosphere". National Weather Service. مؤرشف من الأصل في 2018-08-13. اطلع عليه بتاريخ 2008-06-01.
- ^ ا ب ج د ه و ز H?ussinger, Peter؛ Glatthaar, Reinhard؛ Rhode, Wilhelm؛ Kick, Helmut؛ Benkmann, Christian؛ Weber, Josef؛ Wunschel, Hans-J?rg؛ Stenke, Viktor؛ Leicht, Edith؛ Stenger, Hermann (2002). "Noble gases". Ullmann's Encyclopedia of Industrial Chemistry. Wiley. DOI:10.1002/14356007.a17_485.
- ^ ا ب Hwang, Shuen-Chen؛ Lein, Robert D.؛ Morgan, Daniel A. (2005). "Noble Gases". Kirk Othmer Encyclopedia of Chemical Technology. Wiley. ص. 343–383. DOI:10.1002/0471238961.0701190508230114.a01.
- ^ Winter, Mark (2008). "Helium: the essentials". University of Sheffield. مؤرشف من الأصل في 2019-04-04. اطلع عليه بتاريخ 2008-07-14.
- ^ "Neon". إنكارتا. 2008.
- ^ Zhang, C. J.؛ Zhou, X. T.؛ Yang, L. (1992). "Demountable coaxial gas-cooled current leads for MRI superconducting magnets". Magnetics, IEEE Transactions on. معهد مهندسي الكهرباء والإلكترونيات. ج. 28 ع. 1: 957–959. Bibcode:1992ITM....28..957Z. DOI:10.1109/20.120038.
- ^ Fowler، B.؛ Ackles، K. N.؛ Porlier، G. (1985). "Effects of inert gas narcosis on behavior—a critical review". Undersea Biomed. Res. ج. 12 ع. 4: 369–402. ISSN:0093-5387. OCLC:2068005. PMID:4082343. مؤرشف من الأصل في 2011-07-27. اطلع عليه بتاريخ 2008-04-08.
- ^ Bennett 1998، صفحة 176
- ^ Vann، R. D. (ed) (1989). "The Physiological Basis of Decompression". 38th Undersea and Hyperbaric Medical Society Workshop. 75(Phys)6-1-89: 437. مؤرشف من الأصل في 2010-01-05. اطلع عليه بتاريخ 2008-05-31.
{{استشهاد بدورية محكمة}}:|الأول=باسم عام (مساعدة) - ^ Maiken، Eric (1 أغسطس 2004). "Why Argon?". Decompression. مؤرشف من الأصل في 2018-08-27. اطلع عليه بتاريخ 2008-06-26.
- ^ Horhoianu، G.؛ Ionescu، D. V.؛ Olteanu، G. (1999). "Thermal behaviour of CANDU type fuel rods during steady state and transient operating conditions". Annals of Nuclear Energy. ج. 26 ع. 16: 1437–1445. DOI:10.1016/S0306-4549(99)00022-5.
- ^ "Disaster Ascribed to Gas by Experts". نيويورك تايمز. 7 مايو 1937. ص. 1.
- ^ Freudenrich، Craig (2008). "How Blimps Work". HowStuffWorks. مؤرشف من الأصل في 2010-04-29. اطلع عليه بتاريخ 2008-07-03.
- ^ Dunkin, I. R. (1980). "The matrix isolation technique and its application to organic chemistry". Chem. Soc. Rev. ج. 9: 1–23. DOI:10.1039/CS9800900001.
- ^ Basting, Dirk؛ Marowsky, Gerd (2005). Excimer Laser Technology. Springer. ISBN:3-540-20056-8.
- ^ Sanders, Robert D.؛ Ma, Daqing؛ Maze, Mervyn (2005). "Xenon: elemental anaesthesia in clinical practice". British Medical Bulletin. ج. 71 ع. 1: 115–135. DOI:10.1093/bmb/ldh034. PMID:15728132.
- ^ Albert، M. S.؛ Balamore، D. (1998). "Development of hyperpolarized noble gas MRI". Nuclear Instruments and Methods in Physics Research A. ج. 402 ع. 2–3: 441–453. Bibcode:1998NIMPA.402..441A. DOI:10.1016/S0168-9002(97)00888-7. PMID:11543065.
- ^ Ray, Sidney F. (1999). Scientific photography and applied imaging. Focal Press. ص. 383–384. ISBN:0-240-51323-1. مؤرشف من الأصل في 2020-04-06.
انظر أيضًا
[عدل]وصلات خارجية
[عدل]- نشرة جامعة أوهايولمركبات اليورنيوم مع الغازات النبيلة
- استخدامات وخواص الغازات النبيلة النيون، الكريبتون، الزينون
- استخدامات وخواص الأرجون
| H | He | |||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||





