Акрыляты
Акрыля́ты (ІЮПАК: проп-2-энааты) — солі, эстэры і спалучаныя асновы(d) акрылявай кісьлі. Іён акрыляту — аніён CH2=CHCOO−.
Апісаньне
[рэдагаваць | рэдагаваць крыніцу]Часта акрылятам называюць эстэры акрылявай кісьлі, самы распаўсюджаны зь якіх — мэтылакрылят.
У акрылятах прысутнічае вінілавая група. Такія злучэньні ўяўляюць цікавасьць дзякуючы сваёй двухфункцыйнасьці: вінілавая група адчувальная да палімэрызацыі, а карбаксылятная група мае безьліч асаблівасьцяў. Існуе таксама вялікая колькасьць мадыфікаваных акрылятаў, напрыклад мэтакрыляты (CH2=C(CH3)CO2R) і цыянаакрыляты (CH2=C(CN)CO2R)[1].
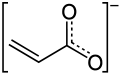
- Будова некаторых акрылятаў ды іхніх вытворных
-
Аніён акрыляту
-
Мэтылакрылят, акрылявы эстэр
-
Этыльцыянаакрылят, прадвесьнік „супэрклею“
-
Тыповы поліакрылят (зьвярніце ўвагу, якую функцыянальнасьць разьвіла вінілавая група)
Акрыляты — бясколерныя вадкасьці, лягчэйшыя за ваду, блага распускаюцца ў ёй.
Выкарыстаньне
[рэдагаваць | рэдагаваць крыніцу]Акрыляты і мэтакрыляты (солі й эстэры мэтакрылявай кісьлі) зьяўляюцца манамэрамі ў палімэрах плястыку, лёгка ўтвараючы палімэры.
Акрыляты шырока выкарыстоўваюць у вытворчасьці палімэраў, дадаюць да друкарскіх фарбаў і пастаў, у лакі й падобныя рэчывы.
Вытворчасьць
[рэдагаваць | рэдагаваць крыніцу]Прамысловы сынтэз акрылятаў адбываецца рэакцыяй акрылявай кісьлі з пэўным сьпіртам у прысутнасьці каталізатара. Рэакцыя зь ніжэйшымі сьпіртамі (мэтанолем, этанолем) праходзіць пры тэмпэратуры 100—120 °C з гетэрагенным каталізам (катыённы абмен). Рэакцыя вышэйшых сьпіртоў (н-бутаноль, 2-этылгексаноль) каталізуецца серчанай кісьляй у гамагеннай фазе. Акрыляты яшчэ вышэйшых сьпіртоў атрымліваюцца пераэстэрыфікацыяй ніжэйшых эстэраў, каталізаванай алькагалятамі тытану або арганічнымі злучэньнямі цыны(d)[2].
Крыніцы
[рэдагаваць | рэдагаваць крыніцу]- ^ Takashi Ohara, Takahisa Sato, Noboru Shimizu, Günter Prescher, Helmut Schwind, Otto Weiberg, Klaus Marten, Helmut Greim. Acrylic Acid and Derivatives // Ullmann's Encyclopedia of Industrial Chemistry. — Weinheim: Wiley-VCH, 2003. — DOI:10.1002/14356007.a01_161.pub2
- ^ Hans-Jürgen Arpe. Industrielle organische Chemie: bedeutende Vor- und Zwischenprodukte. — 6. — Weinheim: Wiley-VCH, 2007. — ISBN 978-3-527-31540-6