বেনজোয়িক অ্যাসিড
| |||

| |||
| নামসমূহ | |||
|---|---|---|---|
| পছন্দসই ইউপ্যাক নাম
বেনজোয়িক আ্যসিড (Benzoic acid)[১] | |||
| পদ্ধতিগত ইউপ্যাক নাম
বেনজিনকার্বক্সিলিক আ্যসিড | |||
অন্যান্য নাম
| |||
| শনাক্তকারী | |||
ত্রিমাত্রিক মডেল (জেমল)
|
|||
| থ্রিডিমেট | |||
| বেইলস্টেইন রেফারেন্স | ৬৩৬১৩১ | ||
| সিএইচইবিআই | |||
| সিএইচইএমবিএল | |||
| কেমস্পাইডার | |||
| ড্রাগব্যাংক | |||
| ইসিএইচএ ইনফোকার্ড | ১০০.০০০.৫৬২ | ||
| ইসি-নম্বর |
| ||
| ই নম্বর | E২১০ (সংরক্ষকদ্রব্য) | ||
| মেলিন রেফারেন্স | ২৯৪৬ | ||
| কেইজিজি | |||
| এমইএসএইচ | benzoic+acid | ||
পাবকেম CID
|
|||
| আরটিইসিএস নম্বর |
| ||
| ইউএনআইআই | |||
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|||
| |||
| |||
| বৈশিষ্ট্য | |||
| C7H6O2 | |||
| আণবিক ভর | ১২২.১২ g·mol−১ | ||
| বর্ণ | রংবিহীন স্বচ্ছ কঠিন | ||
| গন্ধ | মৃদু | ||
| ঘনত্ব | ১.২৬৫৯ গ্রাম/সেমি৩ (১৫ °C) ১.০৭৪৯ গ্রাম/সেমি৩ (১৩০ °C)[২] | ||
| গলনাঙ্ক | ১২২ °সে (২৫২ °ফা; ৩৯৫ K)[৭] | ||
| স্ফুটনাঙ্ক | ২৫০ °সে (৪৮২ °ফা; ৫২৩ K)[৭] | ||
| ১.৭ গ্রাম/লিটার (০ °সে) ২.৭ গ্রাম/লিটার (১৮ °সে) ৩.৪৪ গ্রাম/লিটার (২৫ °সে) ৫.৫১ গ্রাম/লিটার (৪০ °সে) ২১.৪৫ গ্রাম/লিটার (৭৫ °সে) ৫৬.৩১ গ্রাম/লিটার (১০০ °সে)[২][৩] | |||
| দ্রাব্যতা | আ্যসিটোন, বেনজিন, CCl4, CHCl3, আ্যলকোহল, ইথাইল ইথার, হেক্সেন, ফিনাইল, তরল আ্যমোনিয়া, আ্যসিটেট এই দ্রাবকগুলোতে দ্রাব্য | ||
| লগ পি | ১.৮৭ | ||
| বাষ্প চাপ | ০.১৬ পাস্কাল (২৫ °সে) ০.১৯ কিলোপাস্কাল (১০০ °সে) ২২.৬ কিলোপাস্কাল (২০৯ °সে)[৪] | ||
| অম্লতা (pKa) | |||
| -৭০.২৮·১০−৬ সেমি৩/মোল | |||
| প্রতিসরাঙ্ক (nD) | ১.৫৩৯৭ (২০ °সে) ১.৫০৪ (১৩২ °সে)[২] | ||
| সান্দ্রতা | ১.২৬ মিলি পাস্কাল (১৩০ °সে) | ||
| গঠন | |||
| স্ফটিক গঠন | মনোক্লিনিক | ||
| আণবিক আকৃতি | সমতল | ||
| ডায়াপল মুহূর্ত | ১.৭২ ডিবাই ডাইঅক্সেনের মধ্যে | ||
| তাপ রসায়নবিদ্যা | |||
| তাপ ধারকত্ব, C | ১৪৬.৭ জুল/মোল·কেলভিন[৪] | ||
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
১৬৭.৬ জুল/মোল·কেলভিন[২] | ||
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
-৩৮৫.২ কিলোজুল/মোল[২] | ||
| দহনে প্রমান এনথ্যাল্পির পরিবর্তন ΔcH |
-৩২২৮ কিলোজুল/মোল[৪] | ||
| ঝুঁকি প্রবণতা | |||
| প্রধান ঝুঁকিসমূহ | যন্ত্রণাদায়ক | ||
| নিরাপত্তা তথ্য শীট | JT Baker | ||
| জিএইচএস চিত্রলিপি |   [৮] [৮]
| ||
| জিএইচএস সাংকেতিক শব্দ | বিপদজনক | ||
| জিএইচএস বিপত্তি বিবৃতি | H318, H335[৮] | ||
| জিএইচএস সতর্কতামূলক বিবৃতি | P261, P280, P305+351+338[৮] | ||
| এনএফপিএ ৭০৪ | |||
| ফ্ল্যাশ পয়েন্ট | ১২১.৫ °সে (২৫০.৭ °ফা; ৩৯৪.৬ K)[৭] | ||
| ৫৭১ °সে (১,০৬০ °ফা; ৮৪৪ K)[৭] | |||
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |||
LD৫০ (মধ্যমা ডোজ)
|
1700 mg/kg (rat, oral) | ||
| সম্পর্কিত যৌগ | |||
সম্পর্কিত কার্বক্সিলিক আ্যসিড
|
হাইড্রক্সিবেনজয়িক আ্যসিড আ্যমিনোবেনজয়িক আ্যসিড, নাইট্রোবেনজয়িক আ্যসিড, ফিনাইলআ্যসিটিক আ্যসিড | ||
সম্পর্কিত যৌগ
|
বেঞ্জালডিহাইড, বেঞ্জাইল আ্যলকোহল, বেনজোইল ক্লোরাইড, বেঞ্জাইল আ্যমিন, বেঞ্জামাইড | ||
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |||
| তথ্যছক তথ্যসূত্র | |||
বেনজোয়িক আ্যসিড হল রংবিহীন স্বচ্ছ কঠিন এবং সরলতম আ্যরোমেটিক কার্বক্সিলিক আ্যসিড। নামটি আঠা জাতীয় পদার্থ বেনজোয়েন (রেজিন) থেকে করা হয়েছে, যেটি বহুসময় ধরে এটির একমাত্র জানা উৎস ছিল। বেনজোয়িক আ্যসিড প্রাকৃতিকভাবে বিভিন্ন গাছ[৯] থেকে উৎপন্ন হয় এবং অনেক দ্বিতীয় পর্যায়ের মেটাবোলাইটের জৈবসংশ্লেষনে অন্তর্বর্তী হিসাবে কাজ করে। বেনজোয়িক আ্যসিডের লবণগুলো খাদ্য সংরক্ষক হিসাবে ব্যবহার করা হয় এবং বেনজোয়িক আ্যসিড হল বিভিন্ন জৈব যৌগ প্রস্তুতির জন্য একটি গুরুত্বপূর্ণ যৌগ। বেনজোয়িক আ্যসিডের লবণ ও এস্টারগুলো বেনজোয়েট নামে পরিচিত।
ইতিহাস
[সম্পাদনা]ষোলোর দশকে বেনজোয়িক আ্যসিড আবিষ্কার হয়। আঠালো বেনজোয়েনের শুষ্ক পাতন প্রথম ব্যাখ্যা করেছিলেন নস্ট্রাদামুস (১৫৫৬ সাল), তারপর আলেক্সিউস পেডেমন্তনুস (১৫৬০) এবং ব্লাইসে দে ভিগেনরে (১৫৯৬)।[১০]
আমিগ্যালিনের উপর ভিত্তি করে ১৮৩০ সালের বিভিন্ন অভিজ্ঞতার কাজ, যা তিক্ত কাজুবাদামের তেল থেকে প্রাপ্ত দুই ফরাসি রসায়নবিদ দ্বারা, বেঞ্জালডিহাইড[১১] প্রস্তুত করেছিলেন। কিন্তু তারা আমিগ্যালিনের গঠনের সঠিক ব্যাখ্যার উপর কাজ করতে ব্যর্থ হয়েছিলেন, ফলে বেনজোইল র্যাডিকালের (C7H5O.) উপস্থিতি তারা বুঝতে পারেননি। কয়েক মাস পরে জুউস ভন লিবিগ এবং ফ্রেডরিক ওয়ায়োলার ১৮৩২ সালে শেষ ধাপটি সম্পূর্ণ করতে সক্ষম হন, যারা বেনজোয়িক আ্যসিডের কমপজিশন নির্ধারণ করেন।[১২] পরবর্তীতে আরও গবেষণা করে দেখা যায় যে হিপপিউরিক আ্যসিড কীভাবে বেনজোয়িক আ্যসিডের সাথে সম্পর্কিত।
১৮৭৫ সালে সালকউস্কি (একজন বিজ্ঞানী) বেনজোয়িক আ্যসিডের অ্যান্টিফাঙ্গাল ক্ষমতা আবিষ্কার করেন, যা দীর্ঘদিন ধরে ব্যবহার করা হত বেনজোয়েট-যুক্ত ক্লাউডবেরি ফল সংরক্ষণে।[১৩]
এটি একটি রাসায়নিক যৌগ যা ক্যাস্টোরমে পাওয়া যায়। উত্তর আমেরিকার বিভার ক্যাস্টর থলি থেকে এই যৌগ জড়ো করা হয়।
উৎপাদন
[সম্পাদনা]শিল্পে প্রস্তুতি
[সম্পাদনা]বেনজোয়িক আ্যসিড অক্সিজেনের সাথে টলুইনের আংশিক জারণের (অক্সিডেশন) দ্বারা বাণিজ্যিকভাবে উৎপাদিত করা হয়। বিক্রিয়াটি কোবাল্ট বা ম্যাঙ্গানিজ ন্যাপথেনেট দ্বারা ত্বরান্বিত করা হয়। বিক্রিয়াটিতে প্রচুর উপকরণ ব্যবহৃৎ হয়, উচ্চ ফলাফলের সাথে এগিয়ে যায়।[১৪]

শিল্পে প্রথম পদ্ধতিটি ছিল বেনজোট্রাইক্লোরাইডের (ট্রাইক্লোরোমিথাইল বেনজিন) সাথে ক্যালসিয়াম হাইড্রোঅক্সাইডের জলের মধ্যে বিক্রিয়া, আয়রন (লোহা) বা আয়রন সল্ট অনুঘটক হিসাবে ব্যবহার করে। প্রাপ্ত ক্যালসিয়াম বেনজোয়েটকে হাইড্রোক্লোরিক আ্যসিড দিয়ে বেনজোয়িক আ্যসিডে রূপান্তরিত করা হয়। বিক্রিয়াজাত পদার্থের মধ্যে উল্লেখযোগ্য পরিমানে ক্লোরিন যুক্ত বেনজোয়িক আ্যসিড ডেরিভেটিভ উপস্থিত থাকে। এই কারণে, মানুষের ব্যবহারের জন্য বেনজোয়িক আ্যসিড বেনজোয়েনের শুষ্ক পাতন থেকে পাওয়া যায়। ফুড-গ্রেড বেনজোয়িক আ্যসিড এখন সিন্থেটিকভাবে উৎপাদিত হয়।
ল্যাবরেটরিতে প্রস্তুতি
[সম্পাদনা]বেনজোয়িক আ্যসিড হল সস্তা এবং সহজলভ্য, তাই ল্যাবোরেটরিতে প্রস্তুত বেনজোয়িক আ্যসিড মূলত তার শিক্ষামানের জন্য অনুশীলন করা হয়। এটি একটি সাধারণ স্নাতক স্তরের প্রস্তুতি।
গরম জলে উচ্চ দ্রাব্যতা এবং ঠান্ডা জলে কম দ্রাব্যতার কারণে বেনজোয়িক আ্যসিড জল থেকে রিক্রিস্টালাইজেশন দ্বারা পরিশুদ্ধ করা যেতে পারে। রিক্রিস্টালাইজেশনের জন্য জৈব দ্রাবক ব্যবহার না করা এই পরীক্ষাটিকে বিশেষভাবে নিরাপদ করে তোলে। পদ্ধতিটি সাধারণত ৬৫% বিক্রিয়াজাত পদার্থ উৎপন্ন করে।[১৫]
হাইড্রোলাইসিসের দ্বারা
[সম্পাদনা]ক্ষারীয় বা অম্লীয় (আ্যসিডিক) অবস্থায় অন্যান্য নাইট্রাইল এবং আ্যমাইড, বেনজোনাইট্রাইল এবং বেঞ্জামাইড এর মত যৌগগুলোকে বেনজোয়িক আ্যসিড বা তার কনজুগেট ক্ষারে হাইড্রোলাইজ করা যেতে পারে।
গ্রিগনার্ড বিকারক থেকে
[সম্পাদনা]ব্রোমোবেনজিনকে বেনজোয়িক আ্যসিডে রূপান্তরিত করা যেতে পারে অন্তর্বর্তী ফিনাইলম্যাগনেসিয়াম ব্রোমাইডের কার্বক্সিলেশন দ্বারা।[১৬] এই পদ্ধতিটি গ্রিগনার্ড বিক্রিয়া চালানোর জন্য ছাত্রছাত্রীদের সুবিধাজনক অনুশীলন প্রদান করে, জৈব রসায়নে কার্বন-কার্বন বন্ধন তৈরির একটি গুরুত্বপূর্ণ বিক্রিয়া।[১৭][১৮]
বেঞ্জাইল যৌগের অক্সিডেশন দ্বারা
[সম্পাদনা]বেনজাইল অ্যালকোহল এবং বেনজাইল ক্লোরাইড এবং কার্যত সব বেনজাইল ডেরিভেটিভগুলো খুব সহজে বেনজোয়িক আ্যসিডে রূপান্তরিত করা যায় অক্সিডেশন দ্বারা।
ব্যবহার
[সম্পাদনা]বেনজোয়িক আ্যসিড প্রধানত ৩০০-৪০০°সেন্টিগ্রেড তাপমাত্রায় অক্সিডেটিভ ডিকার্বক্সিলেশন দ্বারা ফেনল উৎপাদনে বব্যবহার হয়:[১৯]
- C6H5CO2H + +২/১ O2 → C6H5OH + CO2
প্রয়োজনীয় তাপমাত্রা ২০০ ডিগ্রি সেন্টিগ্রেড পর্যন্ত কমানো যেতে পারে অনুঘটকীয় পরিমাণ কপার (II) সল্ট ব্যবহার করে। ফেনলকে রূপান্তরিত করা যেতে পারে সাইক্লোহেক্সানলে, যা নাইলন তৈরির একটি প্রাথমিক উপাদান।
প্লাস্টিসাইজারের উপাদান
[সম্পাদনা]বেনজোয়েট প্লাস্টিসাইজার, যেমন গ্লাইকল-, ডাইইথিলিনগ্লাইকল-, ট্রাইইথিলিনগ্লাইকল এস্টারগুলো সংশ্লিষ্ট ডাইঅলের সাথে মিথাইল বেনজোয়েটের ট্রান্সএস্টারিফিকেশন দ্বারা পাওয়া যায়। বিকল্পভাবে এই যৌগগুলো ডাইঅলের সাথে বেনজোয়িলক্লোরাইডের বিক্রিয়ায় উৎপন্ন হয়। এই প্লাস্টিসাইজারগুলো একইভাবে টেরিথ্যালিক আ্যসিড এস্টার থেকে প্রাপ্ত প্লাস্টিসাইজারগুলোর মত ব্যবহৃত হয়।
সোডিয়াম বেনজোয়েট এবং সম্পর্কিত সংরক্ষকগুলোর অগ্রদূত
[সম্পাদনা]বেনজোয়িক আ্যসিড এবং এর লবণগুলো খাদ্য সংরক্ষক হিসাবে ব্যবহৃত হয়, E-সংখ্যা দ্বারা প্রকাশ করা হয় যেমন E210 (বেনজোয়িক আ্যসিড নিজেই), E211 (সোডিয়াম বেনজোয়েট), E212 (পটাশিয়াম বেনজোয়েট) এবং E213 (ক্যালসিয়াম বেনজোয়েট)। বেনজোয়িক আ্যসিড ছাঁচ, খামির এবং কিছুকিছু ব্যাকটেরিয়ার বৃদ্ধি বাধা দেয়।[২০] এটি সরাসরি যোগ করা হয় বা তার সোডিয়াম, পটাশিয়াম, বা ক্যালসিয়াম লবণের সঙ্গে বিক্রিয়া করিয়ে যোগ করা হয়। প্রতিক্রিয়াটি কোষের মধ্যে বেনজোয়িক আ্যসিডের শোষণের সঙ্গে শুরু হয়। যদি কোষ-অভ্যন্তরীণ পি.এইচ (pH) ৫ বা তার বেশি কমে যায়, তাহলে ফসফোফ্রুক্টোকিনেজের মাধ্যমে গ্লুকোজের অ্যানেরবিক ফারম্যানটেশন ৯৫ শতাংশ কমে যায়। সুতরাং বেনজোয়িক আ্যসিড এবং বেনজোয়েটের কার্যকারিতা খাবারের pH এর উপর নির্ভরশীল।[২১] অম্লীয় খাদ্য ও পানীয় যেমন ফলের রস (সাইট্রিক আ্যসিড), চমৎকার পানীয় (কার্বন ডাইঅক্সাইড), নরম পানীয় (ফসফরিক আ্যসিড), আঁচার (ভিনিগার) এবং অন্যান্য অম্লীয় খাদ্যগুলো বেনজোয়িক আ্যসিড এবং বেনজোয়েট দ্বারা সংরক্ষণ করা হয়।
খাদ্য সংরক্ষক হিসাবে বেনজোয়িক আ্যসিড ব্যবহারের সাধারণ মাত্রা হল ০.০৫-০.১ শতাংশ। যে খাবারগুলোতে বেনজিক অ্যাসিড ব্যবহার করা যেতে পারে তার প্রয়োগের সর্বাধিক মাত্রা স্থানীয় খাদ্য আইন দ্বারা নিয়ন্ত্রিত হয়।[২২][২৩]
উদ্বেগ প্রকাশ করা হয়েছে যে বেনজোয়িক আ্যসিড এবং এর লবণগুলো কিছুকিছু নরম পানীয়র মধ্যে অ্যাসকরবিক আ্যসিডের (ভিটামিন সি) সাথে বিক্রিয়া করতে পারে, যা সামান্য পরিমানে কার্সিনোজেনিক বেনজিন উৎপন্ন করে।
ঔষধসম্বন্ধীয়
[সম্পাদনা]বেনজোয়িক আ্যসিড হল হোয়াইটফিল্ড মলমের উপাদান যা ফাংগাল জাতীয় চর্ম রোগ যেমন তিনিয়া, রিংঅৰ্ম এবং আ্যথলিট ফুটের চিকিত্সার জন্য ব্যবহার করা হয়।[২৪] গাম বেনজোয়েনের এর প্রধান উপাদান হিসাবে, বেনজোয়িক আ্যসিড এছাড়াও বেনজোয়েন এবং ফ্রিয়ারের বলসাম উভয় মিশ্রণে একটি প্রধান উপাদান। টপিকাল অ্যান্টিসেপটিকস এবং ইনহল্যান্ট ডিকনগেসট্যান্টস হিসাবে এই যৌগগুলোর ব্যবহারের দীর্ঘ ইতিহাস রয়েছে।
কুড়ি শতকের প্রথম দিকে বেনজোয়িক আ্যসিড এক্সপেক্টোরান্ট, বেদনানাশক এবং জীবাণুনাশক হিসাবে ব্যবহার করা হতো।[২৫]
বেনজোয়িল ক্লোরাইড
[সম্পাদনা]বেনজোয়িক আ্যসিড হল বেনজোয়িল ক্লোরাইড প্রস্তুতির অগ্রদূত, C6H5C(O)Cl পাওয়া যায় থায়োনিল ক্লোরাইড, ফসজিন বা ফসফরাস হ্যালাইডের সাথে বিক্রিয়ায়। বেনজোয়িল ক্লোরাইড হল বিভিন্ন বেনজোয়িক আ্যসিড ডেরিভেটিভ যেমন বেঞ্জাইল বেনজোয়েট প্রস্তুতির শুরুর উপাদান, যা কৃত্রিম ফ্লেভার এবং পোকামাকড় তাড়াতে ব্যবহার হয়।
ল্যাবরেটরিতে ব্যবহার
[সম্পাদনা]শিক্ষনীয় ল্যাবরেটরিগুলোতে বেনজোয়িক আ্যসিড হল বোম্ব ক্যালোরিমিটার এর ক্রমান্ক করার জন্য একটি সাধারণ সাপেক্ষ।[২৬]
জীববিজ্ঞানে এবং স্বাস্থ্যে প্রভাব
[সম্পাদনা]বেনজোয়িক আ্যসিড প্রাকৃতিকভাবে অনেক উদ্ভিদ ও প্রাণী প্রজাতিতে পাওয়া যায় যেমন তার এস্টার। যথেষ্ট পরিমাণ বেরি ফলের মধ্যেই পাওয়া যায় (০.০৫ শতাংশের কাছাকাছি)। বিভিন্ন ভ্যাকসিনিয়াম প্রজাতির পাকা ফলগুলোতে (যেমন ক্র্যানবেরি, ভি. ভাইটিস ম্যাক্রোকার্পন, ভি. মিরটিলাস) ০.০৩-০.১৩% বেনজোয়িক আ্যসিড মুক্ত হিসাবে থাকে। বেনজোয়িক আ্যসিড এছাড়াও নেকট্রিয়া গ্যালিগেনা নামক ছত্রাক সংক্রমনের ফলে আপেলের মধ্যে গঠিত হয়। পশুদের মধ্যে, বেনজোয়িক আ্যসিড প্রাথমিকভাবে সর্বভুবিক বা ফাইটোফ্যাগিয়াস প্রজাতিদের মধ্যে চিহ্নিত করা হয়েছে যেমন ভিসেরা, রক টারমিগ্যানের (ল্যাগোপাস মুটা) পেশী, পাশাপাশি পুরুষ মসকোক্সন বা এশীয় হাতির (এলিফ্যাজ ম্যাক্সিমাস) গ্রন্থি নিঃসরণ রসের মধ্যে।[২৭] আঠালো বেনজোয়েনের মধ্যে ২০% বেনজোয়িক আ্যসিড এবং ৪০% বেনজোয়িক আ্যসিড এস্টার থাকে।[২৮]
জৈবসংশ্লেষনের মতে, উদ্ভিদে সিনামিক আ্যসিড থেকে বেনজোয়েট উৎপন্ন হয়।[২৯] ফেনল থেকে ৪-হাইড্রক্সিবেনজোয়েটের মাধ্যমে বেনজোয়িক আ্যসিড প্রস্তুতির একটি পদ্ধতি চিহ্নিত করা হয়েছে।[৩০]
বিক্রিয়াগুলো
[সম্পাদনা]বেনজোয়িক আ্যসিডের বিক্রিয়াগুলো বেনজিন বলয়ে বা কার্বক্সিল গ্রুপে হতে পারে:
আ্যরোমেটিক রিং
[সম্পাদনা]ইলেক্ট্রফিলিক আ্যরোমেটিক সাবস্টিটিউশন বিক্রিয়া (বেনজিন বলয়ের হাইড্রোজেন ইলেক্ট্রফাইল দ্বারা প্রতিস্থাপন) প্রধানত ৩ নম্বর স্থানে হয়, কার্বক্সিলিক গ্রুপের ইলেক্ট্রন উইথড্রইং ধর্মের জন্য, সুতরাং বেনজোয়িক আ্যসিড মেটা-নির্দেশিকা।
দ্বিতীয় প্রতিস্থাপন বিক্রিয়াটি (ডানদিকে) ধীর গতিসম্পন্ন কারণ প্রথম নাইট্রো গ্রুপটি বেনজিন বলয়কে নিষ্ক্রিয় করে তোলে।[৩১] বিপরীতক্রমে, যদি একটি সক্রিয়করন গ্রুপ (ইলেক্ট্রন ডোনেটিং) যুক্ত করা হয় (যেমন আ্যলকাইল), তাহলে দ্বিতীয় প্রতিস্থাপন বিক্রিয়াটি প্রথমটির তুলনায় সহজেই ঘটতে পারে, এবং দ্বি-প্রতিস্থাপিত বিক্রিয়াজাত পদার্থটি যথেষ্ট পরিমাণে উৎপন্ন হতে পারে।
কার্বক্সিল গ্রুপ
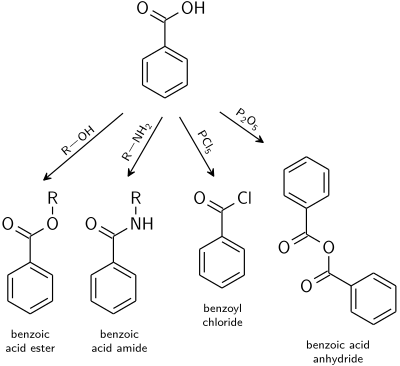
[সম্পাদনা]কার্বক্সিলিক আ্যসিডের জন্য উল্লিখিত বিক্রিয়াগুলো বেনজোয়িক আ্যসিডের জন্যও সম্ভব।
- বেনজোয়িক আ্যসিড এস্টারগুলো আ্যলকোহলের সাথে আ্যসিড অনুঘটকীয় বিক্রিয়ার ফলে উৎপন্ন হয়।
- বেনজোয়িক আ্যসিড আ্যমাইডগুলো খুব সহজেই পাওয়া যায় সক্রিয় আ্যসিড ডেরিভেটিভ ব্যবহার করে (যেমন বেনজোয়িল ক্লোরাইড), অথবা DCC এবং DMAP এর মতো পেপটাইড সংশ্লেষনে ব্যবহৃত কাপলিং বিকারকগুলো ব্যবহার করে।
- আরও সক্রিয় বেনজোয়িক আ্যনহাইড্রাইড তৈরি হয় জল শোষণের ফলে আ্যসিটিক আ্যনহাইড্রাইড বা ফসফরাস পেন্টাঅক্সাইড ব্যবহার করে।
- অ্যাসিড হ্যালাইডের মতো অত্যন্ত প্রতিক্রিয়াশীল অ্যাসিড ডেরিভেটিভিগুলো সহজেই পাওয়া যায় ফসফরাস ক্লোরাইড এবং থায়োনিল ক্লোরাইড এর মতো হ্যালোজিনেশন যৌগগুলোর সাথে মিশিয়ে।
- অর্থোএস্টার পাওয়া যেতে পারে আ্যসিড মুক্ত অবস্থায় বেনজোনাইট্রাইলের সাথে আ্যলকোহলের বিক্রিয়ায়।
- DIBAL-H, LiAlH4 কিংবা [[সোডিয়াম বোরোহাইড্রাইড|NaBH<sub
4 ব্যবহার করে বেঞ্জালডিহাইড এবং বেনজাইল আ্যলকোহলে বিজারিত করা যায়।
- কুইনোলিনের এর মধ্যে গরম করলে কপার অনুঘটকীয় বেনজোয়েটের ডিকার্বক্সিলেশন প্রভাবিত হতে পারে। এছাড়াও, হুন্সডিকার ডিকার্বক্সিলেশন সিলভার সল্ট তৈরি এবং গরম করার মাধ্যমে অর্জন করা যেতে পারে। বেনজোয়িক অ্যাসিডকে ক্ষারীয় হাইড্রক্সাইড বা ক্যালসিয়াম হাইড্রক্সাইডের সাথে গরম করে ডিকার্বক্সিলেট করা যেতে পারে।
নিরাপত্তা এবং স্তন্যপায়ী প্রাণীর বিপাক
[সম্পাদনা]এটি হিপপিউরিক অ্যাসিড হিসাবে নির্গত হয়।[৩২] বিউটাইরেট-CoA লাইগেজ দ্বারা বেনজোয়িক আ্যসিড বিপাকের ফলে মধ্যবর্তী বেনজোয়িল-CoA[৩৩] যে রূপান্তরিত হয়, পরে যেটি গ্লাইসিন-N-আ্যসাইলট্রান্সফেরেজ দ্বারা বিপাকীয় প্রক্রিয়ার মাধ্যমে হিপপিউরিক আ্যসিডে রূপান্তরিত হয়।[৩৪] টলুইন এবং বেনজোয়িক আ্যসিডকে মানুষ বিপাকের সাহায্যে হিপপিউরিক অ্যাসিড হিসাবে নির্গত করে।[৩৫]
মানুষের জন্য, বিশ্ব স্বাস্থ্য সংস্থার ইন্টারন্যাশনাল প্রোগ্রাম অন কেমিক্যাল সেফটি (আইপিসিএস) থেকে জানা যায়, একটি অস্থায়ী সহনীয় মানুষের জন্য প্রতিদিন ৫ মিলিগ্রাম/কেজি শরীরের ওজন প্রতি বেনজোয়িক আ্যসিড প্রয়োজন।[২৭] বিড়ালের বেনজোয়িক আ্যসিড এবং তার সল্টগুলোর প্রতি ইঁদুরের চেয়ে উল্লেখযোগ্যভাবে নিম্ন সহনশীলতা আছে। বিড়াল জন্য প্রাণঘাতী ডোজ ৩০০ মিলিগ্রাম/কেজি শরীরের ওজন হিসাবে কম হতে পারে।[৩৬]
তাইপে, তাইওয়ান, ২০১০ সালে একটি শহরের স্বাস্থ্য সমীক্ষায় দেখা গেছে যে ৩০% শুকনো এবং আচার জাতীয় খাদ্যে বেনজোয়িক আ্যসিড ছিল।
তথ্যসূত্র
[সম্পাদনা]- ↑ "Front Matter"। Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)। Cambridge: The Royal Society of Chemistry। ২০১৪। পৃষ্ঠা 745। আইএসবিএন 978-0-85404-182-4। ডিওআই:10.1039/9781849733069-FP001।
- ↑ ক খ গ ঘ ঙ "benzoic acid"। chemister.ru। ২৩ মে ২০১৪ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২৪ অক্টোবর ২০১৮।
- ↑ Seidell, Atherton; Linke, William F. (১৯৫২)। Solubilities of Inorganic and Organic Compounds। Van Nostrand। সংগ্রহের তারিখ ২০১৪-০৫-২৯।
- ↑ ক খ গ Benzoic acid in Linstrom, P.J.; Mallard, W.G. (eds.) NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD. http://webbook.nist.gov (retrieved 2014-05-23)
- ↑ Harris, Daniel (২০১০)। Quantitative Chemical Analysis (8 সংস্করণ)। New York: W. H. Freeman and Company। পৃষ্ঠা AP12। আইএসবিএন 9781429254366।
- ↑ Olmstead, William N.; Bordwell, Frederick G. (১৯৮০)। "Ion-pair association constants in dimethyl sulfoxide"। The Journal of Organic Chemistry। 45 (16): 3299–3305। ডিওআই:10.1021/jo01304a033।
- ↑ ক খ গ ঘ Record in the GESTIS Substance Database from the IFA
- ↑ ক খ গ Sigma-Aldrich Co. Retrieved on 2014-05-23.
- ↑ "Scientists uncover last steps for benzoic acid creation in plants - Purdue University"। www.purdue.edu। ২০২১-১২-২৩ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০১৯-০৮-০৯।
- ↑ Neumüller, Otto-Albrecht. (১৯৮৮)। Römpps Chemie-Lexikon / 6, T - Z. (8., neubearb. u. erw. Aufl সংস্করণ)। Stuttgart: Franckh। আইএসবিএন 3440045161। ওসিএলসি 311075142।
- ↑ Wisniak, Jaime (২০১৮-০৮-২৫)। "Pierre-Jean Robiquet"। Educación Química (ইংরেজি ভাষায়)। 24 (1): 139 – 149–149। আইএসএসএন 1870-8404। ডিওআই:http://dx.doi.org/10.1016/S0187-893X(13)72507-2
|doi=এর মান পরীক্ষা করুন (সাহায্য)। - ↑ Wöhler; Liebig (১৮৩২)। "Untersuchungen über das Radikal der Benzoesäure"। Annalen der Pharmacie (ইংরেজি ভাষায়)। 3 (3): 249–282। আইএসএসএন 1099-0690। ডিওআই:10.1002/jlac.18320030302।
- ↑ "Veranstaltungstipps:"। Wiener klinische Wochenschrift। 131 (11-12): 297–298। 2019-06। আইএসএসএন 0043-5325। ডিওআই:10.1007/s00508-019-1520-7। এখানে তারিখের মান পরীক্ষা করুন:
|তারিখ=(সাহায্য) - ↑ "Book sources"। Wikipedia (ইংরেজি ভাষায়)।
- ↑ Perrin, D. D. (Douglas Dalzell), 1922- (১৯৮৮)। Purification of laboratory chemicals। Armarego, W. L. F. (3rd ed সংস্করণ)। Oxford: Pergamon Press। আইএসবিএন 0080347150। ওসিএলসি 18018739।
- ↑ Introduction to organic laboratory techniques : a small scale approach। Pavia, Donald L. (2nd ed সংস্করণ)। Belmont, CA: Thomson Brooks/Cole। ২০০৫। আইএসবিএন 0534408338। ওসিএলসি 56051109।
- ↑ Shirley, David A. (২০১১)। Organic Reactions (ইংরেজি ভাষায়)। American Cancer Society। পৃষ্ঠা 28–58। আইএসবিএন 9780471264187। ডিওআই:10.1002/0471264180.or008.02/abstract।
- ↑ Huryn, Donna M. (১৯৯১-০১-০১)। Trost, Barry M.; Fleming, Ian, সম্পাদকগণ। Comprehensive Organic Synthesis। Oxford: Pergamon। পৃষ্ঠা 49–75। আইএসবিএন 9780080523491। ডিওআই:10.1016/b978-0-08-052349-1.00002-0।
- ↑ Maki, Takao; Takeda, Kazuo (২০০০)। Ullmann's Encyclopedia of Industrial Chemistry (ইংরেজি ভাষায়)। American Cancer Society। আইএসবিএন 9783527306732। ডিওআই:10.1002/14356007.a03_555।
- ↑ Warth, A. D. (১৯৯১-১২-০১)। "Mechanism of action of benzoic acid on Zygosaccharomyces bailii: effects on glycolytic metabolite levels, energy production, and intracellular pH."। Applied and Environmental Microbiology (ইংরেজি ভাষায়)। 57 (12): 3410–3414। আইএসএসএন 0099-2240। পিএমআইডি 1785916। ২০১৯-০৮-২৯ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০১৯-০৮-২৯।
- ↑ Pastorova, I.; Koster, C. G. de; Boon, J. J. (১৯৯৭)। "Analytical Study of Free and Ester Bound Benzoic and Cinnamic Acids of Gum Benzoin Resins by GC–MS and HPLC–frit FAB–MS"। Phytochemical Analysis (ইংরেজি ভাষায়)। 8 (2): 63–73। আইএসএসএন 1099-1565। ডিওআই:10.1002/(SICI)1099-1565(199703)8:23.0.CO;2-Y।
- ↑ "GSFA Online Food Additive Group Details: Benzoates (2006)"। ২৬ সেপ্টেম্বর ২০০৭ তারিখে মূল থেকে আর্কাইভ করা।
- ↑ "Wayback Machine" (পিডিএফ)। web.archive.org। ২০০৩-০৪-১৯। Archived from the original on ২০০৩-০৪-১৯। সংগ্রহের তারিখ ২০১৯-০৮-২৯।
- ↑ Wilson and Gisvold's textbook of organic medicinal and pharmaceutical chemistry। Wilson, Charles Owens, 1911-, Gisvold, Ole, 1904-, Block, John H., Beale, John Marlowe. (11th ed সংস্করণ)। Philadelphia: Lippincott Williams & Wilkins। ২০০৪। আইএসবিএন 0781734819। ওসিএলসি 52079928।
- ↑ Lillard, Benjamin (১৯১৯)। Practical Druggist and Pharmaceutical Review of Reviews (ইংরেজি ভাষায়)। Lillard & Company।
- ↑ "Wayback Machine" (পিডিএফ)। web.archive.org। ২০১২-০৩-০৯। Archived from the original on ২০১২-০৩-০৯। সংগ্রহের তারিখ ২০১৯-০৮-২৯।
- ↑ ক খ "BENZOIC ACID AND SODIUM BENZOATE"। www.inchem.org। সংগ্রহের তারিখ ২০১৯-০৮-২৯।
- ↑ Tomokuni, K.; Ogata, M. (1972-4)। "Direct colorimetric determination of hippuric acid in urine"। Clinical Chemistry। 18 (4): 349–351। আইএসএসএন 0009-9147। পিএমআইডি 5012256। এখানে তারিখের মান পরীক্ষা করুন:
|তারিখ=(সাহায্য) - ↑ Vogt, Thomas (২০১০-০১-০১)। "Phenylpropanoid Biosynthesis"। Molecular Plant (English ভাষায়)। 3 (1): 2–20। আইএসএসএন 1674-2052। ডিওআই:10.1093/mp/ssp106। পিএমআইডি 20035037।
- ↑ Juteau, Pierre; Côté, Valérie; Duckett, Marie-France; Beaudet, Réjean; Lépine, François; Villemur, Richard; Bisaillon, Jean-Guy (২০০৫)। "Cryptanaerobacter phenolicus gen. nov., sp. nov., an anaerobe that transforms phenol into benzoate via 4-hydroxybenzoate"। International Journal of Systematic and Evolutionary Microbiology,। 55 (1): 245–250। আইএসএসএন 1466-5026। ডিওআই:10.1099/ijs.0.02914-0।
- ↑ "http://www.orgsyn.org/demo.aspx?prep=cv3p0337"। www.orgsyn.org (ইংরেজি ভাষায়)। সংগ্রহের তারিখ ২০১৯-০৮-২৯।
|title=এ বহিঃসংযোগ দেয়া (সাহায্য) - ↑ "Final Report on the Safety Assessment of Benzyl Alcohol, Benzoic Acid, and Sodium Benzoate"। International Journal of Toxicology (ইংরেজি ভাষায়)। 20 (3_suppl): 23–50। 2001-01। আইএসএসএন 1091-5818। ডিওআই:10.1080/10915810152630729। এখানে তারিখের মান পরীক্ষা করুন:
|তারিখ=(সাহায্য) - ↑ "BRENDA - Information on EC 6.2.1.2 - medium-chain acyl-CoA ligase"। www.brenda-enzymes.org। সংগ্রহের তারিখ ২০১৯-০৮-২৯।
- ↑ "BRENDA - Information on EC 2.3.1.13 - glycine N-acyltransferase"। www.brenda-enzymes.info। সংগ্রহের তারিখ ২০১৯-০৮-২৯।
- ↑ Krebs, H. A.; Wiggins, D.; Stubbs, M.; Sols, A.; Bedoya, F. (১৯৮৩-০৯-১৫)। "Studies on the mechanism of the antifungal action of benzoate"। The Biochemical Journal। 214 (3): 657–663। আইএসএসএন 0264-6021। ডিওআই:10.1042/bj2140657। পিএমআইডি 6226283। পিএমসি 1152300
 ।
।
- ↑ Clarke, E. G.; Bedford, P. G. (১৯৭২-০১-১৫)। "Experimental benzoic acid poisoning in the cat"। Veterinary Record (ইংরেজি ভাষায়)। 90 (3): 53–58। আইএসএসএন 0042-4900। ডিওআই:10.1136/vr.90.3.53। ২০১৯-০৮-২৯ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০১৯-০৮-২৯।