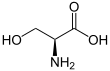
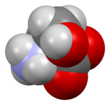
সেরিন
| |||
| |||
| নামসমূহ | |||
|---|---|---|---|
| ইউপ্যাক নাম
Serine
| |||
| অন্যান্য নাম
2-Amino-3-hydroxypropanoic acid
| |||
| শনাক্তকারী | |||
ত্রিমাত্রিক মডেল (জেমল)
|
|||
| সিএইচইবিআই |
| ||
| সিএইচইএমবিএল |
| ||
| কেমস্পাইডার | |||
| ড্রাগব্যাংক |
| ||
| ইসিএইচএ ইনফোকার্ড | ১০০.০০০.২৫০ | ||
| ইসি-নম্বর |
| ||
| |||
| কেইজিজি | |||
পাবকেম CID
|
|||
| ইউএনআইআই |
| ||
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|||
| |||
| |||
| বৈশিষ্ট্য[২] | |||
| C3H7NO3 | |||
| আণবিক ভর | ১০৫.০৯ g·mol−১ | ||
| বর্ণ | সাদা কেলাস বা দানা | ||
| ঘনত্ব | ১.৬০৩ g/cm3 (২২ °C) | ||
| গলনাঙ্ক | ২৪৬ ডিগ্রি সেলসিয়াস (৪৭৫ ডিগ্রি ফারেনহাইট; ৫১৯ kelvin) ভেঙে যায় | ||
| দ্রাব্য | |||
| অম্লতা (pKa) | ২.২১ (কার্বক্সিল), ৯.১৫ (অ্যামিনো)[১] | ||
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |||
| তথ্যছক তথ্যসূত্র | |||
সেরিন (চিহ্ন Ser বা S)[৩][৪] হল একটি α-অ্যামিনো অ্যাসিড যা প্রোটিনের জৈব সংশ্লেষণে ব্যবহৃত হয়। এটিতে একটি α-অ্যামিনো গ্রুপ রয়েছে (প্রোটোনেটেড হয়ে NH+
3 গঠন ধারণ করে), একটি কার্বক্সিল গ্রুপ (ডিপ্রোটোনেটেড হয়ে COO−
গঠন ধারণ করে), এবং একটি হাইড্রক্সিমিথাইল গ্রুপ নিয়ে গঠিত একটি পার্শ্ব শৃঙ্খল রয়েছে। এটি পোলার অ্যামিনো অ্যাসিড। এটি সাধারণ শারীরবৃত্তীয় পরিস্থিতিতে মানবদেহে সংশ্লেষিত হতে পারে। তাই এটিকে অ-অপরিহার্য অ্যামিনো অ্যাসিড বিবেচনা করা হয়। এটি কোডন UCU, UCC, UCA, UCG, AGU এবং AGC দ্বারা এনকোড করা হয়।
অবস্থা
[সম্পাদনা]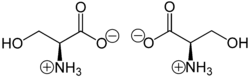
এই যৌগটি প্রোটিনোজেনিক অ্যামিনো অ্যাসিডগুলির মধ্যে একটি। প্রোটিনগুলিতে শুধুমাত্র L-স্টেরিওআইসোমার প্রাকৃতিকভাবে উপস্থিত হয়। এটি মানব খাদ্যের জন্য অপরিহার্য নয়, কারণ এটি গ্লাইসিন সহ অন্যান্য বিপাক থেকে শরীরে সংশ্লেষিত হয়। ১৮৬৫ সালে এমিল ক্রেমার দ্বারা বিশেষভাবে সমৃদ্ধ উৎস সিল্ক প্রোটিন থেকে সেরিন প্রথম পান।[৫] সিল্কের ল্যাটিন নাম, সেরিকাম এর জন্য সেরিন নামকরণ করা হয়েছে। সেরিনের কাঠামো ১৯০২ সালে প্রতিষ্ঠিত হয়েছিল।[৬][৭]
প্রস্তুতি ও বিক্রিয়া
[সম্পাদনা]হাইড্রক্সিমিথাইলট্রান্সফারেজ উৎসেচকের উপস্থিতিতে গ্লাইসিন ও মিথানল থেকে L-সেরিনের শিল্প উৎপাদন করা হয়।[৮]
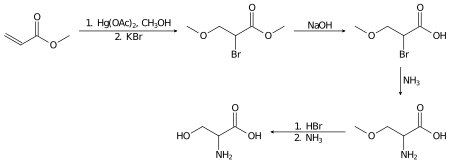
মিথাইল অ্যাক্রাইলেট থেকে সেরিনের রেসিমিক মিশ্রণ তৈরী করা যায়।[৯]
সেরিনের হাইড্রোজিনেশন সেরিনল উৎপন্ন করে:
HOCH2CH(NH2)CO2H + 2 H2 → HOCH2CH(NH2)CH2OH + 2 H2O
জীববৈজ্ঞানিক ক্রিয়া
[সম্পাদনা]বিপাক
[সম্পাদনা]
সেরিন বিপাকের ক্ষেত্রে গুরুত্বপূর্ণ কারণ এটি পিউরিন এবং পিরিমিডিনের জৈব সংশ্লেষণে অংশগ্রহণ করে। এটি গ্লাইসিন এবং সিস্টাইন সহ বেশ কয়েকটি অ্যামিনো অ্যাসিডের অগ্রদূত, সেইসাথে ব্যাকটেরিয়াতে ট্রিপটোফ্যান এরও। এটি স্ফিংগোলিপিড এবং ফোলেট সহ অসংখ্য অন্যান্য বিপাকজাত দ্রব্যের অগ্রদূত, যা জৈব সংশ্লেষণে এক-কার্বন খণ্ডের প্রধান দাতা।
সংকেত বহন
[সম্পাদনা]L-সেরিন থেকে সেরিন রেসিমেজ দ্বারা নিউরনে D-সেরিনসংশ্লেষিত হয়, এনএমডিএ রিসেপ্টরগুলিকে সমন্বিত করে নিউরোমোডুলেটর হিসাবে কাজ করে, যদি তারা গ্লুটামেটকেও আবদ্ধ করে তবে তাদের খুলতে সক্ষম করে। D-সেরিন হল ক্যানোনিকাল ডাইহেটেরোমেরিক এনএমডিএ রিসেপ্টরগুলির গ্লাইসিন সাইটের (NR1) একটি শক্তিশালী অ্যাগোনিস্ট (সহায়ক)। রিসেপ্টর খোলার জন্য, গ্লুটামেট এবং হয় গ্লাইসিন বা D-সেরিন অবশ্যই এটির সাথে আবদ্ধ হবে; উপরন্তু একটি ছিদ্র ব্লকার আবদ্ধ করা উচিত নয় (যেমন Mg2+ বা Zn2+)।[১০] প্রকৃতপক্ষে, D-সেরিন এনএমডিএআর-এর গ্লাইসিন সাইটে গ্লাইসিনের চেয়ে আরও শক্তিশালী অ্যাগোনিস্ট।[১১][১২] যাইহোক, D-সেরিনকে GluN3 সাবইউনিটে গ্লাইসিন বাইন্ডিং সাইটের মাধ্যমে টি-এনএমডিএ রিসেপ্টরগুলির প্রতিপক্ষ/বিপরীত সহ-অ্যাগোনিস্ট হিসাবে কাজ করতে দেখানো হয়েছে।[১৩][১৪]
লিগ্যান্ড
[সম্পাদনা]তুলনামূলকভাবে সম্প্রতি অবধি D-সেরিন কেবল ব্যাকটেরিয়ায় বিদ্যমান বলে মনে করা হয়েছিল; এটি ছিল দ্বিতীয় D অ্যামিনো অ্যাসিড যা মানুষের মধ্যে স্বাভাবিকভাবে বিদ্যমান ছিল, যা D-অ্যাস্পার্টেট আবিষ্কারের পরপরই মস্তিষ্কে একটি সংকেত অণু হিসাবে উপস্থিত ছিল। যদি মানুষের মধ্যে ডি অ্যামিনো অ্যাসিডগুলি শীঘ্রই আবিষ্কৃত হয়, তবে এনএমডিএ রিসেপ্টরের গ্লাইসিন সাইটটির পরিবর্তে D-সেরিন সাইট নামকরণ করা যেতে পারে।[১৫] কেন্দ্রীয় স্নায়ুতন্ত্র ছাড়াও, D-সেরিন পার্শ্ববর্তী কলা এবং তরুণাস্থি,[১৬] বৃক্ক[১৭], এবং কর্পাস ক্যাভারনোসামের[১৮] মতো অঙ্গগুলিতে একটি সংকেত ভূমিকা পালন করে।
স্বাদ সংবেদন
[সম্পাদনা]বিশুদ্ধ D-সেরিন হল একটি সাদা স্ফটিক দানা যার খুব ক্ষীণ মিষ্টি সুগন্ধ বর্তমান। D-সেরিন মাঝারি এবং উচ্চ ঘনত্বে অতিরিক্ত সামান্য টক স্বাদের সাথে মিষ্টি।[১৯]
উপকারিতা
[সম্পাদনা]শরীরে সেরিনের ঘাটতি দেখা দিলে সমস্যা দেখা দিতে পারে। সাধারণত তিনটি সমস্যা উল্লেখযোগ্য:
এই উৎসেচক ত্রুটিগুলি জন্মগত মাইক্রোসেফালি এব সাইকোমোটর প্রতিবন্ধকতার মতো গুরুতর স্নায়বিক লক্ষণগুলির দিকে পরিচালিত করে এবং উপরন্তু, ৩-ফসফোগ্লিসারেট ডিহাইড্রোজেনেজের ঘাটতি সহ রোগীদের মধ্যে খিঁচুনি হতে পারে। এই উপসর্গগুলি L-সেরিন দিয়ে চিকিৎসা করলে উহার পরিবর্তনশীল বিভিন্ন মাত্রায় সাড়া দেয়, কখনও কখনও গ্লাইসিনের সাথে মিলিত হয়ে চিকিৎসা করা হয়।[২০][২১] চিকিৎসার প্রতিক্রিয়া পরিবর্তনশীল এবং দীর্ঘমেয়াদী এবং কার্যকরী ফলাফল অজানা। এপিডেমিওলজি, জিনোটাইপ/ফেনোটাইপ পারস্পরিক সম্পর্ক এবং এই রোগগুলির ফলাফলের বোঝার উন্নতির জন্য একটি ভিত্তি প্রদান করার জন্য রোগীদের জীবনযাত্রার মানের উপর তাদের প্রভাব, সেইসাথে ডায়াগনস্টিক এবং থেরাপিউটিক কৌশলগুলি মূল্যায়নের জন্য একটি রোগীর রেজিস্ট্রি অবাণিজ্যিক সংস্থা ইন্টারন্যাশনাল ওয়ার্কিং গ্রুপ অন নিউরোট্রান্সমিটার রিলেটেড ডিসঅর্ডার (iNTD) প্রতিষ্ঠিত হয়েছিল।[২২]
সেরিনের জৈব সংশ্লেষণ সহ, এর পরিবহনেও ব্যাঘাত ঘটতে পারে। একটি উদাহরণ হল স্পাস্টিক টেট্রাপ্লেজিয়া, পাতলা কর্পাস ক্যালোসাম এবং প্রগতিশীল মাইক্রোসেফালি, মিউটেশনের কারণে সৃষ্ট একটি রোগ যা নিউট্রাল অ্যামিনো অ্যাসিড ট্রান্সপোর্টার এ-এর কাজকে প্রভাবিত করে।
একটি অ-অপরিহার্য অ্যামিনো অ্যাসিড হিসাবে L-সেরিনের শ্রেণিবিভাগকে শর্তসাপেক্ষ হিসাবে বিবেচনা করা হয়েছে, যেহেতু মানুষের মতো মেরুদণ্ডী প্রাণীরা সর্বদা সমগ্র জীবনকাল ধরে সর্বোত্তম পরিমাণে সংশ্লেষ করতে পারে না।[২৩] অ্যামিওট্রফিক ল্যাটারাল স্ক্লেরোসিস (ALS), রোগীদের (ClinicalTrials.gov শনাক্তকারী: NCT01835782),[২৪][২৫] এফডিএ-অনুমোদিত মানব পর্যায় I ক্লিনিকাল ট্রায়ালে L-সেরিনের নিরাপত্তা প্রদর্শন করা হয়েছে, তবে ALS উপসর্গগুলির চিকিৎসা এখনও হয়নি। একটি ২০১১ মেটা-বিশ্লেষণে সিজোফ্রেনিয়ার নেতিবাচক এবং মোট উপসর্গগুলির জন্য অ্যাডজাঙ্কটিভ সারকোসিনের মাঝারি প্রভাবের আকার পাওয়া গেছে।[২৬] এছাড়াও প্রমাণ আছে যে L-সেরিন ডায়াবেটিসে একটি থেরাপিউটিক ভূমিকা অর্জন করতে পারে।[২৭]
সিজোফ্রেনিয়ার সম্ভাব্য চিকিৎসা হিসেবে ইঁদুরদের মধ্যে D-সেরিন অধ্যয়ন করা হচ্ছে।[২৮] সম্ভাব্য আলঝেইমার রোগীদের সেরিব্রোস্পাইনাল ফ্লুইডে এর তুলনামূলক উচ্চ ঘনত্বের কারণে D-সেরিনকে প্রাথমিকভাবে এই রোগ নির্ণয়ের জন্য একটি সম্ভাব্য বায়োমার্কার হিসাবেও বর্ণনা করা হয়েছে।[২৯] D-সেরিন, যা মস্তিষ্কে তৈরি করা হয়, টি-এনএমডিএ রিসেপ্টরগুলির প্রতিপক্ষ/বিপরীত সহ-অ্যাগোনিস্ট হিসাবে কাজ করতে দেখা গেছে যা টেম্পোরাল লোব মৃগী রোগের একটি প্রাণীর মডেলে নিউরন ক্ষয় হ্রাস করে।[৩০]
D-সেরিনকে শ্রবণশক্তি হ্রাস এবং টিনিটাসের মতো সংবেদনশীল শ্রবণজনিত ব্যাধিগুলির জন্য একটি সম্ভাব্য চিকিৎসা হিসাবে তাত্ত্বিক করা হয়েছে।[৩১]
তথ্যসূত্র
[সম্পাদনা]- ↑ Dawson, R.M.C., et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ↑ Weast, Robert C., সম্পাদক (১৯৮১)। CRC Handbook of Chemistry and Physics (62nd সংস্করণ)। Boca Raton, FL: CRC Press। পৃষ্ঠা C-512। আইএসবিএন 0-8493-0462-8।
- ↑ "Nomenclature and Symbolism for Amino Acids and Peptides"। IUPAC-IUB Joint Commission on Biochemical Nomenclature। ১৯৮৩। ৯ অক্টোবর ২০০৮ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ৫ মার্চ ২০১৮।
- ↑ "Nomenclature and symbolism for amino acids and peptides (IUPAC-IUB Recommendations 1983)", Pure Appl. Chem., 56 (5): 595–624, ১৯৮৪, ডিওআই:10.1351/pac198456050595.
- ↑ Cramer, Emil (১৮৬৫)। "Ueber die Bestandtheile der Seide" [On the constituents of silk]। Journal für praktische Chemie (German ভাষায়)। 96: 76–98। Serine is named on p. 93: "Ich werde den in Frage stehenden Körper unter dem Namen Serin beschreiben." (I will describe the body [i.e., substance] in question by the name "serine".)
- ↑ Fischer, Emil; Leuchs, Hermann (১৯০২)। "Synthese des Serins, der l-Glucosaminsäure und anderer Oxyaminosäuren" [Synthesis of serine, of l-glucosaminic acid, and other oxyamino acids]। Berichte der Deutschen Chemischen Gesellschaft (জার্মান ভাষায়)। 35 (3): 3787–3805। ডিওআই:10.1002/cber.190203503213।
- ↑ "Serine"। The Columbia Encyclopedia 6th ed.। encyclopedia.com। সংগ্রহের তারিখ ২২ অক্টোবর ২০১২।
- ↑ Karlheinz Drauz, Ian Grayson, Axel Kleemann, Hans-Peter Krimmer, Wolfgang Leuchtenberger, Christoph Weckbecker (২০০৬)। উলম্যানস এনসাইক্লোপিডিয়া অব ইন্ডাস্ট্রিয়াল কেমিস্ট্রি। ওয়েইনহেইম: উইলি-ভিসিএইচ। ডিওআই:10.1002/14356007.a02_057.pub2।
- ↑ Carter, Herbert E.; West, Harold D. (১৯৪০)। "dl-Serine"। Org. Synth.। 20: 81। ডিওআই:10.15227/orgsyn.020.0081।
- ↑ Liu Y, Hill RH, Arhem P, von Euler G (২০০১)। "NMDA and glycine regulate the affinity of the Mg2+-block site in NR1-1a/NR2A NMDA receptor channels expressed in Xenopus oocytes"। Life Sciences। 68 (16): 1817–1826। ডিওআই:10.1016/S0024-3205(01)00975-4। পিএমআইডি 11292060।
- ↑ MacKay, Mary-Anne B.; Kravtsenyuk, Maryana; Thomas, Rejish; Mitchell, Nicholas D.; Dursun, Serdar M.; Baker, Glen B. (৬ ফেব্রুয়ারি ২০১৯)। "D-Serine: Potential Therapeutic Agent and/or Biomarker in Schizophrenia and Depression?"। Frontiers in Psychiatry। 10: 25। আইএসএসএন 1664-0640। ডিওআই:10.3389/fpsyt.2019.00025
 । পিএমআইডি 30787885। পিএমসি 6372501
। পিএমআইডি 30787885। পিএমসি 6372501  ।
। D-Serine is more potent than glycine as a coagonist at the NMDA receptor, has a regional distribution in the brain that is similar to that of NMDA receptors and appears to be more closely associated with synaptic NMDA receptors than glycine (which is more closely associated with non-synaptic NMDA receptors).
- ↑ Wolosker, Herman; Balu, Darrick T. (৯ জুন ২০২০)। "D-Serine as the gatekeeper of NMDA receptor activity: implications for the pharmacologic management of anxiety disorders"। Translational Psychiatry। 10 (1): 184। আইএসএসএন 2158-3188। ডিওআই:10.1038/s41398-020-00870-x। পিএমআইডি 32518273
|pmid=এর মান পরীক্ষা করুন (সাহায্য)। পিএমসি 7283225
|pmc=এর মান পরীক্ষা করুন (সাহায্য)।D-Serine is functionally a more potent activator of synaptic NMDARs than glycine, and mounting evidence suggests that it serves as the major NMDAR co-agonist in limbic brain regions implicated in neuropsychiatric disorders.
- ↑ Pilli, J.; Kumar, S. S. (২০১২-১০-১১)। "Triheteromeric N-methyl-D-aspartate receptors differentiate synaptic inputs onto pyramidal neurons in somatosensory cortex: involvement of the GluN3A subunit"। Neuroscience। 222: 75–88। আইএসএসএন 1873-7544। এসটুসিআইডি 23158971। ডিওআই:10.1016/j.neuroscience.2012.07.020। পিএমআইডি 22814002।
- ↑ Beesley, Stephen; Kumar, Sanjay S. (২০২৩-১১-০১)। "The t-N-methyl-d-aspartate receptor: Making the case for d-Serine to be considered its inverse co-agonist"। Neuropharmacology। 238: 109654। আইএসএসএন 1873-7064। ডিওআই:10.1016/j.neuropharm.2023.109654
 । পিএমআইডি 37437688
। পিএমআইডি 37437688 |pmid=এর মান পরীক্ষা করুন (সাহায্য)। - ↑ Mothet JP, Parent AT, Wolosker H, Brady RO, Linden DJ, Ferris CD, Rogawski MA, Snyder SH (এপ্রিল ২০০০)। "D-Serine is an endogenous ligand for the glycine site of the N-methyl-D-aspartate receptor"। Proceedings of the National Academy of Sciences of the United States of America। 97 (9): 4926–4931। ডিওআই:10.1073/pnas.97.9.4926
 । পিএমআইডি 10781100। পিএমসি 18334
। পিএমআইডি 10781100। পিএমসি 18334  । বিবকোড:2000PNAS...97.4926M।
। বিবকোড:2000PNAS...97.4926M।
- ↑ Takarada T, Hinoi E, Takahata Y, Yoneda Y (মে ২০০৮)। "Serine racemase suppresses chondrogenic differentiation in cartilage in a Sox9-dependent manner"। Journal of Cellular Physiology। 215 (2): 320–328। এসটুসিআইডি 45669104। ডিওআই:10.1002/jcp.21310। পিএমআইডি 17929246।
- ↑ Ma MC, Huang HS, Chen YS, Lee SH (নভে ২০০৮)। "Mechanosensitive N-methyl-D-aspartate receptors contribute to sensory activation in the rat renal pelvis"। Hypertension। 52 (5): 938–944। ডিওআই:10.1161/HYPERTENSIONAHA.108.114116
 । পিএমআইডি 18809793।
। পিএমআইডি 18809793।
- ↑ Ghasemi M, Rezania F, Lewin J, Moore KP, Mani AR (জুন ২০১০)। "D-Serine modulates neurogenic relaxation in rat corpus cavernosum"। Biochemical Pharmacology। 79 (12): 1791–1796। ডিওআই:10.1016/j.bcp.2010.02.007। পিএমআইডি 20170643।
- ↑ Kawai M, Sekine-Hayakawa Y, Okiyama A, Ninomiya Y (ডিসে ২০১২)। "Gustatory sensation of L- and D-amino acids in humans"। Amino Acids। 43 (6): 2349–2358। এসটুসিআইডি 17671611। ডিওআই:10.1007/s00726-012-1315-x। পিএমআইডি 22588481।
- ↑ de Koning TJ (এপ্রিল ২০০৬)। "Treatment with amino acids in serine deficiency disorders"। Journal of Inherited Metabolic Disease। 29 (2): 347–351। এসটুসিআইডি 25013468। ডিওআই:10.1007/s10545-006-0269-0। পিএমআইডি 16763900।
- ↑ Tabatabaie L; Klomp LW; Berger R; de Koning TJ (মার্চ ২০১০)। "L-Serine synthesis in the central nervous system: a review on serine deficiency disorders"। Mol Genet Metab। 99 (3): 256–262। ডিওআই:10.1016/j.ymgme.2009.10.012। পিএমআইডি 19963421।
- ↑ "Patient registry"।
- ↑ Metcalf, J. S.; Dunlop, R. A.; Powell, J. T.; Banack, S. A.; Cox, P. A. (২০১৭)। "L-Serine: a Naturally-Occurring Amino Acid with Therapeutic Potential"। Neurotoxicity Research। 33 (1): 213–221। আইএসএসএন 1029-8428। এসটুসিআইডি 20271849। ডিওআই:10.1007/s12640-017-9814-x। পিএমআইডি 28929385।
- ↑ Dunlop RA, Cox PA, Banack SA, Rodgers KJ (২০১৩)। "The non-protein amino acid BMAA is misincorporated into human proteins in place of L-serine causing protein misfolding and aggregation"। PLOS ONE। 8 (9): e75376। ডিওআই:10.1371/journal.pone.0075376
 । পিএমআইডি 24086518। পিএমসি 3783393
। পিএমআইডি 24086518। পিএমসি 3783393  । বিবকোড:2013PLoSO...875376D।
। বিবকোড:2013PLoSO...875376D।
- ↑ Levine, Todd D.; Miller, Robert G.; Bradley, Walter G.; Moore, Dan H.; Saperstein, David S.; Flynn, Lynne E.; Katz, Jonathan S.; Forshew, Dallas A.; Metcalf, James S.; Banack, Sandra A.; Cox, Paul A. (২০১৭-০১-০২)। "Phase I clinical trial of safety of L-serine for ALS patients"। Amyotrophic Lateral Sclerosis and Frontotemporal Degeneration (ইংরেজি ভাষায়)। 18 (1–2): 107–111। আইএসএসএন 2167-8421। এসটুসিআইডি 4584977। ডিওআই:10.1080/21678421.2016.1221971
 । পিএমআইডি 27589995।
। পিএমআইডি 27589995।
- ↑ Singh SP, Singh V (অক্টো ২০১১)। "Meta-analysis of the efficacy of adjunctive NMDA receptor modulators in chronic schizophrenia"। CNS Drugs। 25 (10): 859–885। এসটুসিআইডি 207299820। ডিওআই:10.2165/11586650-000000000-00000। পিএমআইডি 21936588।
- ↑ Holm, Laurits J.; Buschard, Karsten (২০১৯)। "L-serine: a neglected amino acid with a potential therapeutic role in diabetes"। APMIS। 127 (10): 655–659। আইএসএসএন 0903-4641। ডিওআই:10.1111/apm.12987
 । পিএমআইডি 31344283। পিএমসি 6851881
। পিএমআইডি 31344283। পিএমসি 6851881  ।
।
- ↑ Balu DT, Li Y, Puhl MD, Benneyworth MA, Basu AC, Takagi S, Bolshakov VY, Coyle JT (জুন ২০১৩)। "Multiple risk pathways for schizophrenia converge in serine racemase knockout mice, a mouse model of NMDA receptor hypofunction"। Proceedings of the National Academy of Sciences of the United States of America। 110 (26): E2400–E2409। ডিওআই:10.1073/pnas.1304308110
 । পিএমআইডি 23729812। পিএমসি 3696825
। পিএমআইডি 23729812। পিএমসি 3696825  । বিবকোড:2013PNAS..110E2400B।
। বিবকোড:2013PNAS..110E2400B।
- ↑ Madeira C, Lourenco MV, Vargas-Lopes C, Suemoto CK, Brandão CO, Reis T, Leite RE, Laks J, Jacob-Filho W, Pasqualucci CA, Grinberg LT, Ferreira ST, Panizzutti R (মে ৫, ২০১৫)। "D-Serine levels in Alzheimer's disease: implications for novel biomarker development"। Translational Psychiatry। 5 (5): e561। ডিওআই:10.1038/tp.2015.52। পিএমআইডি 25942042। পিএমসি 4471283
 ।
।
- ↑ Beesley, Stephen; Sullenberger, Thomas; Crotty, Kathryn; Ailani, Roshan; D'Orio, Cameron; Evans, Kimberly; Ogunkunle, Emmanuel O.; Roper, Michael G.; Kumar, Sanjay S. (২০২০-১০-০২)। "D-serine mitigates cell loss associated with temporal lobe epilepsy"। Nature Communications। 11 (1): 4966। আইএসএসএন 2041-1723। ডিওআই:10.1038/s41467-020-18757-2। পিএমআইডি 33009404
|pmid=এর মান পরীক্ষা করুন (সাহায্য)। পিএমসি 7532172
|pmc=এর মান পরীক্ষা করুন (সাহায্য)। বিবকোড:2020NatCo..11.4966B। - ↑ Wang, Jing; Serratrice, Nicolas; Lee, Cindy J.; François, Florence; Sweedler, Jonathan V.; Puel, Jean-Luc; Mothet, Jean-Pierre; Ruel, Jérôme (১৭ ডিসেম্বর ২০২১)। "Physiopathological Relevance of D-Serine in the Mammalian Cochlea"। Frontiers in Cellular Neuroscience। Frontiers Media SA। 15: 733004। আইএসএসএন 1662-5102। ডিওআই:10.3389/fncel.2021.733004
 । পিএমআইডি 34975405
। পিএমআইডি 34975405 |pmid=এর মান পরীক্ষা করুন (সাহায্য)। পিএমসি 8718999
|pmc=এর মান পরীক্ষা করুন (সাহায্য)।
বহিঃসংযোগ
[সম্পাদনা]
| ২০টি অ্যামিনো অ্যাসিড প্রোটিন তৈরীতে ব্যবহৃত | ||
|---|---|---|
| অ্যালানিন (dp) | আর্জিনিন (dp) | অ্যাস্পারাজিন (dp) | অ্যাস্পার্টিক অ্যাসিড (dp) | সিস্টিন (dp) | গ্লুটামিক অ্যাসিড (dp) | গ্লুটামিন (dp) | গ্লাইসিন (dp) | হিস্টিডিন (dp) | আইসোলিউসিন (dp) | লিউসিন (dp) | লাইসিন (dp) | মিথায়োনিন (dp) | ফেনাইল অ্যালানিন (dp) | প্রোলিন (dp) | সেরিন (dp) | থ্রিয়োনিন (dp) | ট্রিপ্টোফ্যান (dp) | টাইরোসিন (dp) | ভ্যালিন (dp) | ||
| ←Peptides | Major families of biochemicals | Nucleic acids→ |