Hemeprotein

Hemeprotein ili hemski protein, je protein koji sadrži hemsku prostetsku grupu. Oni su veoma velika klasa metaloproteina. Hem grupa daje funkcionalnost, koja može uključivati prenošenje kisika, redukciju kisika, prijenos elektrona i druge procese. Hem je vezan za protein ili kovalentno ili nekovalentno ili oboje.[1]
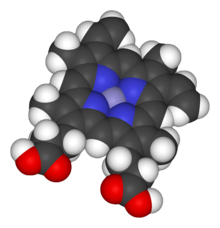
Hem se sastoji od kationa gvožđa vezanog u centru konjugovane baze porfirina, kao i drugih liganada vezanih za "aksijalna mjesta" gvožđa. Porfirinski prsten je planarni dijaionski, tetradentatni ligand. Gvožđe je obično Fe2+ ili Fe3+. Jedan ili dva liganda vezani su na aksijalnim mjestima. Porfirinski prsten ima četiri atoma dušika koji se vežu za gvožđe, ostavljajući dvije druge koordinacijske pozicije gvožđa na raspolaganju za vezivanje za histidin proteina i dvovalentni atom.[1]
Hemeproteini su vjerovatno evoluirali da inkorporiraju atom gvožđa sadržan u protoporfirinskom IX prstenu hema u proteine. Kako hemeproteine čini osjetljivima na molekule koji mogu vezati dvovalentno gvožđe, ova strategija se održavala tokom evolucije jer ima ključne fiziološke funkcije. Kisik (O2), dušik-oksid (NO), ugljik-monoksid (CO) i vodik-sulfid (H2S) vezuju se za atom gvožđa u proteinima hema. Jednom vezani za prostetske hemske grupe, ove molekule mogu modulirati aktivnost/funkciju tih hemeproteina, omogućavajući transdukciju signala. Stoga, kada se proizvode u biološkim sistemima (ćelijama), ove plinovite molekule nazivaju se plinotransmiterima.
Zbog svojih raznolikih bioloških funkcija i široko rasprostranjenog izobilja, hemeproteini su među najistraženijim biomolekulama.[2] Podaci o strukturi i funkciji proteina hema agregirani su u The Heme Protein Database (HPD), sekundarnu bazu podataka proteinsku bazu podataka.[3]
Uloge
[uredi | uredi izvor]Hemeproteini imaju različite biološke funkcije uključujući transport kisika, koji se završava preko hemeproteina uključujući hemoglobin, mioglobin, neuroglobin, citoglobin i leghemoglobin.[4]
Neki hemeproteini – citohrom P450, citohrom c-oksidaza, ligninaza, katalaza i peroksidaza – su enzimi. Često aktiviraju O2 za oksidaciju ili hidroksilaciju.
Hemeproteini također omogućavaju transfer elektrona jer čine dio lanca transporta elektrona. Ciktohrom a, citohrom b i citohrom c imaju takve funkcije prijenosa elektrona. Senzorni sistem se također oslanja na neke hemeproteine uključujući FixL, senzor kisika, CooA, senzor ugljik-monoksida i rastvorljivu gvanilil-ciklazu.
Hemoglobin i mioglobin
[uredi | uredi izvor]Hemoglobin i mioglobin su primjeri hemeproteina koji transportiraju i skladište kisik kod sisara. Hemoglobin je kvarternarni protein koji se javlja u crvenim krvnim zrncima, dok je mioglobin tercijarni protein koji se nalazi u mišićnim ćelijama sisara. Iako se mogu razlikovati po lokaciji i veličini, njihova funkcija je slična. Budući da su hemeproteini, oba sadrže hemski prostetsku grupu.
His-F8 mioglobina, također poznat kao proksimalni histidin, kovalentno je vezan za 5. koordinacijski položaj gvožđa. Kisik stupa u interakciju sa distalnim His putem vodikove veze, a ne kovalentne. On se vezuje za 6. koordinacionu poziciju gvožđa, His-E7 mioglobina se vezuje za kisik koji je sada kovalentno vezan za gvožđe. Isto važi i za hemoglobin; međutim, budući da je protein sa četiri podjedinice, hemoglobin sadrži ukupno četiri hemske jedinice, omogućavajući ukupno četiri molekule kisika da se vežu za protein.
Mioglobin i hemoglobin su globulasti proteini koji služe za vezivanje i isporuku kisika pomoću prostetske grupe. Ovi globini dramatično poboljšavaju koncentraciju molekulskog kisika koji se može prenositi u biološkim tečnostima kičmenjaka i nekih beskičmenjaka.
Razlike se javljaju u vezivanju liganda i alosternnoj regulaciji.
Mioglobin
[uredi | uredi izvor]Mioglobin se nalazi u mišićnim ćelijama kičmenjaka. Mišićne ćelije, kada se pokrenu, mogu brzo zahtijevati veliku količinu kisika za disanje zbog svojih energetskih potreba. Stoga mišićne ćelije koriste mioglobin da ubrzaju difuziju kisika i djeluju kao lokalizirane rezerve kisika za vrijeme intenzivnog disanja. Mioglobin također skladišti potrebnu količinu kisika i čini ga dostupnim za mitohondrije mišićnih ćelija.
Hemoglobin
[uredi | uredi izvor]U kičmenjaka, hemoglobin se nalazi u citosolu crvenih krvnih zrnaca. Hemoglobin se ponekad naziva i protein za transport kisika, kako bi se suprotstavio mioglobinu, koji je stacionaran.
Kod kičmenjaka, kisik se u organizam unosi tkivima pluća i prenosi do crvenih krvnih zrnaca u krvotoku. Kisik se zatim distribuira u sva tkiva u tijelu i prenosi iz crvenih krvnih zrnaca do ćelija koje dišu. Hemoglobin zatim pokupi ugljik-dioksid da bi se vratio u pluća. Dakle, hemoglobin veže i oslobađa kisik i ugljik-dioksid u odgovarajuća tkiva, služeći za isporuku kisika potrebnog za ćelijski metabolizam i uklanjanje rezultirajućeg otpadnog proizvoda, CO2.
Citohrom c-oksidaza
[uredi | uredi izvor]Citokrom c-oksidaza je enzim ugrađen u unutrašnju membranu mitohondrija. Njegova glavna funkcija je da oksidira protein citokrom c. Citokrom c-oksidaza sadrži nekoliko metalnih aktivnih mjesta.
Dizajnirani hemski proteini
[uredi | uredi izvor]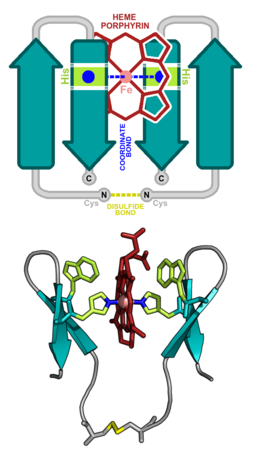
Zbog različitih funkcija molekula hema: kao transportera elektrona, prijenosnika kisika i kao kofaktora enzima, proteini koji vezuju hem stalno privlače pažnju dizajnera proteina. Početni pokušaji dizajna bili su fokusirani na proteine koji vežu α-heliksni hem, dijelom zbog relativne jednostavnosti dizajniranja spiralnih snopova koji se sami sklapaju. Vezna mjesta za hem su dizajnirana unutar inter-heliksnih hidrofobnih žljebova. Primjeri takvih dizajna uključuju:
- Helihrom[6][7]
- Globin-1[8]
- Cy-AA-EK[9]
- Peptidi IIa/IId[10]
- α2[11]
- Transmembranski heliksni dizajn[12][13][14]
Kasniji pokušaji dizajna usredotočili su se na stvaranje funkcionalnih spiralnih snopova koji vežu hem, kao što su:
- Oksidoreduktaze [15][16]
- Peroksidaze[17][18]
- Elektronski transportni proteini[19]
- Kisični transportni proteini[20]
- Photosensitive proteins[15]
Tehnike dizajna su sazrele do te mjere da je sada moguće generirati čitave biblioteke spiralnih proteina koji vezuju hem.[21]
Nedavni pokušaji dizajna fokusirani su na stvaranje proteina koji vezuju sve beta-hem, čija je nova topologija vrlo rijetka u prirodi. Takvi dizajni uključuju:
Reference
[uredi | uredi izvor]- ^ a b Nelson DL, Cox MN (2000). Lehninger, Principles of Biochemistry (3rd izd.). New Yorkm: Worth Publishing. ISBN 1-57259-153-6.
- ^ Reedy CJ, Elvekrog MM, Gibney BR (januar 2008). "Development of a heme protein structure-electrochemical function database". Nucleic Acids Research. 36 (Database issue): D307–D313. doi:10.1093/nar/gkm814. PMC 2238922. PMID 17933771.
- ^ Gibney BR. "Heme Protein Database". Brooklyn, NY: Brooklyn College.
- ^ Lippard J, Berg JM (1994). Principles of Bioinorganic Chemistry. Mill Valley, CA: University Science Books. ISBN 0-935702-73-3.
- ^ a b Nagarajan D, Sukumaran S, Deka G, Krishnamurthy K, Atreya HS, Chandra N (juni 2018). "Design of a heme-binding peptide motif adopting a β-hairpin conformation". The Journal of Biological Chemistry (jezik: English). 293 (24): 9412–9422. doi:10.1074/jbc.RA118.001768. PMC 6005436. PMID 29695501.CS1 održavanje: nepoznati jezik (link)
- ^ Sasaki T, Kaiser ET (1. 1. 1989). "Helichrome: synthesis and enzymic activity of a designed hemeprotein". Journal of the American Chemical Society (jezik: engleski). 111 (1): 380–381. doi:10.1021/ja00183a065. ISSN 0002-7863.
- ^ Sasaki T, Kaiser ET (januar 1990). "Synthesis and structural stability of helichrome as an artificial hemeproteins". Biopolymers. 29 (1): 79–88. doi:10.1002/bip.360290112. PMID 2328295. S2CID 35536899.
- ^ Isogai Y, Ota M, Fujisawa T, Izuno H, Mukai M, Nakamura H, et al. (juni 1999). "Design and synthesis of a globin fold". Biochemistry. 38 (23): 7431–7443. doi:10.1021/bi983006y. PMID 10360940.
- ^ Rosenblatt MM, Wang J, Suslick KS (novembar 2003). "De novo designed cyclic-peptide heme complexes". Proceedings of the National Academy of Sciences of the United States of America. 100 (23): 13140–13145. Bibcode:2003PNAS..10013140R. doi:10.1073/pnas.2231273100. PMC 263730. PMID 14595023.
- ^ Robertson DE, Farid RS, Moser CC, Urbauer JL, Mulholland SE, Pidikiti R, et al. (mart 1994). "Design and synthesis of multi-haem proteins". Nature. 368 (6470): 425–432. Bibcode:1994Natur.368..425R. doi:10.1038/368425a0. PMID 8133888. S2CID 4360174.
- ^ Choma CT, Lear JD, Nelson MJ, Dutton PL, Robertson DE, DeGrado WF (1. 2. 1994). "Design of a heme-binding four-helix bundle". Journal of the American Chemical Society (jezik: engleski). 116 (3): 856–865. doi:10.1021/ja00082a005. ISSN 0002-7863.
- ^ Discher BM, Noy D, Strzalka J, Ye S, Moser CC, Lear JD, et al. (septembar 2005). "Design of amphiphilic protein maquettes: controlling assembly, membrane insertion, and cofactor interactions". Biochemistry. 44 (37): 12329–12343. doi:10.1021/bi050695m. PMC 2574520. PMID 16156646.
- ^ Mahajan M, Bhattacharjya S (juni 2014). "Designed di-heme binding helical transmembrane protein". ChemBioChem. 15 (9): 1257–1262. doi:10.1002/cbic.201402142. PMID 24829076. S2CID 20982919.
- ^ Korendovych IV, Senes A, Kim YH, Lear JD, Fry HC, Therien MJ, et al. (novembar 2010). "De novo design and molecular assembly of a transmembrane diporphyrin-binding protein complex". Journal of the American Chemical Society. 132 (44): 15516–15518. doi:10.1021/ja107487b. PMC 3016712. PMID 20945900.
- ^ a b Farid TA, Kodali G, Solomon LA, Lichtenstein BR, Sheehan MM, Fry BA, et al. (decembar 2013). "Elementary tetrahelical protein design for diverse oxidoreductase functions". Nature Chemical Biology. 9 (12): 826–833. doi:10.1038/nchembio.1362. PMC 4034760. PMID 24121554.
- ^ Huang SS, Koder RL, Lewis M, Wand AJ, Dutton PL (april 2004). "The HP-1 maquette: from an apoprotein structure to a structured hemoprotein designed to promote redox-coupled proton exchange". Proceedings of the National Academy of Sciences of the United States of America. 101 (15): 5536–5541. doi:10.1073/pnas.0306676101. PMC 397418. PMID 15056758.
- ^ Faiella M, Maglio O, Nastri F, Lombardi A, Lista L, Hagen WR, Pavone V (decembar 2012). "De novo design, synthesis and characterisation of MP3, a new catalytic four-helix bundle hemeprotein". Chemistry. 18 (50): 15960–15971. doi:10.1002/chem.201201404. PMID 23150230.
- ^ Cherry JR, Lamsa MH, Schneider P, Vind J, Svendsen A, Jones A, Pedersen AH (april 1999). "Directed evolution of a fungal peroxidase". Nature Biotechnology. 17 (4): 379–384. doi:10.1038/7939. PMID 10207888. S2CID 41233353.
- ^ Anderson JL, Armstrong CT, Kodali G, Lichtenstein BR, Watkins DW, Mancini JA, et al. (februar 2014). "Constructing a man-made c-type cytochrome maquette in vivo: electron transfer, oxygen transport and conversion to a photoactive light harvesting maquette". Chemical Science. 5 (2): 507–514. doi:10.1039/C3SC52019F. PMC 3952003. PMID 24634717.
- ^ Koder RL, Anderson JL, Solomon LA, Reddy KS, Moser CC, Dutton PL (mart 2009). "Design and engineering of an O(2) transport protein". Nature. 458 (7236): 305–309. Bibcode:2009Natur.458..305K. doi:10.1038/nature07841. PMC 3539743. PMID 19295603.
- ^ Moffet DA, Foley J, Hecht MH (septembar 2003). "Midpoint reduction potentials and heme binding stoichiometries of de novo proteins from designed combinatorial libraries". Biophysical Chemistry. Walter Kauzmann`s 85th Birthday. 105 (2–3): 231–239. doi:10.1016/S0301-4622(03)00072-3. PMID 14499895.
- ^ Mahajan M, Bhattacharjya S (juni 2013). "β-Hairpin peptides: heme binding, catalysis, and structure in detergent micelles". Angewandte Chemie. 52 (25): 6430–6434. doi:10.1002/anie.201300241. PMID 23640811.
- ^ D'Souza A, Wu X, Yeow EK, Bhattacharjya S (maj 2017). "Designed Heme-Cage β-Sheet Miniproteins". Angewandte Chemie. 56 (21): 5904–5908. doi:10.1002/anie.201702472. PMID 28440962.
- ^ D'Souza A, Mahajan M, Bhattacharjya S (april 2016). "Designed multi-stranded heme binding β-sheet peptides in membrane". Chemical Science. 7 (4): 2563–2571. doi:10.1039/C5SC04108B. PMC 5477022. PMID 28660027.
Vanjski linkovi
[uredi | uredi izvor]- Heme Protein Database
- Hemeproteins na US National Library of Medicine Medical Subject Headings (MeSH)