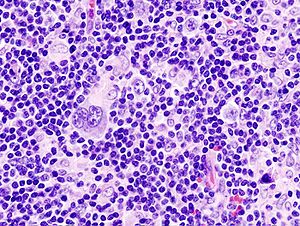
Limfoma de Hodgkin
 | |
| Tipus | limfoma |
|---|---|
| Epònim | Thomas Hodgkin |
| Especialitat | hematologia |
| Clínica-tractament | |
Medicació | |
| Patogènesi | |
| Associació genètica | GATA3 (en) |
| Causat per | infecció pel virus d'Epstein-Barr |
| Classificació | |
| CIM-11 | 2B30 |
| CIM-10 | C81.9 i C81 |
| CIM-9 | 201.0, 201.2, 201.1, 201 i 201.9 |
| CIM-O | 9650/3, 9667/3 i 965-966 |
| CIAP | B72 |
| Recursos externs | |
| Enciclopèdia Catalana | 0032786 |
| OMIM | 236000, 300221 i 400021 |
| DiseasesDB | 5973 |
| MedlinePlus | 000580 |
| eMedicine | 201886 |
| Patient UK | hodgkins-lymphoma-pro |
| MeSH | D006689 |
| Orphanet | 98293 |
| UMLS CUI | C0019829 |
| DOID | DOID:8567 |

El limfoma de Hodgkin, també conegut com a malaltia de Hodgkin, és una mena de limfoma, un càncer que s'origina a un tipus específic de glòbuls blancs anomenat limfòcits, en què cèl·lules gegants (anomenades de Reed-Sternberg) s'acumulen en els ganglis limfàtics de la persona afectada.[1][2]
Aquest teixits formen part del sistema immunitari i del sistema productor de sang del cos. Aquest tipus de càncer produeix un engrandiment del teixit limfàtic, la qual cosa pot ocasionar pressió sobre estructures importants. La forma principal de propagació de la malaltia de Hodgkin és entre els vasos limfàtics propers. Menys comunament pot estendre's a gairebé qualsevol altra part del cos, incloent-hi el fetge i els pulmons. Els símptomes inclouen febre, sudoració nocturna, i pèrdua de pes. També apareix fatiga i pruïja.[1][3]
Hi ha dos grans tipus de limfoma de Hodgkin: l'anomenat clàssic, el majoritari; i el limfoma de Hodgkin amb limfòcits nodulars predominants, que presenta unes característiques diferents.[4] Aproximadament la meitat dels casos de limfoma de Hodgkin es relacionen amb la infecció amb el virus d'Epstein-Barr (VEB), que generalment causen la forma clàssica.[5][6] Altres factors de risc inclouen casos familiars i ser seropositiu pel VIH.[1][5] El diagnòstic s'assoleix amb la identificació les cèl·lules de Reed-Sternberg en una biòpsia d'un gangli limfàtic afectat.[1]
El limfoma de Hodgkin es pot tractar amb quimioteràpia, radioteràpia, i trasplantament de medul·la òssia.[7] El tipus de tractament sovint depén de com d'avançat es trobe el càncer i si presenta característiques favorables o no.[7] En tots els estadis sovint és possible la curació.[8] Als Estats Units, el 88% dels pacients diagnosticats amb limfoma de Hodgkin tenen una supervivència superior als cinc anys.[4] Per als menors de 20 anys, la taxa de supervivència és del 97%.[9] A Catalunya, té una taxa de supervivència a cinc anys per a homes al voltant del 85% i per a dones al voltant del 87%.[10] No obstant això, la radiació i la quimioteràpia augmenten el risc de patir un altre càncer, malaltia cardiovascular, o malaltia pulmonar durant les següents dècades.[8]
Al 2015, al voltant de 574.000 persones arreu del món patien limfoma de Hodgkin, i d'elles 23.900 (un 4,2%) van morir.[11][12] Als Estats Units, un 0,2% de la població s'ha trobat afectada en algun moment de la seua vida.[4] És un tipus de limfoma maligne, encara que molt menys freqüent que el limfoma no hodgkinià. L'edat més comuna de diagnòstic és entre els 20 i 40 anys.[4] Rep el seu nom del metge britànic Thomas Hodgkin, el primer en descriure la condició en 1832.[8][13]
Símptomes
[modifica]Aquesta mena de limfoma es pot presentar amb aquests símptomes:[14][15]
- Limfadenopatia: el símptoma més freqüent és el creixement no dolorós d'un o diversos ganglis limfàtics. Els ganglis acostumen a tindre un tacte dur i inflamat quan s'examinen. Els ganglis del coll, aixelles i engonals són els més involucrats (aproximadament un 80-90% dels casos). Els ganglis del pit es troben afectats sovint, i es poden observar en una radiografia de tòrax.
- Símptomes sistèmics: un terç de les persones amb limfoma de Hodgkin poden presentar els següents símptomes, coneguts com a símptomes B:
- Pruïja
- Hiperhidrosi nocturna
- Pèrdua de pes sense explicar d'almenys un 10% de la massa corporal total de la persona en sis mesos o menys
- Febrícula
- Fatiga.
- Esplenomegàlia: sovint podem trobar l'engrandiment de la melsa en el limfoma de Hodgkin. Aquest creixement, però, rara volta és massiu, i la mida de la melsa pot fluctuar durant el tractament.
- Hepatomegàlia: encara que infreqüent, es pot trobar l'engrandiment del fetge.
- Hepatosplenomegàlia: a vegades es troba hepatomegàlia i esplenomegàlia en un mateix individu.
- Dolor després de consumir alcohol: clàssicament, els ganglis afectats fan mal després de consumir alcohol, però aquest fenomen és molt rar,[16] ocorrent en només d'un dos a tres per cent de persones amb limfoma de Hodgkin,[17] per això es considera una troballa amb baixa sensibilitat. D'altra banda, té un valor predictiu positiu prou alt en ser considerar un signe patognomònic del limfoma de Hodgkin. El dolor típicament apareix en pocs minuts d'ingerir alcohol, i se sent als voltants dels ganglis limfàtics afectats. Aquest dolor s'ha descrit com a agut i punxant o sord i general.
- Mal d'esquena: un mal d'esquena inespecífic (un dolor que no es pot localitzar o determinar una causa a través de l'examinació física o amb proves d'imatge) s'ha descrit en alguns casos de limfoma de Hodgkin. Sovint es troba afectada l'esquena inferior.[18]
- Febre cíclica: algunes persones poden presentar una febre cíclica i d'alta temperatura coneguda com a febre de Pel-Ebstein,[19] o simplement "febre P-E". No obstant això hi ha un debat sobre la validesa d'aquest signe.[20]
- Una síndrome nefròtica pot sorgir en individus amb limfoma de Hodgkin, sovint causada per una malaltia de canvis mínims.[21]
- Pot presentar obstrucció de les vies respiratòries, efusió pleural/del pericardi, disfunció hepatocel·lular o infiltració de la medul·la òssia.
Diagnòstic
[modifica]El limfoma de Hodgkin s'ha de distingir de causes no malignes del creixement dels ganglis limfàtics (com diverses infeccions) i altres tipus de càncer. El diagnòstic definitiu es fa a través de la biòpsia d'un gangli limfàtic (usualment amb una excisió i la posterior anàlisi de microscopi). L'hemograma pot servir per a jutjar la funció dels òrgans principals i per a comprovar la seguretat de la quimioteràpia. El PET-TAC s'utilitza per a trobar xicotets dipòsits que no es mostren en els TAC.
Tipus
[modifica]Hi ha dos tipus principals de limfoma de Hodgkin: el clàssic i el limfoma de Hodgkin amb limfòcits nodulars predominants. La prevalència del clàssic i del nodular són del 90% i el 10% respectivament.[22][23] La morfologia, fenotip, característiques moleculars, i presentació i comportament clínic d'aquests dos grups són, aleshores, diferent.[24]
Clàssic
[modifica]El limfoma de Hodgkin clàssic es pot classificar en quatre subtipus patològics basats en la morfologia de les cèl·lules de Reed-Sternberg i la composició de l'infiltrat reactiu de la cèl·lula que s'ha pogut observar en la biòpsia del gangli limfàtic (és a dir, quines cèl·lules acompanyes a la cèl·lula R-S).
| Nom | Descripció |
|---|---|
| Limfoma de Hodgkin amb esclerosi nodular | És el subtipus més comú i es compon de grans nòduls tumorals mostrant cèl·lules R-S disperses en un rerefons de limfòcits, eosinòfils i plasmòcits reactius amb graus variables de fibrosi del colàgen o esclerosi. |
| Subtipus de cel·lularitat mixta | És un subtipus comú i es caracteritza per tindre nombroses cèl·lules RS clàssiques barrejades amb cèl·lules inflamatòries reactives com limfòcits, histiòcits, eosinòfils, i plasmòcits sense esclerosi. Aquest tipus s'associa freqüentment a la infecció amb el virus d'Epstein-Barr i es pot confondre amb l'anomenada fase "cel·lular" o temprana del subtipus d'esclerosi nodular. Aquesta mena de limfoma de Hodgkin es troba sovint en pacients immunodeprimits. |
| Ric en limfòcits | És un subtipus rar que mostra moltes característiques el podrien fer confondre amb el limfoma no hodgkinià de cèl·lules B amb limfòcits nodulars predominants. Aquesta forma té el millor pronòstic. |
| Baix en limfòcits | És un subtipus rar, compost de grans quantitats de cèl·lules RS pleomòrfiques amb només uns quants limfòcits reactius que es pot confondre amb un limfoma difús de cèl·lules B grans. Molts d'aquests casos es classificarien en l'actualitat dins dels limfoma anaplàstic de cèl·lules gegants.[25] |


Encara que no s'expressen en totes les cèl·lules els marcadors tradicionals dels limfòcits B (com el CD20),[25] les cèl·lules de Reed-Sternberg sovint són de tipus B.[26][27] Encara que es classifica el limfoma de Hodgkin amb altres càncers de cèl·lula B, s'expressen alguns marcadors de limfòcits T (com a CD2 and CD4) de forma ocasional.[28] No obstant això, açò pot ser causat per interferències en les tècniques d'anàlisi.
Les cèl·lules de Hodgkin produeixen interleucina-21 (IL-21), que abans es creïa que era exclusiva dels limfòcits T. Aquesta característica pot explicar el comportament del limfoma de Hodgkin clàssic, incloent clústers d'altres cèl·lules immunes als voltants de les cèl·lules neoplàsiques.[29]
Amb limfòcits nodulars predominants
[modifica]El limfoma de Hodgkin amb limfòcits nodulars predominants (NLPHL en anglés) és un altre subtipus de limfoma de Hodgkin, diferent del limfoma de Hodgkin clàssic i es caracteritza per la presència de cèl·lules en forma de roses que expressen la proteïna CD20.[23][30] Arran d'aquestes diferències, entre d'altres, aquest subtipus sovint es tracta de forma diferent al limfoma de Hodgkin clàssic, amb l'ús de rituximab en combinació amb quimioteràpia AVBD, encara que els casos individuals varien i hi ha estudis clínics en procés.[23]
Estadiatge
[modifica]Després del diagnòstic del limfoma de Hodgkin, es farà un estadiatge, és a dir, una sèrie de proves que determinaran quines parts del cos es troben afectades. Segons aquest estadiatge, la persona serà classificada segons la classificació d'Ann Arbor:
- L'estadi I és l'afectació d'una única regió de ganglis limfàtics (I) (sobretot la zona cervical) o un sol lloc extralimfàtic (Ie);
- L'estadi II és l'afectació de dos o més regions de ganglis limfàtics en el mateix espai del diafragma (II) o d'una regió limfàtica i un lloc extralimfàtic contigu (IIe);
- L'estadi III és l'afectació de regions de ganglis limfàtics en ambdós llocs del diafragma, que poden incloure la melsa (IIIs) o extensió limitada i contigua a òrgans o espais extra limfàtics (IIIe, IIIes);
- L'estadi IV és l'afectació disseminada d'un o diversos òrgans extralimfàtics.
L'absència de símptomes sistèmics es representa afegint-hi "A" a l'estadiatge; la presència de símptomes sistèmics se significa afegint "B" a l'estadiatge. Per a l'extensió extranodal d'una massa de ganglis que no fa avançar l'estadiatge, es marca amb una "E". L'afectació de la melsa s'escriu afegint "S". La malaltia amb grans masses se defineix amb una "X".
- Estadis del limfoma de Hodgkin
-
Estadi I
-
Estadi II
-
Estadi III
-
Estadi IV
L'estadiatge és el mateix per als limfomes de Hodgkin i no hodgkinians.
Patologia
[modifica]- Macroscòpicament
Els ganglis limfàtics afectats (sovint els laterocervicals) es troben engrandits, però la seua forma és preservada i la càpsula no és envaïda pel tumor. Sovint, la superfície és blanca-grisenca i uniforme; en alguns subtipus com l'esclerosi nodular poden tindre un aspecte nodular.
En ocasions es pot observar un granuloma en anell de fibrina.
- Microscòpicament

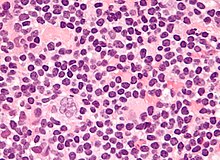
L'examinació de la biòpsia del gangli limfàtic mostra una destrucció completa o parcial de la seua arquitectura per cèl·lules grans i disperses conegudes com a cèl·lules Reed-Sternberg (CRS) barrejades amb un infiltrat de cèl·lules reactives compostes de proporcions vàries de limfòcits, histiòcits, eosinòfils i plasmòcits. Les cèl·lules de Reed-Sternberg s'identifiquen com cèl·lules grans, sovint binucleades amb nuclèols prominents i un fenotip inusual CD45-, CD30+, CD15+/-. En aproximadament un 50% dels casos, les cèl·lues de Reed–Sternberg es troben infectades pel virus d'Epstein-Barr.[31]
D'entre les característiques de les cèl·lules Reed-Sternberg clàssiques, podem trobar una mida cel·lular molt gran (20–50 micròmetres), un citoplasma abundant, amfofílic, amb un grànuls fins o homogeni, dos nuclis simètrics i emmirallats (ulls d'òliba) amb sengles nuclèols eosinofílics i una membrana nuclear gruixuda (es distribueix la cromatina vora la membrana nuclear). Quasi totes aquestes cèl·lules tenen còpies extra del cromosoma 9p/9p24.1.[32]
En podem observar les següents variants ariants:
- Cèl·lula de Hodgkin (CRS mononuclear atípic) és una variant de cèl·lula RS amb les mateixes característiques però que és mononucleada.
- RSC lacunar: són grans, amb un nucli hiperlobulat únic, nuclèols múltiples i petits i amb un citoplasma eosinofílic que envolta el nucli, creant un espai buit ("lacunae").
- CRS pleomòrfiques: tenen múltiples nuclis irregulars.
- CRS en forma de rosa (variant limfo-histiocítica): cèl·lula petita, amb nuclèols petits i un nucli molt lobulat.
- CRS "mòmia": té un nucli compacte sense nuclèol i amb citoplasma basofílic.
Encara que el limfoma de Hodgkin es pot subclassificar per tipus histiològics, no és tan important com en el limfoma no hodgkinià, ja que el tractament i el pronòstic en el limfoma de Hodgkin clàssic sovint depén més de l'estadiatge de la malaltia que en l'histotipus.[33]
Tractament
[modifica]L'enfocament actual del tractament vol evitar les toxicitats agudes (a curt termini) i a llarg termini associades amb el tractament, com la malaltia cardiovascular i els càncers secundaris, de forma que cresca la supervivència global.[34]
Tractaments històrics
[modifica]- MOPP (Meclormetina, Oncovin, Procarbazina, Prednisona): És el tractament original. El tractament s'administra en sis cicles de quatre setmanes. La meclormetina i la vincristina (Oncovin és el nom comercial anglés) s'administren per via intravenosa, i la procarbazina i la prednisona són pastilles que es prenen via oral. MOPP era el primer règimen de quimioteràpia que va assolir una gran quantitat d'èxit en la curació de la malaltia. Es va desenvolupar als Estats Units en la dècada dels anys 60. Ja no es considera un tractament efectiu per al limfoma de Hodgkin per la seua toxicitat i la seua relativa inefectivitat comparada amb tractaments més moderns.
- Stanford V: És una variant del règim ABVD de major intensitat i incorporant radioteràpia. En un estudi aleatori controlat fet en Itàlia, Stanford V era inferior a ABVD.[35] No obstant això, s'ha criticat aquest estudi per administrar la radioteràpia d'una forma diferent a l'establerta en el protocol inicial[36] Un estudi posterior mostra que el tractament Stanford V augmenta les toxicitats però no és superior a ABVD. Per això, no és un règim recomanat en l'actualitat.[37]
Tractaments actuals
[modifica]- Les persones amb malaltia inicial (IA or IIA) tenen una bona resposta a la radioteràpia. La presència d'una massa en el mediastí en qualsevol estadiatge es tracta amb una combinació de radioteràpia i quimioteràpia.[33] Els estadis > II (III, IVA, o IVB) només reben quimioteràpia. Per les toxicitats associades a la radioteràpia s'intenta reduir al màxim el seu ús, però encara es considera una part important del tractament de les persones amb malaltia amb massa o estadiatges menors.[38]
- ABVD (Adriamicina, Bleomicina, Vinblastina, Dacarbazina): És l'estratègia de quimioteràpia més usada arreu del món. Es va desenvolupar en Itàlia en 1970. Típicament el tractament s'administra cada dos setmanes durant sis o set mesos, encara que en ocasions pot ser necessari el tractament durant més temps.
- BEACOPP (Bleomicina, Adriamicina, Ciclofosfamida, Oncovin, Procarbazina i Prednisona) és una evolució del tractament BEACOPP que s'utilitza sobretot per a estadiatges > II en Europa. Per als estadiatges més alts la taxa de curació creix en un 10-15% respecte del règim ABVD, però la toxicitat (sobretot la taxa de càncers secundaris) és molt major. Per això, només s'administra a pacients selectes seguint el protocol PET-TAC.[39] Per la seua alta toxicitat aguda cal administrar-la junt a una medicació estimulant del sistema immunitari anomenada GCSF.[40]
- A+AVD (Adriamicina, brentuximab vedotina, Vinblastina, Dacarbicina) és una evolució del tractament ABVD amb la retirada de la bleomicina (que pot causar toxicitat cardíaca i pulmonar) i la inclusió d'una medicina de precisió que ataca les cèl·lules canceroses marcades amb CD30. Està pensada per a persones amb malaltia en estadi III o IV. Encara que és menys tòxic a llarg termini que el règim BEACOPP[41] i estalvia els efectes negatius de la bleomicina, presenta toxicitat en forma de neutropènia, exigint el tractament concomitant amb GCSF, i en forma de neuropatia perifèrica, que en un nombre molt petit dels casos pot arribar a ser permanent. Les taxes de cura, però, són molt altes.[42]
- Autotrasplantament de medul·la òssia en els pacients que responen de forma inadequada a la quimioteràpia o que tenen una malaltia que retorna després d'una primera remissió. Aproximadament el 50% dels pacients són curats amb aquest tractament.[43] Les persones que tornen a tindre una recaiguda després del trasplantament presenten un pronòstic molt pobre.[43]
Tractaments en desenvolupament
[modifica]- La inclusió d'immunoteràpia amb bloquejadors de PD-1 com nivolumab o pembroluzimab per a la malaltia que retorna després d'un autotransplantament de medul·la òssia o en aquelles persones que tenen contraindicat aquest tractament. En monoteràpia[44][45] es considera com un tractament pal·liatiu, després de (és a dir, per a reduir els símptomes). En combinació amb la brentuximab vedotina té una intenció curativa en una part dels pacients.[46] Aquest tractament és altament efectiu però s'associa a toxicitat autoimmune i pulmonar en un quart dels pacients tractats i es reserva a pacients que no responen als tractaments habituals. Sovint s'utilitza també com a pont per a un al·lotransplantament de medul·la òssia en persones amb un autotransplantament previ que no controlen la malaltia. Aquest tractament es considera curatiu en la majoria de persones però té un grau de complicacions derivades molt alt, podent causar la mort per la malaltia de l'empelt contra l'hoste o per la profunda immunodepressió conseqüència de la quimioteràpia per a poder dur endavant el tractament.
- Cèl·lules CAR-T. És una mena d'immunoteràpia que utilitza cèl·lules immunes de l'individu i les programa per a atacar les cèl·lules canceroses. Aquest tractament s'utilitza principalment per a les leucèmies agudes i els limfoma no hodgkinians, però s'ha demostrat que també són útils en el limfoma de Hodgkin refractari i retornat, fins i tot aquells que no han respost a una gran quantitat de règims de quimioteràpia i trasplantaments anteriors.[47] El tractament amb cèl·lules CAR-T s'associa a una síndrome d'alliberament de citocines i toxicitat neuronal transitòries, per això s'ha d'administrar en centres d'especialitat. És un tractament amb un cost elevat i requereix unes necessitats tècniques i logístiques molt complexes que retarden la seua generalització.[48] Als Països Catalans només tenen llicència per a administrar aquest tractament els centres del Clínic de Barcelona, l'Hospital Clínic Universitari de València, l'Hospital de la Santa Creu i Sant Pau, l'Hospital Universitari i Politècnic La Fe, i l'Hospital Sant Joan de Déu, encara que no s'ha aprovat encara les cèl·lules CAR-T per al limfoma de Hodgkin.[49]
El rituximab (anticòs monoclonal contra CD20), tractament important en el limfoma no hodgkinià, no s'utilitza perquè la majoria dels casos les cèl·lules no presenten l'antigen CD20. Podria tindre alguna utilitat en els casos de limfòcits nodulars predominants.[50] En un estudi de 2019 es va veure que era eficaç en la majoria dels casos en combinació amb altres règims de quimioteràpia.[51]
Encara que una major edat al diagnòstic és un factor de pronòstic advers per al limfoma de Hodgkin, en general les persones majors sense comorbiditats poden tolerar la teràpia estàndard, i tenen uns resultats comparables als dels jóvens. No obstant això, es considera una entitat diferent en les persones majors i hi ha consideracions diferents en el moment de decidir els tractaments.[52]
Les altes taxes de curació i la llarga supervivència de molts pacients amb limfoma de Hodgkin han portat a una alta preocupació pels efectes a llarg termini del tractament, incloent la malaltia cardiovascular i segons càncers com leucèmies agudes, limfomes, i tumors sòlids en el camp de radiació. La majoria dels pacients amb malaltia primerenca reben un tractament abreujat i radioteràpia localitzada en comptes de general.
En els casos infantils es poden observar problemes endocrins crònics com disfunció gonadal i problemes de creixement. La disfunció gonadal és el més sever, i és causat sobretot per la quimioteràpia o la radioteràpia pèlvica.[53]
Pronòstic
[modifica]El tractament del limfoma de Hodgkin ha millorat les darreres dècades. Els últims assajos clínics amb nous tipus de quimioteràpia han permés taxes de supervivència més altes que mai. En un assaig europeu recent, la supervivència durant 5 anys de les persones amb un pronòstic favorable era dle 98%, mentre que aquella amb un pronòstic pitjor era almenys del 85%.[54]
Els factors que indiquen un pronòstic advers que es van identificar en un estudi europeu[55] són:
- Edat ≥ 45 anys
- Estadi IV
- Hemoglobina < 10,5 g/dl
- Limfòcits < 600/µl o < 8%
- Mascle
- Albúmina < 4.0 g/dl
- Leucòcits ≥ 15,000/µl
Altres estudis han reportat que els subtipus histològics de cel·lularitat mixta o baix en limfòcits, la presència de símptomes B, una velocitat de sedimentació globular alta, i una malaltia amb massa (bulky disease) al mediastí són també marques de pronòstic advers. En els darrers anys, l'ús de la tomografia per emissió de positrons(PET-TAC) poc després d'iniciar la quimioteràpia ha demostrat un gran poder pronòstic.[55] Açò permet establir la resposta d'un individu a la quimioteràpia ja que el PET es desactiva ràpidament en persones que responen a la teràpia. En aquest estudi,[55] després de dos cicles de quimioteràpia ABVD, un 83% de persones es trobaven en remissió després de 3 anys si tenien un PET negatiu contra només un 28% en aquells amb estudis PET positius. Aquest mètode és una millora dels factors pronòstics habituals. Un estudi de 2019 demostra l'eficàcia d'adaptar el tractament a la resposta radiogràfica segons l'estadiatge de la malaltia i els resultats de les proves d'imatges PET-TAC, de forma que les persones amb malaltia activa després de dos cicles de quimioteràpia estàndard poden ampliar a un règim més agressiu, o en canvi, si s'observa una resposta molt positiva, estalviar tractament innecessari per al pacient, reduint les toxicitats i efectes secundaris.[39] No obstant això, l'estudi reconeix que el PET-TAC no sempre és eficaç i que malgrat les adaptacions del tractament es poden observar toxicitats a llarg termini, com a càncers secundaris.[39]
Epidemiologia
[modifica]
Al contrari que altres limfomes, en què la incidència creix amb la edat, el limfoma de Hodgkin té una corba bimodal de casos, és a dir, que ocorre més freqüentment en dos grups d'edats diferents, el primer sent els adults jóvens (15-35 anys) i el segon en majors de 55 anys, encara que aquesta distribució varia lleument en diferents parts del món.[57] De mitjana, és més comú en els hòmens, llevat de la variant amb esclerosi nodular, que és lleument més comú en dones. Els casos a l'any de limfoma de Hodgkin són 2.7 per 100,000 persones per any, i la malaltia causa un poc menys del 1% dels càncers arreu del món.[58]
El 2010 va causar 18.000 morts globalment, un descens de les 19.900 registrades en 1990.[59] El 2012 es van estimar 65.950 casos i 25.469 morts pel limfoma de Hodgkin arreu del món, amb 28.852 i 37.098 casos en els països desenvolupats i en vies de desenvolupament, respectivament.[60] No obstant això, si ajustem a l'edat, les taxes més altes es troben en les zones desenvolupades, amb les taxes més altes en les Amèriques i el Mediterrani Oriental (1,5 per 100.000) i Europa (2 per 100.000).[60] El Mediterrani oriental també té la mortalitat ajustada a l'edat més alta, amb una mort per cada 100.000, atribuït principalment a l'estil de vida i als riscs ambientals associats amb les economies en transició com fumar, obesitat, inactivitat física, i els comportament reproductius, així com la baixa disponibilitat de les pràctiques diagnòstiques i una baixa coneixença de la malaltia.[60]
El nombre de casos de limfoma de Hodgkin creix en les persones infectades amb el VIH.[61] En contrast amb els altres limfomes que s'associen a la infecció per VIH ocorre normalment en persones amb comptes més alts de cèl·lules T CD4
S'ha estimat que a l'estat espanyol es realitzen anualment uns 1.400 diagnòstics de limfoma de Hodgkin, segons la prevalència europea de 2019.[62] Per a l'any 2021 s'estimaren 1.527 casos.[63]
Història
[modifica]
El limfoma de Hodgkin es va descriure per primera vegada en un reportatge de 1832 per Thomas Hodgkin, encara que Hodgkin va avisar que potser ja s'havia descrit amb anterioritat per Marcello Malpighi en 1666.[64][13] Mentre treballava al museu del Guy's Hospital, en Londres, Hodgkin va estudiar set persones amb creixement indolor dels ganglis limfàtics. Dels set casos, dos es trobaven sota l'auspici de Richard Bright, un altre de Thomas Addison, i un altre de Robert Carswell.[64] El reportatge de Carswell del seu cas es trobava acompanyat de nombroses il·lustracions que acompanyaven les primeres descripcions de la malaltia.[65]
L'estudi de Hodgkin dels set casos, titulat "On some morbid appearances of the absorbent glands and spleen", es va presentar a la Medical and Chirurgical Society of London el gener de 1832 i es va publicar subseqüentment en la resvista de la societat.[64] L'article de Hodgkin no va tindre gaire repercussió, fins i tot malgrat el destacament de Bright en una publicació posterior.[64] De fet, Hodgkin mateix pensava que l'article no tenia excessiva rellevància.[66] Mostres dels teixits dels set casos de Hodgkins es van perservar en Guy's Hospital. Vora 100 anys després de la publicació inicial de Hodgkin la reexaminació histopatològica va confirmar el limfoma de Hodgkin només en tres de set persones.[66] La resta de casos incloïen el limfoma no hodgkinià, tuberculosis, i sífilis.[66]
En 1856, Samuel Wilks va reportar de forma independent una sèrie de pacients amb la mateixa malaltia que Hodgkin havia descrit anteriorment.[66] Wilks, un successor de Hodgkin en el Guy's Hospital, no era conscient del seu treball previ en la matèria. Bright va informar Wilks de la contribució de Hodgkin i en 1865, Wilks va publicar un segon article, titulat "Cases of enlargement of the lymphatic glands and spleen", en què va anomenar la malaltia "malaltia de Hodgkin" en honor al seu predecessor.[66]
Theodor Langhans i WS Greenfield van descriure per primera vegada les característiques microscòpiques del limfoma de Hodgkin en 1872 i 1878, respectivament.[64] El 1898 i 1902, respectivament, Carl Sternberg i Dorothy Reed descrigueren de forma independent les característiques citogenètiques de les cèl·lules malignes del limfoma de Hodgkin, ara anomenades cèl·lules Reed-Sternberg.[64]
El limfoma de Hodgkin fou un dels primers càncers en tractar-se exitosament amb radioteràpia i posteriorment amb quimioteràpia.
Referències
[modifica]- ↑ 1,0 1,1 1,2 1,3 «Adult Hodgkin Lymphoma Treatment (PDQ)–Patient Version», 03-08-2016. Arxivat de l'original el 28 juliol 2016. [Consulta: 12 agost 2016].
- ↑ Bower, Mark; Waxman, Jonathan. Lecture Notes: Oncology. 2a edició. John Wiley & Sons, 2011, p. 195. ISBN 978-1118293003.
- ↑ Moses, Scott «Pruritus». American Family Physician, 68, 6, 15-09-2003, pàg. 1135–1142. ISSN: 0002-838X.
- ↑ 4,0 4,1 4,2 4,3 «SEER Stat Fact Sheets: Hodgkin Lymphoma», 01-04-2016. Arxivat de l'original el 17 octubre 2012. [Consulta: 13 agost 2016].
- ↑ 5,0 5,1 World Cancer Report 2014. World Health Organization, 2014, p. Chapter 2.4. ISBN 978-928320429-9.
- ↑ «Hodgkin's lymphoma and its association with EBV and HIV infection». Critical Reviews in Clinical Laboratory Sciences, 55, 2, 3-2018, pàg. 102–114. DOI: 10.1080/10408363.2017.1422692. PMID: 29316828.
- ↑ 7,0 7,1 «Adult Hodgkin Lymphoma Treatment (PDQ)–Patient Version», 03-08-2016. Arxivat de l'original el 28 juliol 2016. [Consulta: 13 agost 2016].
- ↑ 8,0 8,1 8,2 «Early-stage Hodgkin's lymphoma». The New England Journal of Medicine, 363, 7, 8-2010, pàg. 653–62. DOI: 10.1056/NEJMra1003733. PMID: 20818856.
- ↑ «Childhood and adolescent cancer statistics, 2014». Ca, 64, 2, 2014, pàg. 83–103. DOI: 10.3322/caac.21219. PMID: 24488779.
- ↑ «Resultats dels Registres de Tumors Hospitalaris de l'Institut Català d'Oncologia en aliança amb l’Institut Català de la Salut 2013-2017». [Consulta: 30 agost 2020].
- ↑ Vos, Theo; Allen, Christine; Arora, Megha; Barber, Ryan M.; Bhutta, Zulfiqar A.; Brown, Alexandria; Carter, Austin; Casey, Daniel C.; Charlson, Fiona J. «Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015». Lancet, 388, 10053, 10-2016, pàg. 1545–1602. DOI: 10.1016/S0140-6736(16)31678-6. PMC: 5055577. PMID: 27733282.
- ↑ Wang, Haidong; Naghavi, Mohsen; Allen, Christine; Barber, Ryan M.; Bhutta, Zulfiqar A.; Carter, Austin; Casey, Daniel C.; Charlson, Fiona J.; Chen, Alan Zian «Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015». Lancet, 388, 10053, 10-2016, pàg. 1459–1544. DOI: 10.1016/s0140-6736(16)31012-1. PMC: 5388903. PMID: 27733281.
- ↑ 13,0 13,1 Hodgkin T «On some morbid experiences of the absorbent glands and spleen». Med Chir Trans, 17, 1832, pàg. 69–97.
- ↑ «Hodgkin Lymphoma: Diagnosis and Treatment». Mayo Clinic Proceedings, 90, 11, 11-2015, pàg. 1574–83. DOI: 10.1016/j.mayocp.2015.07.005. PMID: 26541251.
- ↑ Portlock CS. «Hodgkin Lymphoma». Merck Manual Professional, 01-07-2008. Arxivat de l'original el 28 juny 2009. [Consulta: 18 juny 2009].
- ↑ «Alcohol-related pain and Hodgkin's disease». The Western Journal of Medicine, 138, 6, 6-1983, pàg. 874–5. PMC: 1010854. PMID: 6613116.
- ↑ Page 242 Arxivat 2015-09-20 a Wayback Machine. in: John Kearsley. Cancer: A Comprehensive Clinical Guide. Washington, DC: Taylor & Francis, 1998. ISBN 978-90-5702-215-9.
- ↑ «Hodgkin Lymphoma». [Consulta: 25 juliol 2021].
- ↑ «Clinical Evaluation and Staging of Hodgkin Lymphoma». A: Hodgkin's disease. 2a edició. Lippincott Williams & Wilkins, 2007, p. 123–132. ISBN 978-0-7817-6422-3.
- ↑ «Pel-Ebstein fever». The New England Journal of Medicine, 333, 1, 7-1995, pàg. 66–7. DOI: 10.1056/NEJM199507063330118. PMID: 7777006.
- ↑ «Occurrence of minimal change nephrotic syndrome in classic Hodgkin lymphoma is closely related to the induction of c-mip in Hodgkin-Reed Sternberg cells and podocytes». Blood, 115, 18, 5-2010, pàg. 3756–62. DOI: 10.1182/blood-2009-11-251132. PMC: 2890576. PMID: 20200355.
- ↑ «Guidelines for the investigation and management of nodular lymphocyte predominant Hodgkin lymphoma». British Journal of Haematology, 172, 1, 1-2016, pàg. 32–43. DOI: 10.1111/bjh.13842. PMID: 26538004.
- ↑ 23,0 23,1 23,2 WHO classification of tumours of haematopoietic and lymphoid tissues. Revised 4th, 2017-09-18. ISBN 978-92-832-4494-3. OCLC 1011064243.
- ↑ Re, Daniel; Thomas, Roman K.; Behringer, Karolin; Diehl, Volker «From Hodgkin disease to Hodgkin lymphoma: biologic insights and therapeutic potential» (en anglès). Blood, 105, 12, 15-06-2005, pàg. 4553–4560. DOI: 10.1182/blood-2004-12-4750. ISSN: 0006-4971. PMID: 15728122.
- ↑ 25,0 25,1 «HMDS: Hodgkin's Lymphoma». Arxivat de l'original el 4 març 2009. [Consulta: 1r febrer 2009].
- ↑ «Biology of Hodgkin's lymphoma». Annals of Oncology, 13 Suppl 1, 2002, pàg. 11–8. DOI: 10.1093/annonc/13.S1.11. PMID: 12078890.
- ↑ «Molecular biology of Hodgkin's and Reed/Sternberg cells in Hodgkin's lymphoma». International Journal of Cancer, 118, 8, 4-2006, pàg. 1853–61. DOI: 10.1002/ijc.21716. PMID: 16385563.
- ↑ «Rare expression of T-cell markers in classic Hodgkin's lymphoma». Modern Pathology, 18, 12, 12-2005, pàg. 1542–9. DOI: 10.1038/modpathol.3800473. PMID: 16056244.
- ↑ «Aberrant expression of the Th2 cytokine IL-21 in Hodgkin lymphoma cells regulates STAT3 signaling and attracts Treg cells via regulation of MIP-3alpha». Blood, 112, 8, 10-2008, pàg. 3339–47. DOI: 10.1182/blood-2008-01-134783. PMID: 18684866.
- ↑ «Hodgkin Lymphoma: Diagnosis and Treatment». Mayo Clinic Proceedings, 90, 11, 2015, pàg. 1574–1583. DOI: 10.1016/j.mayocp.2015.07.005. PMID: 26541251.
- ↑ «Epstein-Barr virus and the origin of Hodgkin lymphoma». Chinese Journal of Cancer, 33, 12, 12-2014, pàg. 591–7. DOI: 10.5732/cjc.014.10193. PMC: 4308654. PMID: 25418190.
- ↑ «Genomic analyses of flow-sorted Hodgkin Reed-Sternberg cells reveal complementary mechanisms of immune evasion». Blood Advances, 3, 23, 12-2019, pàg. 4065–4080. DOI: 10.1182/bloodadvances.2019001012. PMC: 6963251. PMID: 31816062.
- ↑ 33,0 33,1 «Hodgkin lymphoma». [Consulta: 25 juliol 2021].
- ↑ «Interim PET-results for prognosis in adults with Hodgkin lymphoma: a systematic review and meta-analysis of prognostic factor studies». The Cochrane Database of Systematic Reviews, 1, 8, 1-2020, pàg. CD012643. DOI: 10.1002/14651858.CD012643.pub3. PMC: 6984446. PMID: 31930780.
- ↑ «ABVD versus modified stanford V versus MOPPEBVCAD with optional and limited radiotherapy in intermediate- and advanced-stage Hodgkin's lymphoma: final results of a multicenter randomized trial by the Intergruppo Italiano Linfomi». Journal of Clinical Oncology, 23, 36, 12-2005, pàg. 9198–207. DOI: 10.1200/JCO.2005.02.907. PMID: 16172458.
- ↑ «Stanford V program for locally extensive and advanced Hodgkin lymphoma: the Memorial Sloan-Kettering Cancer Center experience». Annals of Oncology, 21, 3, 3-2010, pàg. 574–581. DOI: 10.1093/annonc/mdp337. PMID: 19759185.
- ↑ Hoskin, Peter J.; Lowry, Lisa; Horwich, Alan; Jack, Andrew; Mead, Ben «Randomized Comparison of the Stanford V Regimen and ABVD in the Treatment of Advanced Hodgkin's Lymphoma: United Kingdom National Cancer Research Institute Lymphoma Group Study ISRCTN 64141244». Journal of Clinical Oncology, 27, 32, 08-09-2009, pàg. 5390–5396. DOI: 10.1200/JCO.2009.23.3239. ISSN: 0732-183X.
- ↑ «Omitting Radiation From Treatment for Early-Stage Hodgkin Lymphoma Increases Risk of Recurrence - The ASCO Post». [Consulta: 23 agost 2021].
- ↑ 39,0 39,1 39,2 Stephens, Deborah M.; Li, Hongli; Schöder, Heiko; Straus, David J.; Moskowitz, Craig H. «Five-year follow-up of SWOG S0816: limitations and values of a PET-adapted approach with stage III/IV Hodgkin lymphoma». Blood, 134, 15, 10-10-2019, pàg. 1238–1246. DOI: 10.1182/blood.2019000719. ISSN: 0006-4971.
- ↑ «Home | German Hodgkin Study Group». Ghsg.org. Arxivat de l'original el 2011-08-17. [Consulta: 26 agost 2012].
- ↑ Diehl, Louis F. «A+AVD versus eBEACOPP in advanced-stage Hodgkin lymphoma» (en anglès). The Lancet Haematology, 8, 6, 01-06-2021, pàg. e384–e386. DOI: 10.1016/S2352-3026(21)00129-0. ISSN: 2352-3026. PMID: 34048674.
- ↑ Ansell, Stephen M. «Hodgkin lymphoma: MOPP chemotherapy to PD-1 blockade and beyond» (en anglès). American Journal of Hematology, 91, 1, 2016, pàg. 109–112. DOI: 10.1002/ajh.24226. ISSN: 1096-8652.
- ↑ 43,0 43,1 Broccoli, Alessandro; Zinzani, Pier Luigi «The role of transplantation in Hodgkin lymphoma» (en anglès). British Journal of Haematology, 184, 1, 2019, pàg. 93–104. DOI: 10.1111/bjh.15639. ISSN: 1365-2141.
- ↑ Momotow, Jesko; Goergen, Helen; Behringer, Karolin; Bröckelmann, Paul J.; Borchmann, Sven «Nivolumab in Relapsed/Refractory Classical Hodgkin Lymphoma – Extended Follow-up of 30 Patients Treated Within the CheckMate 205 Trial in a Single-Center» (en anglès). HemaSphere, 3, 5, 10-2019, pàg. e293. DOI: 10.1097/HS9.0000000000000293. ISSN: 2572-9241.
- ↑ «Pembrolizumab aprobado para linfoma de Hodgkin - Instituto Nacional del Cáncer» (en castellà), 05-01-2017. [Consulta: 23 agost 2021].
- ↑ Advani, Ranjana H.; Moskowitz, Alison J.; Bartlett, Nancy L.; Vose, Julie M.; Ramchandren, Radhakrishnan «Brentuximab vedotin in combination with nivolumab in relapsed or refractory Hodgkin lymphoma: 3-year study results». Blood, 138, 6, 12-08-2021, pàg. 427–438. DOI: 10.1182/blood.2020009178. ISSN: 0006-4971.
- ↑ Ramos, Carlos A.; Grover, Natalie S.; Beaven, Anne W.; Lulla, Premal D.; Wu, Meng-Fen «Anti-CD30 CAR-T Cell Therapy in Relapsed and Refractory Hodgkin Lymphoma». Journal of Clinical Oncology, 38, 32, 23-07-2020, pàg. 3794–3804. DOI: 10.1200/JCO.20.01342. ISSN: 0732-183X. PMC: PMC7655020. PMID: 32701411.
- ↑ «El acceso a las CAR-T en España, condicionado por aspectos logísticos y organizacionales | @diariofarma» (en castellà), 10-07-2020. [Consulta: 23 agost 2021].
- ↑ «Ministerio de Sanidad, Consumo y Bienestar Social - Profesionales - Ministerio de Sanidad, Política Social e Igualdad - Profesionales - Terapias Avanzadas». Arxivat de l'original el 2021-08-23. [Consulta: 23 agost 2021].
- ↑ «Rituximab in Hodgkin lymphoma: is the target always a hit?». Cancer Treatment Reviews, 37, 5, 8-2011, pàg. 385–90. DOI: 10.1016/j.ctrv.2010.11.005. PMID: 21183282.
- ↑ Sano, Dahlia; Strati, Paolo; Alcedo, Pedro; Rao, V Ahalya; Singh, Prachee «Maintenance Rituximab in Nodular Lymphocyte Predominant Hodgkin Lymphoma (NLPHL) in the First Line Setting or at Relapse». Blood, 134, Supplement_1, 13-11-2019, pàg. 5291–5291. DOI: 10.1182/blood-2019-125980. ISSN: 0006-4971.
- ↑ «Hodgkin's lymphoma in the elderly: a different disease in patients over 60». Oncology, 21, 8, 7-2007, pàg. 982–90; discussion 990, 996, 998 passim. Arxivat de l'original el 2009-05-12. PMID: 17715698.
- ↑ «Long-term endocrine side effects of childhood Hodgkin's lymphoma treatment: a review». Human Reproduction Update, 18, 1, 2011, pàg. 12–28. DOI: 10.1093/humupd/dmr038. PMID: 21896559.
- ↑ «Chemotherapy plus involved-field radiation in early-stage Hodgkin's disease». The New England Journal of Medicine, 357, 19, 11-2007, pàg. 1916–27. DOI: 10.1056/NEJMoa064601. PMID: 17989384.
- ↑ 55,0 55,1 55,2 «International validation study for interim PET in ABVD-treated, advanced-stage hodgkin lymphoma: interpretation criteria and concordance rate among reviewers». Journal of Nuclear Medicine, 54, 5, 5-2013, pàg. 683–90. DOI: 10.2967/jnumed.112.110890. PMID: 23516309.
- ↑ «WHO Disease and injury country estimates». World Health Organisation, 2009. Arxivat de l'original el 2009-11-11. [Consulta: 11 novembre 2009].
- ↑ Mauch, Peter; Armitage, James; Diehl, Volker; Hoppe, Richard; Weiss, Laurence. Hodgkin's Disease. Lippincott Williams & Wilkins, 1999, p. 62–64. ISBN 978-0-7817-1502-7.
- ↑ «SEER Stat Fact Sheets: Leukemia». Arxivat de l'original el 17 octubre 2012. [Consulta: 18 agost 2014].
- ↑ «Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden 1of Disease Study 2010». Lancet, 380, 9859, 12-2012, pàg. 2095–128. DOI: 10.1016/S0140-6736(12)61728-0. OCLC: 23245604. PMID: 23245604.
- ↑ 60,0 60,1 60,2 «Epidemiological Overview of Hodgkin Lymphoma across the Mediterranean Basin». Mediterranean Journal of Hematology and Infectious Diseases, 6, 1, 29-06-2014, pàg. e2014048. DOI: 10.4084/mjhid.2014.048. PMC: 4103499. PMID: 25045456.
- ↑ «Hodgkin lymphoma and immunodeficiency in persons with HIV/AIDS». Blood, 108, 12, 12-2006, pàg. 3786–91. DOI: 10.1182/blood-2006-05-024109. PMC: 1895473. PMID: 16917006.
- ↑ «Linfoma de Hodgkin - SEOM: Sociedad Española de Oncología Médica © 2019». [Consulta: 23 agost 2021].
- ↑ «Las cifras del cáncer en España». Sociedad Española de Oncología Médica, 2021.
- ↑ 64,0 64,1 64,2 64,3 64,4 64,5 Hellman S. «Brief Consideration of Thomas Hodgkin and His Times». A: Hodgkin Lymphoma. 2a edició. Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins, 2007, p. 3–6. ISBN 978-0-7817-6422-3.
- ↑ «The original illustrations of Hodgkin's disease». Annals of Diagnostic Pathology, 3, 6, 12-1999, pàg. 386–93. DOI: 10.1016/S1092-9134(99)80018-5. PMID: 10594291.
- ↑ 66,0 66,1 66,2 66,3 66,4 «Comments on the anniversary of the description of Hodgkin's disease». Journal of the National Medical Association, 76, 8, 8-1984, pàg. 815–7. PMC: 2609834. PMID: 6381744.
Enllaços externs
[modifica]- «Limfoma de Hodgkin (LH)». Canal Salut. Generalitat de Catalunya.



