Nitrat de liti
 | |
| Substància química | tipus d'entitat química |
|---|---|
| Massa molecular | 69,003822 Da |
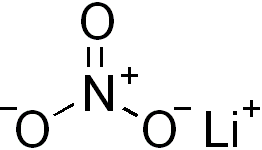
| Estructura química | |
| Fórmula química | LiNO₃ |
 | |
| SMILES canònic | |
| Identificador InChI | Model 3D |
| Propietat | |
| Punt de fusió | 255 °C 253 °C |
| NFPA 704: Standard System for the Identification of the Hazards of Materials for Emergency Response () | |
El nitrat de liti és un compost inorgànic amb la fórmula química LiNO₃. És la sal de liti de l'àcid nítric. Es produeix fent reaccionar carbonat de liti o hidròxid de liti amb àcid nítric.
Usos
[modifica]Aquesta sal deliqüescent incolora és un agent oxidant utilitzat en la fabricació de focs artificials i engales de pirotècnia.
El nitrat de liti s'ha proosat com una manera d'emmagatzemar calor solar per a cuinar. Es podria usar una lent de Fresnel per a fondre el nitrat de liti sòlid, la qual cosa podria fer la funció de 'bateria solar', permetent distribuir la calor més tard per convecció.[1]
El LiNO₃ s'utilitza en les interaccions solut-solvent en temperatures en disminució (és a dir, 329-290 K).[2]
Actualment, el nitrat de liti s'està provant per a poder-lo aplicar en paviments de ciment per disminuir els efectes de la meteorització.[3]
També es fa servir el nitrat de liti com catalitzador en òxids de nitrogen.[4]
Síntesi
[modifica]El nitrat de liti es pot sintetitzar per reacció de l'àcid nítric i el carbonat de liti.
Li₂CO₃ + 2HNO₃ → 2LiNO₃ + H₂O + CO₂
Toxicitat
[modifica]El nitrat de liti pot ser tòxicdins del cos si s'ingereix i afecta el sistema nervós central, la tiroïdes, els ronyons i el sistema cardiovascular.[5] És irritant en contacte amb la pell, ulls i les membranes mucoses.
Referències
[modifica]- ↑ http://barbequelovers.com/grills/a-solar-grill-prototype-for-a-greener-tomorrow
- ↑ Berchiesi, G [et al]. Journal of Chemical and Engineering Data, 30, 1985, pàg. 208–209.
- ↑ Kelly, M [et al]. American Society of Civil Engineers, 191, 2006, pàg. 625–635.
- ↑ Ruiz, M [et al]. I and EC research, 51, 2012, pàg. 1150–1157.
- ↑ «Material Safety Data Sheet». Sigma-Aldrich Catalog. [Consulta: 12 abril 2012].