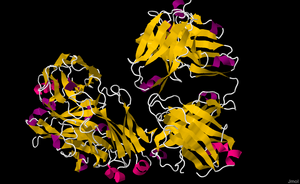
Rituximab
 | |
| Substància química | tipus d'entitat química |
|---|---|
| Rol | factor immunològic, fàrmac antireumàtic modificador de la malaltia, agent antineoplàstic immunològic, medicament essencial i anticòs monoclonal |
| Altres | |
| medicament biològic | |
Rituximab, venut sota la marca Rituxan entre d'altres, és un medicament usat per a tractar determinades malalties autoimmunitàries i alguns tipus de càncer.[1] Es fa servir per al limfoma no hodgkinià, la leucèmia limfocítica crònica, l'artritis reumatoide, la granulomatosi amb poliangiïtis, la púrpura trombocitopènica idiopàtica, el pèmfig vulgar, la miastènia gravis i les aftes positives pel virus d'Epstein-Barr.[1][2][3][4] S'administra per via intravenosa.[1]
Els efectes secundaris més comuns, que sovint ocorren dos hores després d'injectar el medicament, inclouen erupcions, coïssor, hipotensió arterial, i falta d'aire.[1] Altres efectes més greus són la reactivació del virus de l'hepatitis B en persones prèviament infectades, la leucoencefalopatia multifocal progressiva, i la necròlisi epidèrmica tòxica, entre d'altres[1][5] No queda clar si és segur durant l'embaràs per al fetus i el nadó; només hauria d'administrar-se a dones embarassades si els beneficis de la seva administració superen els riscos.[1][6]
El rituximab és un anticòs monoclonal quimèric contra la proteïna CD20, (de l'anglès cluster of differentiation 20) que es troba principalment en la superfície dels limfòcits B.[7] Quan es lliga a aquesta proteïna, inicia la mort cel·lular.[1]
Va rebre l'autorització d'ús mèdic en 1997[7] i és un fàrmac inclòs en la Llista model de Medicaments essencials de l'Organització Mundial de la Salut.[8] La patent es va exhaurir en 2016, i uns quants biosimilars s'han desenvolupat[9]
Usos mèdics
[modifica]Rituximab destrueix els limfòcits B tant malignes com normals que expressen CD20 en la seua superfície, i per això es fa servir en malalties que es caracteritzen per l'activitat anormal d'aquestes cèl·lules.
S'utilitza combinat amb la fludarabina i la ciclofosfamida per a tractar la leucèmia limfocítica crònica CD20+.[10] En combinació amb el metotrexat tracta l'artritis reumatoide moderada o greu amb una resposta inadequada a un o més inhibidors del TNF.[10] Amb combinació amb glucocorticoides tracta la granulomatosi amb poliangiïtis i la poliangiïtis microscòpica.[10]
Amb combinació amb la hialuronidasa humana, comercialitzada amb els noms MabThera SC i Rituxan Hycela,[11] es tracta el limfoma fol·licular, el limfoma difús de cèl·lules B grans, i la leucèmia limfocítica crònica.[12]
Càncers de la sang
[modifica]El rituximab s'utilitza per a tractar els càncers de la sang com la leucèmia i el limfoma, incloent el limfoma no hodgkinià, la leucèmia limfocítica crònica, i el subtipus amb predomini limfocític del limfoma de Hodgkin.[13] Açò també inclou la macroglobulinèmia de Waldenström, una mena de limfoma no hodgkinià.[1]
Malalties autoimmunitàries
[modifica]El rituximab va mostrar-se efectiu com a tractament de l'artritis reumatoide en tres assajos clínics aleatoritzats i té una llicència d'ús per a casos refractaris d'aquest malaltia.[14] Als Estats Units, ha estat aprovat per l'FDA amb combinació del metotrexat (MTX) per a reduir signes i símptomes en pacients adults amb artritis reumatoide activa de moderada a severa que ha tingut una resposta inadequada a més d'un tractament anti-TNF. A Europa, la llicència és una mica més restrictiva: té llicència per a l'ús combinat amb MTX en pacients amb RA activa i severa que han tingut una resposta inadequada a més d'una teràpia anti-TNF.[15]
Hi ha evidència de l'eficàcia, encara que no necessàriament de la seguretat en un rang d'altres malalties autoimmunitàries, i el rituximab s'utilitza amplament fora d'autorització per a tractar casos difícils d'esclerosi múltiple,[16][17] lupus eritematós sistèmic, poliradiculoneuropatia desmielinitzant inflamatòria crònica i anèmies autoimmunitàries.[18] L'efecte secundari més perillós (encara que dels més estranys) és la leucoencefalopatia multifocal progressiva (LMP) causada per una infecció, normalment fatal; no obstant això només s'han registrat una minoria dels casos en malalties autoimmunitàries.[18][19]
Altres malalties autoimmunitàries que s'han tractat amb rituximab inclouen l'anèmia hemolítica autoimmunitària, l'aplàsia pura de l'eritròcit, la púrpura trombocitopènica trombòtica (PTT),[20] la púrpura trombocitopènica idiopàtica (PTI),[21][22] la síndrome d'Evans,[23] les vasculitis (per exemple, la granulomatosi amb poliangiïtis), trastorns de la pell (com el pèmfig o altres dermatosis ampul·lars, amb molts bons resultats d'una cura aproximada del 85 per cent en el pèmfig, segons un estudi de l'any 2006),[24] la diabetis mellitus tipus 1, la síndrome de Sjögren, l'encefalitis per anticossos contra el receptor d'NMDA5, la neuromielitis òptica,[25] l'oftalmopatia de Graves,[26] la pancreatitis autoimmunitària,[27] l'atàxia opsoclona-mioclona (AOM),[28] i la malaltia relacionada amb IgG4.[29] No se n'ha demostrat l'efectivitat per al tractament de les malalties autoimmunitàries relacionades amb la IgA.[30]
Trasplantaments d'òrgans
[modifica]El rituximab es fa servir fora de llicència per a gestionar els trasplantaments de ronyó. Aquest medicament pot ser útil en trasplantaments entre persones amb grups sanguinis incompatibles. També s'utilitza com a teràpia d'inducció en pacients molt sensibles que procediran al trasplantament. No s'ha demostrat l'eficàcia del rituximab en aquest àmbit, i com qualsevol altre agent preparador, comporta un risc d'infecció.
Efectes adversos
[modifica]Els efectes adversos més seriosos, que poden causar mort i discapacitat, inclouen:[10][1]
- Reaccions en el lloc d'administració i síndrome d'alliberament de citocines.
- Aturada cardiorespiratòria
- Síndrome de la lisi tumoral, causant Insuficiència renal aguda
- Infeccions
- Reactivació del virus de l'hepatitis B
- leucoencefalopatia multifocal progressiva (LMP) causada per la reactivació del virus JC[31]
- Altres infeccions virals
- Toxicitat en el sistema immunitari, ja que destrueix del 70 al 80% de les cèl·lules B dels pacients amb limfoma
- Toxicitat pulmonar, obstrucció i perforació gastrointestinal[32][33]
Dos pacients de lupus eritematós sistèmic van morir per leucoencefalopatia multifocal progressiva (LMP) després del tractament amb rituximab. La LMP és causada per la reactivació del virus JC, un virus comú en el cervell que és normalment latent. La reactivació del virus JC normalment resulta en mort o en dany greu al cervell.[34] Almenys un pacient amb artritis reumatoide va desenvolupar LMP després del tractament amb rituximab.[35]
Se sospita de la contribució del rituximab com un dels cofactors en una infecció crònica per hepatitis E en un pacient de limfoma. Atès que la infecció pel virus de l'hepatitis E és normalment aguda, el medicament combinat amb el limfoma podria haver baixat la resposta immunitària del cos al virus.[36]
Mecanismes d'acció
[modifica]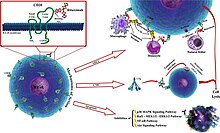

L'anticòs es lliga a la proteïna de la superfície cel·lular CD20. CD20 s'expressa amplament en els limfòcits B, des de les pre-cèl·lules fins a després en la diferenciació, però és absent en els plasmòcits completament diferenciats. Encara que la funció del CD20 és desconeguda, potser que tinga un rol en l'influx de Ca2+ entre les membranes plasmàtiques, mantenint la concentració de calci intracel·lular i permetent l'activació de les cèl·lules B.
El rituximab és relativament inefectiu eliminant les cèl·lules amb nivells baixos de CD20 en la superfície cel·lular. Té una tendència a enganxar-se a un dels costats de les cèl·lules B, on es troba el CD20, formant un tap i atraent les proteïnes a aquest costat. La presència del tap canvia l'efectivitat de les cèl·lules NK en destruir aquestes cèl·lules B. Quan una cèl·lula NK s'enganxa al tap, té un èxit del 80 per cent per a eliminar la cèl·lula. En canvi, quan la cèl·lula B no té aquest clúster de proteïnes asimètric, només era matada un 40% de les vegades.[38][39]
S'han descobert els següents efectes:[40]
- La porció Fc del rituximab media la citotoxicitat mediada per cèl·lules dependents dels anticossos i la citotoxicitat mediada pel complement.
- Rituximab té un efecte regulador general del cicle cel·lular.
- L'eliminació preferencial de les cèl·lules B malignes amb nivells alts de CD20 i una propensió alta de comunicar el gen BCR, especialment en la leucèmia limfocítica crònica (LLC).
- Augmenta el MHC II i les molècules d'adhesió LFA-1 i LFA-3 (antigen associat a la funció del limfòcit).
- Provoca l'expressió de CD23.
- Regula descendent el receptor de la cèl·lula B.
- Indueix l'apoptosi de les cèl·lules CD20+.
L'efecte combinat resulta en l'eliminació de les cèl·lules B (incloent les canceroses) del cos, permetent la generació d'una nova població de cèl·lules B sanes des de les cèl·lules mare limfoides.
El rituximab lliga als aminoàcids 170-173 i 182-185 del CD20, que se situen pròxim entre ells com a resulta d'un lligam de disulfur entre els aminoàcids 167 i 183.[41]
Història
[modifica]El rituximab va ser desenvolupat pels investigadors Nabil Hanna, Mitchell Reff, i els treballadores de l'empresa IDEC Pharmaceuticals amb el nom investigacional de IDEC-C2B8. La patent del medicament als Estats Units es va registrar en 1998 i va expirar en 2015.[42]
Segons la seua seguretat i efectivitat en assajos clínics,[43] el rituximab va ser aprovat per la Food and Drug Administration en 1997 per a tractar el limfoma no hodgkinià de cèl·lules B resistent a altres règims quimioteràpeutics.[44] En combinació amb el règim CHOP és molt superior a només CHOP en el tractament del limfoma difús de cèl·lules B grans i molts altres limfomes de cèl·lules B.[45] L'any 2010 va ser aprovat per la Comissió Europea per a la teràpia de manteniment després del tractament inicial del limfoma fol·licular.[46]
En l'actualitat es comercialitza conjuntament per Biogen i Genentech als EUA, per Hoffmann-La Roche al Canadà i la Unió Europea; per Chugai Pharmaceuticals, Zenyaku Kogyo al Japó i AryoGen en Iran.
L'any 2014 Genentech va reclassificar el Rituxan com un medicament d'especialitat, una mena de medicaments que només es troben disponibles a través de determinats distribuïdors als Estats Units.[47] Com que determinats descomptes ja no hi aplicaven, els hospitals han de pagar-hi més.[47]
Originalment es trobava disponible a través d'injecció intravenosa (amb un temps d'administració de 2.5 hores). En 2016 va adquirir una llicència d'ús subcutani per a la leucèmia limfocítica crònica.[48]
Les patents del medicament van expirar en Europa en febrer de 2013 i als Estats Units en setembre de 2016.[49] Des de novembre de 2018, diversos biosimilars s'han aprovat als EUA, Índia, la Unió Europea, Suïssa, el Japó i Austràlia.[50][49][51]
Investigació
[modifica]Síndrome de la fatiga crònica
[modifica]El rituximab no va millorar els símptomes de pacients amb síndrome de fatiga crònica en un estudi publicat en 2019.[52][53] Un 22% dels participants van patir conseqüències greus.[52] La investigació d'aquest potencial ús es va donar després que dos pacients de càncer tractats amb rituximab milloraren en la fatiga crònica.[54]
Intratecal
[modifica]Per a malalties del SNC, el rituximab es podria administrar per via intratecal i aquesta possibilitat s'està estudiant.[55]
Referències
[modifica]- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 1,8 «Rituximab». The American Society of Health-System Pharmacists. Arxivat de l'original el 27 març 2016.
- ↑ Tandan, Rup; Hehir, Michael K.; Waheed, Waqar; Howard, Diantha B. «Rituximab treatment of miastènia gravis: A systematic review». Muscle & Nerve, 56, 2, 8-2017, p. 185–196. DOI: 10.1002/mus.25597. ISSN: 1097-4598.
- ↑ Singer, O; McCune, WJ «Update on maintenance therapy for granulomatosi amb poliangiïtis and microscopic polyangiitis.». Current Opinion in Rheumatology, 29, 3, 5-2017, p. 248–253. DOI: 10.1097/BOR.0000000000000382.
- ↑ «EBV-Positive Lymphoproliferations of B- T- and NK-Cell Derivation in Non-Immunocompromised Hosts». Pathogens (Basel, Switzerland), 7, 1, 3-2018, p. 28. DOI: 10.3390/pathogens7010028.
- ↑ «Boxed Warning and new recommendations to decrease risk of hepatitis B», 13-01-2017.
- ↑ «Rituximab Use During Pregnancy», 16-12-2019.
- ↑ 7,0 7,1 Bosch, Xavier; Ramos-Casals, Manuel; Khamashta, Munther A. Drugs Targeting B-Cells in malaltia autoimmunes (en anglès). Springer Science & Business Media, 2013, p. 1–4. ISBN 9783034807067.
- ↑ World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization, 2019. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ «Rituximab Biosimilars Shown to Be Safe and Effective». Arxivat de l'original el 15 març 2018.
- ↑ 10,0 10,1 10,2 10,3 «Rituxan- rituximab injection, solution», 06-11-2019.
- ↑ «MabThera SC / Rituxan Hycela (rituximab hyaluronidase)». Arxivat de l'original el 3 d’agost 2020.
- ↑ «Rituxan Hycela- rituximab and hyaluronidase injection, solution», 03-12-2019.
- ↑ «Rituximab in Hodgkin lymphoma: Is the target always a hit?». Cancer Treat Rev, 37, 5, 2011, p. 385–90. DOI: 10.1016/j.ctrv.2010.11.005.
- ↑ «Efficacy of B-cell-targeted therapy with rituximab in patients with rheumatoid arthritis». N Engl J Med, 350, 25, 2004, p. 2572–81. DOI: 10.1056/NEJMoa032534.
- ↑ «Advances in rheumatology: new targeted therapeutics». Arthritis Research & Therapy, 13, Suppl 1, 2011, p. S5. DOI: 10.1186/1478-6354-13-S1-S5.
- ↑ McGinley, MP; Moss, BP; Cohen, JA «Safety of monoclonal antibodies for the treatment of multiple sclerosis.». Expert Opinion on Drug Safety, 16, 1, 1-2017, p. 89–100. DOI: 10.1080/14740338.2017.1250881.
- ↑ He, Dian; Guo, Rui; Zhang, Fubo; Zhang, Chao «Rituximab for relapsing-remitting multiple sclerosis». The Cochrane Database of Systematic Reviews, 12, 06-12-2013, p. CD009130. DOI: 10.1002/14651858.CD009130.pub3. ISSN: 1469-493X.
- ↑ 18,0 18,1 Paul, Marla. «Popular Cancer Drug Linked to Often Fatal 'Brain Eating' Virus». Northwestern University News and Information, 20-05-2009. Arxivat de l'original el 29 maig 2010.
- ↑ (18 desembre 2006). "FDA Warns of Safety Concern Regarding Rituxan in New Patient Population". Nota de premsa.
- ↑ «Rituximab in autoimmune thrombotic thrombocytopenic purpura: A success story.». Eur J Intern Med, 26, 9, 8-2015, p. 659–65. DOI: 10.1016/j.ejim.2015.07.021.
- ↑ «Rituximab chimeric anti-CD20 monoclonal antibody treatment for adult refractory púrpura trombocitopènica idiopàtica». Am. J. Hematol., 78, 4, 4-2005, p. 275–80. DOI: 10.1002/ajh.20276.
- ↑ «Long-term responses seen with rituximab in patients with ITP». Community Oncology, 4, 2, 2007, pàg. 107. Arxivat de l'original el 2007-09-29. DOI: 10.1016/s1548-5315(11)70061-4. Arxivat 2011-07-24 a Wayback Machine.
- ↑ «Rituximab for Immune Cytopenia in Adults: idiopathic thrombocytopenic purpura, Autoimmune Hemolytic Anemia, and Evans Syndrome». Mayo Clinic Proceedings, 78, 11, 2003, pàg. 1340–1346. Arxivat de l'original el 2006-03-13. DOI: 10.4065/78.11.1340. PMID: 14601692. Arxivat 2006-03-13 a Wayback Machine.
- ↑ «Treatment of pèmfig vulgar with Rituximab and Intravenous Immune Globulin». N Engl J Med, 355, 17, 26-10-2006, p. 1772–1779. DOI: 10.1056/nejmoa062930.
- ↑ «Treatment of neuromyelitis optica with rituximab: retrospective analysis of 25 patients». Arch Neurol, 65, 11, 2008, p. 1443–1448. DOI: 10.1001/archneur.65.11.noc80069.
- ↑ «Rituximab Treatment of Patients with Severe, Corticosteroid-Resistant Thyroid-Associated Ophthalmopathy». Arxivat de l'original el 2017-08-22.
- ↑ [2014-05-02] Immunomodulators and Rituximab in the Management of Autoimmune Pancreatitis. DOI 10.3998/panc.2013.20.
- ↑ Pranzatelli, M. R. «Immunologic and Clinical Responses to Rituximab in a Child with Opsoclonus-Myoclonus Syndrome». Pediatrics, 115, 1, 2004, p. e115–9. DOI: 10.1542/peds.2004-0845.
- ↑ Khosroshahi, A.; Wallace, Z. S.; Crowe, J. L.; Akamizu, T. «International Consensus Guidance Statement on the Management and Treatment of IgG4-Related Disease». Arthritis & Rheumatology, 67, 7, 2015, p. 1688–1699. DOI: 10.1002/art.39132.
- ↑ «Persistence of Autoreactive IgA-Secreting B Cells Despite Multiple Immunosuppressive Medications Including Rituximab». JAMA Dermatol, 151, 6, 2015, p. 646–50. DOI: 10.1001/jamadermatol.2015.59.
- ↑ Molloy, Eamonn S.; Calabrese, Leonard H. «leucoencefalopatia multifocal progressiva associated with immunosuppressive therapy in rheumatic diseases: Evolving role of biologic therapies». Arthritis & Rheumatism, 64, 9, 2012, p. 3043–3051. DOI: 10.1002/art.34468.
- ↑ «Interstitial pneumonitis related to rituximab therapy». N Engl J Med, 348, 26, 2003, p. 2690–1; discussion 2690–1. DOI: 10.1056/NEJM200306263482619.
- ↑ «Reports of Bowel Obstruction and Perforation with RITUXAN (rituximab)». Roche Canada, 10-11-2006. Arxivat de l'original el 2014-03-27. [Consulta: 9 febrer 2021].
- ↑ «Rituximab (marketed as Rituxan) Information», 23-07-2015. Arxivat de l'original el 15 novembre 2009.
- ↑ «Rituximab, RA and PML». Arxivat de l'original el 2008-09-16.
- ↑ Kriston, Levente «Challenges in Reporting Meta-analyses of Diagnostic Accuracy Studies». Annals of Internal Medicine, 150, 6, 2009, p. 430. DOI: 10.7326/0003-4819-150-6-200903170-00025.
- ↑ Seyfizadeh, Narges «A molecular perspective on rituximab: A monoclonal antibody for B cell non Hodgkin lymphoma and other affections.». Crit Rev Oncol Hematol, 97, 2016, p. 275–290. DOI: 10.1016/j.critrevonc.2015.09.001.
- ↑ Rudnicka, D.; Oszmiana, A.; Finch, D. K.; Strickland, I. «Scientists discover why a specific cancer drug is so effective». Blood, 121, 23, 2013, p. 4694–4702. Arxivat de l'original el 2013-05-03. DOI: 10.1182/blood-2013-02-482570.
- ↑ Rudnicka, D.; Oszmiana, A.; Finch, D. K.; Strickland, I. «Rituximab causes a polarization of B cells that augments its therapeutic function in NK-cell-mediated antibody-dependent cellular cytotoxicity». Blood, 121, 23, 2013, p. 4694–4702. DOI: 10.1182/blood-2013-02-482570.
- ↑ Shaw, T. «B cell therapy for rheumatoid arthritis: The rituximab (anti-CD20) experience». Annals of the Rheumatic Diseases, 62, 90002, 2003, p. 55ii–59. DOI: 10.1136/ard.62.suppl_2.ii55.
- ↑ Binder M, Otto F, Mertelsmann R, Veelken H, Trepel M. «The epitope recognized by rituximab». Blood, 108, 6, 2006, p. 1975–1978. DOI: 10.1182/blood-2006-04-014639.
- ↑ DrugBank DB00073 Arxivat 2014-01-05 a Wayback Machine.
- ↑ «IDEC-C2B8 (Rituximab) anti-CD20 monoclonal antibody therapy in patients with relapsed low-grade non-Hodgkin's lymphoma». Blood, 90, 6, 9-1997, pàg. 2188–95. Arxivat de l'original el 2020-03-20. DOI: 10.1182/blood.V90.6.2188. PMID: 9310469 [Consulta: 9 febrer 2021].
- ↑ Scott, Shane D. «Rituximab: A New Therapeutic Monoclonal Antibody for Non-Hodgkin's Lymphoma». Cancer Practice, 6, 3, 1998, p. 195–197. DOI: 10.1046/j.1523-5394.1998.006003195.x.
- ↑ Harrison's Principles of Internal Medicine, Longo et al. McGraw Hill Medical 2011 page 931
- ↑ «Roche Gets EC Nod for Follicular Lymphoma Maintenance Therapy». , 29-10-2010.
- ↑ 47,0 47,1 Saporito, Bill. «Hospitals Furious at Cancer-Drug Price Hikes». Time, 27-10-2014. Arxivat de l'original el 20 octubre 2015.
- ↑ «EU approves second indication for subcutaneous form of Roche's rituximab». Arxivat de l'original el 2016-06-07.
- ↑ 49,0 49,1 «Biosimilars of Rituximab» (en anglès britànic). Generics and Biosimilars Initiative, 14-04-2017. Arxivat de l'original el 2017-03-31.
- ↑ (28 novembre 2018). "FDA approves first biosimilar for treatment of adult patients with non-Hodgkin's lymphoma". Nota de premsa.
- ↑ ; Osterman, Cynthia «Novartis abandons effort for U.S. approval of biosimilar rituximab». Reuters, 02-11-2018.
- ↑ 52,0 52,1 Fluge, Øystein; Rekeland, Ingrid G.; Lien, Katarina; Thürmer, Hanne «B-Lymphocyte Depletion in Patients With Myalgic Encephalomyelitis/Chronic Fatigue Syndrome: A Randomized, Double-Blind, Placebo-Controlled Trial» (en anglès). Annals of Internal Medicine, 170, 9, 02-04-2019, p. 585–593. DOI: 10.7326/M18-1451. ISSN: 0003-4819.
- ↑ Tucker, Miriam E. «Rituximab Fails to Improve Symptoms in ME/CFS», 02-04-2019.
- ↑ Castro-Marrero, Jesus; Sáez-Francàs, Naia; Santillo, Dafna; Alegre, Jose «Treatment and management of chronic fatigue syndrome/myalgic encephalomyelitis: All roads lead to Rome». British Journal of Pharmacology, 174, 5, 2017, p. 345–369. DOI: 10.1111/bph.13702.
- ↑ Bonnan, M; Ferrari, S; Bertandeau, E; Demasles, S «Intrathecal rituximab therapy in multiple sclerosis: review of evidence supporting the need for future trials.». Current Drug Targets, 15, 13, 2014, p. 1205–14. DOI: 10.2174/1389450115666141029234644.
Enllaços externs
[modifica]- «Rituximab». Drug Information Portal. U.S. National Library of Medicine.
- «Hyaluronidase mixture with Rituximab». Drug Information Portal. U.S. National Library of Medicine.
- «Rituximab and Hyaluronidase (Professional Patient Advice)».
- «Rituximab and Hyaluronidase Human Injection».