Beta-laktam
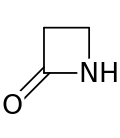
Beta-laktamy (β-laktamy) jsou organické sloučeniny, které ve svých molekulách mají čtyřčlenný laktamový cyklus.[1] Pojmenování vychází ze skutečnosti, že formálně vzniká cyklizací β-aminokyseliny. Nejjednodušším β-laktamem je azetidin-2-on.
Klinický význam
[editovat | editovat zdroj]Beta-laktamový kruh je součástí struktury některých skupin antibiotik jako jsou peniciliny, cefalosporiny, karbapenemy a monobaktamy, které se souhrnně nazývají beta-laktamová antibiotika. Téměř všechna tato antibiotika fungují na principu inhibice biosyntézy v buněčné stěně bakterie, což má pro bakterii smrtící účinek; každá populace bakterií ovšem obvykle obsahuje skupinu, která je vůči β-laktamovým antibiotikům odolná. Antibiotická rezistence se objevuje jako důsledek exprese jednoho z mnoha beta-laktamázových genů. V různých druzích bakterií bylo nalezeno více než 1 800 beta-laktamázových enzymů.[2] Tyto enzymy se značně liší v chemické struktuře a katalytické účinnosti.[3] Pokud populace bakterií obsahuje tyto odolné skupiny, léčba β-laktamy může vést ke zvýšení četnosti odolných kmenů a tím i jejich nebezpečnosti.
Historie
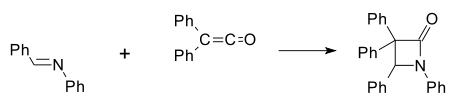
[editovat | editovat zdroj]První syntetický beta-laktam připravil roku 1907 Hermann Staudinger reakcí Schiffovy báze anilinu a benzaldehydu s difenylketenem[4][5] [2+2] cykloadicí (Ph označuje fenylovou funkční skupinu):
Do roku 1970 byl výzkum beta-laktamů zaměřen především na peniciliny a cefalosporiny, poté však byla popsána řada dalších struktur.[6]
Výroba
[editovat | editovat zdroj]K výrobě beta-laktamů se používá Breckpotova syntéza, tedy cyklizace aminokyselin za použití Grignardových činidel[7]:
Reaktivita
[editovat | editovat zdroj]Kvůli úhlovému napětí jsou β-laktamy mnohem snáze hydrolyzovatelné než větší laktamy nebo lineární amidy. Toto napětí se zvyšuje připojením dalšího cyklu, jak je tomu ve většině β-laktamových antibiotik, což je způsobeno omezením amidového charakteru β-laktamu kvůli aplanaritě (nerovinnosti) systému. Dusíkový atom ideálního amidu má sp2 hybridizované orbitaly kvůli rezonanci a molekuly s sp2 hybridizované atomy mají tvar trojúhelníku. Pokud úhlové napětí narušuje tuto strukturu, rezonance amidové vazby se snižuje a karbonylová skupina získává více ketonový charakter. Nositel Nobelovy ceny Robert Burns Woodward popsal parametr h jako jednotku výšky trigonální pyramidy určené dusíkem (ve vrcholu) a třemi připojenými atomy. h odpovídá síle β-laktamové vazby, kde menší hodnota (planárnější tvar molekuly, blíže k ideálnímu amidu) znamená silnější vazbu a menší reaktivitu sloučeniny.[8] Monobaktamy mají hodnoty h mezi 0,05 a 0,10 Å. U cefemů je to 0,20–0,25 Å. Penemy mají hodnoty v rozmezí 0,40–0,50 Å, zatímco karbapenemy a klavamy 0,50–0,60 Å a jsou tak z β-laktamů nejnáchylnější k hydrolýze.[9]
Ostatní použití
[editovat | editovat zdroj]Nové studie ukázaly, že beta-laktamy mohou podstoupit polymerizaci za otevření kruhu, čímž vznikají amidové vazby, které utváří 3-nylonové polymery. Hlavní řetězce těchto polymerů jsou stejné jako u peptidů, což jim dává biologickou funkčnost. Tyto 3-nylonové polymery mohou napodobovat antimikrobiální peptidy.
Odkazy
[editovat | editovat zdroj]Související články
[editovat | editovat zdroj]Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Beta-lactam na anglické Wikipedii.
- ↑ GILCHRIST, T. Heterocyclic Chemistry. Harlow: Longman Scientific, 1987. ISBN 0-582-01421-2.
- ↑ BRANDT, C. In silico serine β-lactamases analysis reveals a huge potential resistome in environmental and pathogenic species. SciRep. 2017. Dostupné online. doi:10.1038/srep43232. Bibcode 2017NatSR...743232B.
- ↑ EHMANN, David E. Avibactam is a covalent, reversible, non-β-lactam β-lactamase inhibitor. PNAS. 2012, s. 11663–11668. doi:10.1073/pnas.1205073109. Bibcode 2012PNAS..10911663E.
- ↑ Tidwell, Thomas T. Hugo (Ugo) Schiff, Schiff Bases, and a Century of β-Lactam Synthesis. Angewandte Chemie International Edition. 2008, s. 1016–20. doi:10.1002/anie.200702965. PMID 18022986.
- ↑ Hermann Staudinger. Zur Kenntniss der Ketene. Diphenylketen. Justus Liebigs Ann. Chem.. 1907, s. 51–123. doi:10.1002/jlac.19073560106.
- ↑ FLYNN, E.H. Cephalosporins and Penicillins : Chemistry and Biology. New York and London: Academic Press, 1972.
- ↑ [1]
- ↑ WOODWARD, R.B. Penems and related substances. Phil Trans Royal Soc Chem B. 1980, s. 239–50. doi:10.1098/rstb.1980.0042. PMID 6109320. Bibcode 1980RSPTB.289..239W.
- ↑ NANGIA, A.; BIRADHA, K.; DESIRAJU, G.R. Correlation of biological activity in β-lactam antibiotics with Woodward and Cohen structural parameters: A Cambridge database study. J Chem Soc, Perkin Trans. 1996, s. 943–53. doi:10.1039/p29960000943.