Nitrony
Nitrony jsou organické sloučeniny obsahující nitronovou funkční skupinu R1R2C=NR +
3 O− (přičemž R3 není vodík); jedná se o N-oxidy iminů. Nitrony mají 1,3-dipolární molekuly a díky tomu se používají k provádění 1,3-dipolárních cykloadicí. Dále mohou podstoupit [3+3] cykloadice za vzniku šestičlenných cyklů i [5+2] cykloadice, při kterých se utváří sedmičlenné cykly.[1] Nitrony by neměly být zaměňovány s nitreny.
Vznik
[editovat | editovat zdroj]Nitrony se nejčastěji připravují oxidací hydroxylaminů či kondenzací monosubstituovaných hydroxylaminů s karbonylovými sloučeninami (ketony nebo aldehydy). K oxidaci se obvykle používá oxid rtuťnatý[2]

Využitím kondenzace karbonylových sloučenin lze omezit vedlejší reakce.[3]

U mnoha nitronů dochází k dimerizaci,[4] které je možné zamezit použitím nadbytku nitronu nebo zvýšením teploty.
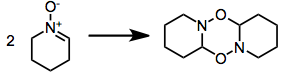
Reakce
[editovat | editovat zdroj]Jelikož jsou nitrony 1,3-dipolární látky, tak mohou podstoupit 1,3-dipolární cykloadice.[1] Při reakci nitronu s alkenem jako dipolarofilem vzniká isoxazolidin:

Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Nitrone na anglické Wikipedii.
- ↑ a b YANG, Jiong. Recent Developments in Nitrone Chemistry. Synlett. 2012, s. 2293-97. doi:10.1055/s-0032-1317096.
- ↑ THIESING, Jan; MAYER, Hans. Cyclische Nitrone, II. Über die Polymeren des 2.3.4.5-Tetrahydro-pyridin-N-oxyds und verwandte Verbindungen. Justus Liebigs Annalen der Chemie. 1957, s. 46-57. doi:10.1002/jlac.19576090105.
- ↑ EXNER, O. A New Synthesis of N-methylketoximes. Collection of Czechoslovak Chemical Communications. 1951, s. 258-267. doi:10.1135/cccc19510258.
- ↑ THIESING, Jan; MAYER, Hans. Cyclische Nitrone I: Dimeres 2.3.4.5-Tetrahydro-pyridin-N-oxyd. Chemische Berichte. 1956, s. 2159-2167. doi:10.1002/cber.19560890919.
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Nitrony na Wikimedia Commons
Obrázky, zvuky či videa k tématu Nitrony na Wikimedia Commons