Chlorophylle


Chlorophylle (Plural von Chlorophyll ‚grüner Blattfarbstoff‘, von altgriechisch χλωρός chlōrós „hellgrün, frisch“ und φύλλον phýllon „Blatt“) oder Blattgrün bezeichnet eine Klasse natürlicher Farbstoffe, die von Organismen gebildet werden, die Photosynthese betreiben. Insbesondere Pflanzen erlangen ihre grüne Farbe durch Chlorophylle.
Pflanzen, Algen und Cyanobakterien besitzen verschiedene Chlorophylltypen, photosynthesetreibende Bakterien verschiedene Typen von Bacteriochlorophyll.
Struktur und Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
Bei chromatographischer Trennung der Blattpigmente aus einem Extrakt sind Chlorophyll a und Chlorophyll b als getrennte Banden mit etwas unterschiedlichem Grünton zu erkennen.[2] Chlorophylle sind Chelat-Komplexe genannte Molekularstrukturen, bestehend aus einem derivatisierten Porphyrin-Ring und Mg2+ als Zentralion. Im Unterschied zum Porphyrin enthält das Grundgerüst der Chlorophylle einen weiteren, fünften Ring an Ring III (Nummerierung nach Fischer). Je nach Art des Chlorophylls sind an den Grundkörper verschiedene Seitenketten angehängt. So ist beispielsweise Chlorophyll a mit Phytol verestert (vgl. Tabelle). Chlorophyllide sind Chlorophylle ohne Seitenketten.[3]
Strukturell sind die Chlorophylle mit den Hämen verwandt, welche als Bestandteil des Blutfarbstoffs (Hämoglobin), des Myoglobins und der Cytochrome auftreten, als Zentralion jedoch nicht Magnesium, sondern Eisen enthalten. Chlorophylle sind gut löslich in Ethanol und Aceton sowie in ähnlichen Lösungsmitteln. Läuft die Photosynthese bei Lebewesen ab, die Sauerstoff freisetzen (oxygene Phototrophe), spricht man allgemein von Chlorophyll. Anoxygene Phototrophe erzeugen jedoch nicht Sauerstoff als Reaktionsprodukt bei der Photosynthese, bei diesen Organismen bezeichnet man das Chlorophyll als Bakteriochlorophyll.
Hans Fischer ermittelte 1940 die Molekülstruktur von Chlorophyll, die absolute Konfiguration wurde 1967 von Ian Fleming aufgeklärt.[4]
Chemische Struktur bei oxygenen Phototrophen
[Bearbeiten | Quelltext bearbeiten]| Name | Struktur | C2-Rest | C3-Rest | C7-Rest | C8-Rest | C17-Rest | C17-18-Bindung | Summenformel |
|---|---|---|---|---|---|---|---|---|
| Chlorophyll a | –CH3 | –CH=CH2 | –CH3 | –CH2CH3 | –CH2CH2COO-Phytyl | Einfachbindung | C55H72O5N4Mg | |
| Chlorophyll b | –CH3 | –CH=CH2 | –CHO | –CH2CH3 | –CH2CH2COO-Phytyl | Einfachbindung | C55H70O6N4Mg | |
| Chlorophyll c1 | –CH3 | –CH=CH2 | –CH3 | –CH2CH3 | –CH=CHCOOH | Doppelbindung | C35H30O5N4Mg | |
| Chlorophyll c2 | –CH3 | –CH=CH2 | –CH3 | –CH=CH2 | –CH=CHCOOH | Doppelbindung | C35H28O5N4Mg | |
| Chlorophyll d | –CH3 | –CHO | –CH3 | –CH2CH3 | –CH2CH2COO-Phytyl | Einfachbindung | C54H70O6N4Mg | |
| Chlorophyll f | –CHO | –CH=CH2 | –CH3 | –CH2CH3 | –CH2CH2COO-Phytyl | Einfachbindung | C55H70O6N4Mg |
 |
 |
 |
Chemische Struktur bei anoxygenen Phototrophen: Bakteriochlorophylle (Bchl)
[Bearbeiten | Quelltext bearbeiten]a: Keine Doppelbindung zwischen C7 und C8 (farblich markiert im Bild)
b: Bei Bchl c, d und e handelt es sich um ein Gemisch von Isomeren, bei denen der Rest R3 oder R4 unterschiedlich substituiert ist.

Spektrale Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
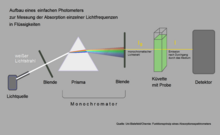

Welches Licht vom Chlorophyll besonders stark absorbiert wird, kann man mit einem einfach gebauten Absorptionsspektrometer messen. In diesem Beispiel ist die Blende so platziert, dass gelbes Licht in die Küvette mit der Chlorophyll-Lösung fällt. Die Menge des auf der anderen Seite der Küvette austretenden gelben Lichts unterschreitet die Menge an einfallendem Licht kaum, weil im Bereich dieser Wellenlängen vom Chlorophyll kaum etwas absorbiert wurde. Verschiebt man die Blende so, dass rotes oder blaues Licht hindurch dringt, misst der Detektor hinter der Küvette eine wesentlich geringere Emission.
Die Absorptionsspektren von in Lösungsmitteln gelösten Chlorophyllen besitzen immer zwei ausgeprägte Absorptionsmaxima, eines zwischen 600 und 800 nm, das als Qy-Bande bezeichnet wird, und eines um 400 nm, das Soret-Bande genannt wird. Die Abbildung rechts zeigt diese Absorptionsmaxima für Chlorophyll a und b. Zusätzlich existiert die Qx-Bande um 580 nm, die senkrecht zu Qy polarisiert ist und in der Regel sehr schwach absorbiert. Für Chlorophyll a ist sie in der Abbildung noch zu erkennen, für Chlorophyll b verschwindet sie im Untergrund. Der zwischen den Banden liegende Bereich wird als Grünlücke bezeichnet.
Anhand der Spektren in der Abbildung kann man leicht verstehen, warum Blätter – diese enthalten Chlorophyll a und b – grün sind. Zusammen absorbieren Chlorophyll a und b hauptsächlich im blauen Spektralbereich (400–500 nm) sowie im roten Spektralbereich (600–700 nm). Im grünen Bereich hingegen findet keine Absorption statt, so dass grünes Licht gestreut wird, was Blätter grün erscheinen lässt.

Die Absorption ist abhängig vom Lösungsmittel und dementsprechend kann die Lage der Absorptionsmaxima je nach Art des Lösungsmittels um einige wenige Nanometer variieren. In der natürlichen Umgebung von Chlorophyllen, also der Proteinumgebung, sieht das anders aus. Hier hängt die Lage der Absorptionsmaxima von zwei Faktoren ab: (1) Je nach Partialladung der umgebenden Aminosäuren und Verbiegung der Seitengruppen der Chlorophyllmoleküle können die Absorptionsmaxima bei stark unterschiedlichen Wellenlängen liegen. (2) In Proteinen kommen sich Chlorophylle sehr nahe, sodass sie eine Wechselwirkung aufeinander ausüben (Dipol-Dipol-Wechselwirkung; bei sehr geringen Abständen auch Austauschwechselwirkung). Diese Wechselwirkung führt zu einer Absenkung der Energieniveaus und damit zu einer Rotverschiebung der Absorptionsmaxima. Dies kann man besonders eindrucksvoll am Beispiel des Antennenkomplexes LH2 von Purpurbakterien sehen. Der LH2-Komplex besteht aus zwei ringförmig angeordneten Gruppen von Bacteriochlorophyllmolekülen (siehe Abbildung). Der obere Ring (B850) enthält 18 BChl a-Moleküle, die in sehr geringen Abständen voneinander liegen, also stark gekoppelt sind. Der untere Ring (B800) besteht aus 9 BChl a-Molekülen, die deutlich weiter voneinander entfernt liegen und somit viel schwächer gekoppelt sind.
Durch die starke Kopplung wird die Absorption von BChl a im B850-Ring zu Rot verschoben. Die Absorptionsbande liegt bei 850 nm. Die schwachgekoppelten BChl a des B800-Rings absorbieren hingegen bei 800 nm, also ungefähr im gleichen Bereich wie in Lösungsmittel gelöste BChl a-Moleküle. Im Absorptionsspektrum (Abbildung rechts) des LH2-Komplexes sind die Absorptionsbanden der B800- und der B850-BChl-a-Moleküle deutlich getrennt. Zusätzlich werden Banden dargestellt, die von Carotinoidmolekülen stammen, diese sind in der Struktur nicht eingezeichnet.


Typen
[Bearbeiten | Quelltext bearbeiten]Es gibt verschiedene Typen von Chlorophyll, die sich in den Seitengruppen des Porphyrins unterscheiden. Sie besitzen verschiedene Absorptionsspektren und kommen bei verschiedenen phototrophen Organismen vor:
| Chlorophylltyp | Farbe | Absorptionsmaxima (in nm)[6] |
Vorkommen |
|---|---|---|---|
| Chlorophyll a | blaugrün | 430, 662 (in Aceton) | Cyanobakterien und alle phototrophen Eukaryoten |
| Chlorophyll b | gelbgrün | 454, 643 (in Diethylether) | Grünalgen (Chlorophyta), Euglenozoa und alle Landpflanzen |
| Chlorophyll c | grün | 444, 576, 626 | an Stelle von Chlorophyll b bei Braunalgen (Phaeophyta)[7], Kieselalgen (Bacillariophyta)[7], Goldalgen (Chrysophyta), Gelbgrüne Algen (Xanthophyta), Haptophyta, Dinophyta und Raphidophyceae |
| Chlorophyll d | 447, 688 | Cyanobakterium Acaryochloris marina | |
| Chlorophyll f | 706 | Cyanobakterien (z. B. Ordnung Nodosilineales[8]), zuerst gefunden in westaustralischen Stromatolithen[9][10] | |
| Bacteriochlorophyll a | grün | 358, 577, 773 (in Aceton) | Purpurbakterien[11] (Rhodospirillaceae, Chromatiaceae) |
| Bacteriochlorophyll b | 368, 580, 794 (in Aceton) | Schwefelpurpurbakterien (Chromatiaceae); Purpurbakterien[11] | |
| Bacteriochlorophyll c | grün | 432, 660 (in Aceton?) | Grüne Schwefelbakterien[11] (Chlorobiaceae) |
| Bacteriochlorophyll cs | 740[11] (in vivo) | Grüne Nichtschwefelbakterien[11] (Chloroflexaceae) | |
| Bacteriochlorophyll d | 458, 646 (in was?) 427, 654 (in Aceton) | Grüne Schwefelbakterien[11] (Chlorobiaceae) | |
| Bacteriochlorophyll e | 424, 654 (in was?) 462, 649 (in Aceton) | Grüne Schwefelbakterien[11] (Chlorobiaceae) | |
| Bacteriochlorophyll g | 408, 418, 470, 575, 763 (in was?) 412, 788 (in vivo) | Heliobacteria[11] |
Biosynthese
[Bearbeiten | Quelltext bearbeiten]


Chlorophyll wird bei Eukaryoten in den Chloroplasten synthetisiert, bei Prokaryoten im Cytoplasma. Bei vielen Phototrophen wird die Chlorophyll-Bildung durch Licht induziert und bleibt ohne Belichtung aus. Die Biosynthese besteht aus einer Reihe zahlreicher Schritte mit einer entsprechenden Anzahl spezifischer Enzyme.[12]
Die Synthese dieses und anderer Tetrapyrrole ist ein mehrstufiger Prozess, der verschiedene Verzweigungspunkte aufweist. Die Biosynthese geht von L-Glutamat aus und endet in einem Sirohäm-, einem Häm- und einem Chlorophyll-Zweig.
Nach mehreren Schritten wird aus L-Glutamat Uroporphyrinogen III gebildet, dem ersten Verzweigungspunkt, aus dem Sirohäm gebildet werden kann. Uroporphyrinogen III wird dann in drei Schritten zu Protoporphyrin IX umgesetzt, was den zweiten Verzweigungspunkt zu den Hämen darstellt. In Protoporphyrin IX wird bei einer ATP-abhängigen Reaktion das Magnesiumion eingeführt, was eine Magnesium-Chelatase (EC 6.6.1.1) katalysiert. Das hierbei gebildete Mg-Protoporphyrin IX wird über Mg-Protoporphyrin IX-Monoethylester zu Divinyl-Protochlorophyllid a umgesetzt. Jenen Schritt katalysiert eine Cyclase, die den fünften Ring in Chlorophyll einführt. In Pflanzen ist dieses Enzym O2-abhängig, während es bei Prokaryonten sowohl O2-abhängige als auch -unabhängige Cyclasen gibt.
Im nächsten Schritt wird der D-Ring des Protochloropylls durch eine Oxidoreduktase (EC 1.3.1.33) zu Divinyl-Chlorophylid a reduziert. In Angiospermen ist diese Reaktion absolut lichtabhängig. Daher bilden Keimlinge erst dann Chlorophyll, wenn sie dem Licht ausgesetzt sind.[13] Andere Pflanzen (einige Gymnospermen), Algen, aber auch Cyanobakterien haben sowohl eine lichtabhängige als auch lichtunabhängige Oxidoreduktase. Infolgedessen können diese Organismen Chlorophyll auch im Dunkeln synthetisieren. Divinyl-Chlorophylid a wird durch eine Reduktase zu Monovinyl-Chlorophylid a reduziert, bevor dieses in einem letzten Schritt mittels Phytolphosphat zu Chlorophyll a verestert wird. Diesen terminalen Schritt katalysiert eine Chlorophyll-Synthase, eine Prenyltransferase (EC 2.5.1.62).
Aus Chlorophyll a kann auch Chlorophyll b oder umgekehrt gebildet werden.
Abbau von Chlorophyll
[Bearbeiten | Quelltext bearbeiten]
Der Abbau des Chlorophylls in Laubbäumen im Herbst erzeugt charakteristische Veränderungen der Färbung der Blätter.[14] Auch beim Verwelken kann es zum Chlorophyllabbau kommen. Der Chlorophyllabbau in Laubblättern zählt zu den Seneszenzerscheinungen bei Pflanzen. Das Chlorophyll wird durch die Chlorophyllase zu Chlorophyllid verstoffwechselt.[15] Anschließend erfolgt ein Ionenaustausch durch die Mg2+-Dechelatase zu Phäophorbid.[15] Phäophorbid wird durch die Phäophorbid-A-Oxygenase mit dem Cofaktor Ferredoxin oxidiert, wodurch die Grünfärbung verschwindet und zuerst verschiedene fluoreszente Abbauprodukte (FCC, von engl. fluorescent chlorophyll catabolites) und im weiteren Abbau nichtfluoreszente Stoffe (NCC) entstehen.[15] In Spitzahorn wird Chlorophyll über einen anderen Abbauweg zu Dioxobilan abgebaut.[14]
Bedeutung in der Photosynthese
[Bearbeiten | Quelltext bearbeiten]Chlorophylle haben innerhalb der Photosynthese im Photosystem I sowie im Photosystem II mehrere Aufgaben. Der mit Abstand größte Anteil dient der Lichtabsorption und der Weiterleitung der absorbierten Energie. Sie wirken also als Photosensibilisatoren. Hierzu sind die Chlorophyllmoleküle in Lichtsammelkomplexen organisiert, die so angeordnet sind, dass einerseits eine möglichst große absorbierende Fläche gebildet wird und andererseits ein energetischer Trichter entsteht, der die absorbierte Energie zum sogenannten Reaktionszentrum leitet. Im Reaktionszentrum dienen zwei Chlorophylle als Akzeptor dieser Energie. Sie sind so speziell angeordnet, dass ihre Anregung zu einer Ladungstrennung führt, die als erster Schritt der eigentlichen Photosynthese betrachtet werden kann. Dieses Chlorophyllpaar wird im Englischen als special pair bezeichnet.
Bei den sehr verschiedenen photosynthesebetreibenden Organismen gibt es vielfältige Unterschiede in der Struktur der Lichtsammelkomplexe, das Reaktionszentrum hingegen ist immer nahezu gleich strukturiert. Das special pair wird bei Pflanzen, Algen und Cyanobakterien immer von Chlorophyll a, bei Bakterien von verschiedenen Bakteriochlorophyllen gebildet.
Vorkommen in Lebensmitteln
[Bearbeiten | Quelltext bearbeiten]Der Chlorophyllgehalt ist vor allem in grünem Gemüse hoch. Der Chlorophyll a- und b-Gehalt von Gemüse und Obst je 100 g Frischsubstanz ist in folgender Tabelle geordnet nach absteigendem Chlorophyll a-Gehalt aufgeführt:[7]
| Chlorophyll a | Chlorophyll b | |
|---|---|---|
| Grünkohl | 189 mg | 41 mg |
| Große Brennnessel | 185 mg | 173 mg |
| Petersilie | 157 mg | 55 mg |
| Spinat | 95 mg | 20 mg |
| Broccoli | 26 mg | 6 mg |
| grüne Bohnen | 12 mg | 4 mg |
| grüne Erbsen | 10 mg | 2 mg |
| Gurke | 6 mg | 2 mg |
| Kiwis | 1,7 mg | 0,4 mg |
| Weißkohl | 0,3–1 mg | 0,1–0,2 mg |
Studien belegen, dass sekundäre Pflanzenstoffe menschliche Stoffwechselvorgänge positiv beeinflussen. Das gilt für Chlorophyll genauso wie für Flavonoide und Carotinoide.[16]
Verwendung als Lebensmittelzusatzstoff
[Bearbeiten | Quelltext bearbeiten]In Deutschland wurde Chlorophyll durch die Farbstoff-Verordnung ab 1959 für die Verwendung als Lebensmittelfarbstoff zugelassen.[17] Zur Übernahme der Richtlinie des Rats zur Angleichung der Rechtsvorschriften der Mitgliedstaaten für färbende Stoffe, die in Lebensmitteln verwendet werden dürfen in nationales Recht wurde die Farbstoff-Verordnung 1966 angepasst und für Chlorophyll (C.I. Natural Green 3) die E-Nummer E 140[18] aufgenommen.[19] Ab 1978 wurde die Verwendung in Deutschland durch die Zusatzstoff-Zulassungsverordnung geregelt. Durch die Verordnung (EG) Nr. 1333/2008, die am 20. Januar 2009 in Kraft trat, ist die Verwendung von Chlorophyll als Lebensmittelzusatzstoff im ganzen EWR einheitlich geregelt.[20][21] Chlorophyll kann dabei ohne Mengenbegrenzung zugegeben werden (quantum satis).[20]
Medizinische Verwendung
[Bearbeiten | Quelltext bearbeiten]Chlorophyll oder Chlorophyll-Derivate werden auch als Arzneistoff verwendet, so bereits in den 1950er Jahren etwa im Rein-Chlorophyll/Mistel-Extrakt Viscophyll bei Altershochdruck und Arteriosklerose[22] sowie in Wundtherapeutika wie dem wundreinigend und desodorierend wirkenden Cenat (ursprünglich das Versuchspräparat MS 109 von Dr. Madaus & Co.),[23] Vulnophyll oder dem Wundstreupulver Ulcophyll. Eugen Roth schrieb um 1933 in seinem Gedicht Entdeckung: „[…] Und durch die Welt geht’s mit Gebrüll, Heilkraft entdeckt im Chlorophyll!“ Die perorale Desodoration durch ein bestimmte proteoloytische Endoenzyme hemmendes Chlorophyll-Derivat wurde von A. Albrecht 1952 in seiner in Mainz vorgelegten Dissertation am Bacillus proteus chemisch und papierchromatographisch nachgewiesen. Durch die Fermentblockierung kommt es demnach zu einer Hemmung der Schwefelwasserstoff- und Ammoniak-Entwicklung.[24] Wegen dieser geruchsneutralisierenden Wirkung ist Chlorophyll in Drageeform in Apotheken erhältlich als Mittel gegen Mund- und Körpergeruch.
Geschichte
[Bearbeiten | Quelltext bearbeiten]Erste Beschreibungen eines „Farbstoffes“, der durch Ethanol („Weingeist“) extrahiert werden kann und unter Lichteinfluss zersetzt wird, finden sich bei Heinrich Friedrich Link in seinem Buch „Grundlehren der Anatomie und Physiologie der Pflanzen“, Göttingen 1807. Ebenso findet man uneindeutige Nachweise, dass Joseph Louis Proust den grünen Farbstoff als „Fécule“ beschrieben hat. Pierre Joseph Pelletier und Joseph Bienaimé Caventou extrahierten den Stoff erneut und nannten ihn Chlorophyll.[25] Erste Studien über die chemische Struktur des Chlorophylls stammen von Richard Willstätter (1913). Der Chemiker Hans Fischer nahm Willstätters Forschungen in den 1930er Jahren wieder auf, 1940 konnte er die Struktur des Moleküls aufklären. Auch Emil Bürgi gehörte zu den Pionieren der Chlorophyll-Forschung.[26] Fischers Forschungsergebnisse wurden 1960 durch Robert B. Woodwards Chlorophyllsynthese bestätigt. Schon vor Woodward gelang die Totalsynthese einer Gruppe von Chemikern an der ehemaligen Wirkungsstätte von Fischer (TU München) auf etwas anderem Weg. Fischers ehemalige Mitarbeiter Alfred Treibs und Martin Strell setzten dort dessen Arbeiten zur Totalsynthese von Chlorophyll fort.[27] Ziel beider Gruppen war die Synthese von Phäophorbid a, da Willstätter von diesem ausgehend die Restsynthese schon beschrieben hatte.[28]
Sonstiges
[Bearbeiten | Quelltext bearbeiten]Eine wichtige Eigenschaft des Chlorophylls ist die Chlorophyllfluoreszenz. Sie wird vor allem zum Bestimmen des Chlorophyllgehalts und dessen Aktivität sowie für andere wissenschaftliche Analysen genutzt.
Siehe auch
[Bearbeiten | Quelltext bearbeiten]- Lichtsammelkomplex
- Engelmannscher Bakterienversuch
- Liste der E-Nummern
- Liste der Lebensmittelzusatzstoffe
Literatur
[Bearbeiten | Quelltext bearbeiten]- Hans W. Heldt, Birgit Piechulla: Pflanzenbiochemie. 4. Auflage. Spektrum Akademischer Verlag, 2008, ISBN 978-3-8274-1961-3.
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biochemie. 6. Auflage. Spektrum Akademischer Verlag, Heidelberg 2007, ISBN 978-3-8274-1800-5.
- R. Tanaka, A. Tanaka: Tetrapyrrole biosynthesis in higher plants. In: Annu Rev Plant Biol, Band 58; 2007, S. 321–346; doi:10.1146/annurev.arplant.57.032905.105448, PMID 17227226 (englisch).
- Lígia Fonseca Coelho, Lisa Kaltenegger, Stephen Zinder, William Philpot, Taylor L. Price, Trinity L. Hamilton: Purple is the new green: biopigments and spectra of Earth-like purple worlds. In: Monthly Notices of the Royal Astronomical Society, Band 530, Nr. 2, May 2024, S. 1363–1368; doi:10.1093/mnras/stae601, Epub: 16. April 2024 (englisch). Dazu:
- Michelle Starr: Purple Planets Could Be The Signs of Alien Life We've Been Looking For. Auf: sciencealert vom 21. April 2024.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Stoffwechselweg für die Bildung von Chlorophyll und Häm bei KEGG-Enzyme
- Absorptionsspektren der Oregon University of Health & Sciences
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ S. W. Jeffrey: Paper-chromatographic separation of chlorophylls and carotenoids from marine algae. In: The Biochemical journal, Band 80, August 1961, S. 336–342; doi:10.1042/bj0800336, PMID 13789753, PMC 1244004 (freier Volltext) (englisch).
- ↑ The colour of leaves. Encyclopedia of the environment. Université Grenoble Alpes, 12. Juli 2022.
- ↑ Andreas Bresinsky, Christian Körner, Joachim W. Kadereit, G. Neuhaus, Uwe Sonnewald: Strasburger – Lehrbuch der Botanik. 36. Auflage, Spektrum Akademischer Verlag, Heidelberg 2008, S. 277, S. 315, ISBN 978-3-8274-1455-7.
- ↑ Ian Fleming: Absolute Configuration and the Structure of Chlorophyll, Nature 1967, 216, 151–152 doi:10.1038/216151a0.
- ↑ Hyperphysics: Spectral Colors
- ↑ Hugo Scheer (Editor): Chlorophylls. CRC Press, 1991. ISBN 0-8493-6842-1.
- ↑ a b c Gerhard G. Habermehl, Peter E. Hammann, Hans C. Krebs, W. Ternes: Naturstoffchemie. Eine Einführung. 3. Auflage. Springer, Berlin 2008, ISBN 978-3-540-73732-2, S. 530.
- ↑
Christopher J. Gisriel, Donald A. Bryant, Gary W. Brudvig, Tanai Cardona: Molecular diversity and evolution of far-red light-acclimated photosystem I. In: Frontiers in Plant Science, Band 14, 20. November 2023, Sec. Photosynthesis and Photobiology; doi:10.3389/fpls.2023.1289199 (englisch). Dazu:
- A spectrum of possibilities: insights into the evolution of far-red light photosynthesis. Auf: EurekAlert! vom 28. November 2023.
- ↑ M. Chen, M. Schliep, R.D. Willows, Z.-L. Cai, B.A. Neilan, H. Scheer: A red-shifted chlorophyll. In: Science. 329. Jahrgang, Nr. 5997, 2010, S. 1318–1319, doi:10.1126/science.1191127, PMID 20724585, bibcode:2010Sci...329.1318C (englisch).
- ↑ Ferris Jabr: A new form of chlorophyll? In: Scientific American, 19. August 2010. Abgerufen am 28. November 2023 (englisch).
- ↑ a b c d e f g h Michael T. Madigan, John M. Martinko: Brock – Mikrobiologie. 11. Auflage. Pearson Studium, München / Boston u.a. 2009, ISBN 978-3-8273-7358-8, S. 607 (englisch: Brock biology of microorganisms. Übersetzt von Thomas Lazar, Freya Thomm-Reitz).
- ↑ Samuel I. Beale: Enzymes of chlorophyll biosynthesis (Übersichtsartikel). In: Photosynthesis Research. Bd. 60, 1999. S. 43–73. Hier die Darstellung des Biosynthese-Wegs.
- ↑ Hans W. Heldt, Birgit Piechulla: Pflanzenbiochemie. 4. Auflage. Spektrum Akademischer Verlag, 2008, ISBN 978-3-8274-1961-3, S. 292.
- ↑ a b T. Müller, M. Rafelsberger, C. Vergeiner, B. Kräutler: A dioxobilane as product of a divergent path of chlorophyll breakdown in Norway maple. In: Angewandte Chemie. Band 50, Nr. 45, November 2011, S. 10724–10727; doi:10.1002/anie.201103934, PMID 21928453, PMC 3262146 (freier Volltext) (englisch).
- ↑ a b c P. Matile, S. Hortensteiner, H. Thomas, B. Krautler: Chlorophyll Breakdown in Senescent Leaves. In: Plant physiology, Band 112, Nr. 4, Dezember 1996, S. 1403–1409; doi:10.1104/pp.112.4.1403, PMID 12226455, PMC 158071 (freier Volltext) (englisch).
- ↑ Sekundäre Pflanzenstoffe und ihre Wirkung auf die Gesundheit – Eine Aktualisierung anhand des Ernährungsberichts 2012. Abgerufen am 15. April 2021.
- ↑ BGBl. 1959 I S. 756 vom 19. Dezember 1959
- ↑ Eintrag zu E 140: Chlorophylls and Chlorophyllins in der Europäischen Datenbank für Lebensmittelzusatzstoffe, abgerufen am 16. Juni 2020.
- ↑ BGBl. 1966 I S. 74 vom 20. Januar 1966
- ↑ a b Verordnung (EG) Nr. 1333/2008 des Europäischen Parlaments und des Rates vom 16. Dezember 2008 über Lebensmittelzusatzstoffe.
- ↑ Spezifikationen der zugelassenen Lebensmittelzusatzstoffe
- ↑ Seit 1835 Gehe Arzneimittel. In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. VI.
- ↑ Unseren wasserlöslichen Chlorophyllpuder Cenat […]. In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. LXXVI (Anzeige von Dr. Madaus & Co.)
- ↑ Kritische Betrachtung zum Thema Chlorophyll. In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. XXV.
- ↑ Pelletier, Caventou: Sur la Matiere verte des Feuilles. In: Annales de Chimie et de Physique, 1818, 9, S. 194–196; eingeschränkte Vorschau in der Google-Buchsuche (französisch).
- ↑ Kritische Betrachtung zum Thema Chlorophyll. In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. XXV.
- ↑ M. Strell, A. Kalojanoff, H. Koller: Teilsynthese des Grundkörpers von Chlorophyll a, des Phäophorbids a, In: Angewandte Chemie, Band 72, 1960, S. 169–170.
- ↑ Eric Fontain, Die Münchner Chlorophyll-Synthese, TU München, 2000

