Geobacter sulfurreducens
| Geobacter sulfurreducens | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
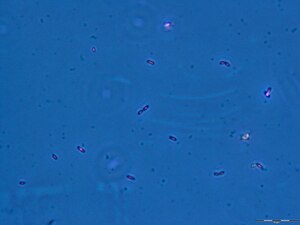
Geobacter sulfurreducens | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Geobacter sulfurreducens | ||||||||||||
| Caccavo et al. 1995 |
Das Proteobakterium Geobacter sulfurreducens ist eine Geobacter-Spezies, die zur schwefelreduzierenden Gruppe der Ordnung Desulfuromonadales gehört.
Beschreibung
[Bearbeiten | Quelltext bearbeiten]Die Bakterien sind gramnegative unbewegliche Stäbchen, die 2 bis 3 × 0,5 µm groß werden. Es werden keine Sporen gebildet. Die Zellen enthalten Cytochrom c und wachsen noch in Medien mit einer Salzkonzentration, die der Hälfte der von Meerwasser entspricht, also 1,75 %. Ihr Wachstumsoptimum liegt zwischen 30 und 35 °C.
Sie sind strikt anaerob und chemoorganotroph, das heißt, sie gewinnen ihre Energie aus organischen Stoffen. Sie oxidieren Acetat mit Eisen(III), Schwefel, Kobalt(III), Fumarat, oder Malat als Elektronenakzeptor. Auch Wasserstoff wird als Elektronendonor zur Eisen(III)reduzierung verwendet.
G. sulfurreducens ist das erste isolierte Bakterium, das die Oxidation von Acetat oder Wasserstoff an die Eisen(III)reduzierung koppelt.
Artabgrenzung
[Bearbeiten | Quelltext bearbeiten]Phylogenetisch ist G. sulfurreducens am nächsten mit Geobacter metallireducens verwandt. Beides sind metallreduzierende Bakterien, aber G. sulfurreducens kann im Vergleich dazu Mangan(IV) nicht reduzieren, kann dafür aber Wasserstoff als Elektronendonor nutzen. G. sulfurreducens kann auch keine Alkohole oder aromatische Verbindungen wie Phenole als Elektronendonoren verwenden.
Habitat
[Bearbeiten | Quelltext bearbeiten]G. sulfurreducens wurde aus Oberflächensedimenten eines Grabens in Norman (Oklahoma) isoliert, der mit Kohlenwasserstoffen verunreinigt war.[1] Acetat fungierte hierbei als Elektronendonor und dreiwertiges Eisen als Elektronenakzeptor [Eisenphosphat in Form von Eisen(III)-haltigem Diphosphat].
Historisches
[Bearbeiten | Quelltext bearbeiten]Die erste Isolation von Mikroben der späteren Gattung Geobacter erfolgte 1987 durch Derek Lovley aus Sedimenten des Potomac River.[2] Die Gattung Geobacter wurde 1993 zusammen mit ihrer Typusart G. metallireducens durch Lovley et al. beschrieben[3] und 1995 bestätigt.[4] 1994 erfolgte durch Caccavo et al. eine Beschreibung von Geobacter sulfurreducens als neue Art,[1] die ebenfalls 1995 bestätigt wurde.[4]
Wissenschaftliche Anwendungen
[Bearbeiten | Quelltext bearbeiten]
Eine Arbeitsgruppe um den amerikanischen Physiker Mark Tuominen hat 2011 nachgewiesen, dass ein dünner Film aus G. sulfurreducens eine elektrische Leitfähigkeit von ca. 0,5 S/m aufweist.[5] Eine ähnliche elektrische Leitfähigkeit zeigen Nanofilamente, die man aus den Bakterien gewinnen kann. Die Leitfähigkeit des Materials bleibt dabei über mehrere Zentimeter erhalten und ähnelt damit den elektrischen Eigenschaften synthetischer metallischer Nanostrukturen. Die Wissenschaftler interpretierten ihre Befunde so, dass G. sulfurreducens Proteine produziert, die elektrischen Strom leiten, was große Bedeutung für den Bau von Elektronikbauteilen im Nanomaßstab haben könnte. 2020 entwickelten Forscher mit Hilfe der leitfähigen mikrobiellen Nanodrähten des Bakteriums einen Memristor, der bei elektrischen Spannungen von unter 100 mV funktioniert. Der Memristor erlaubt den Betrieb durch Aktionspotenziale von natürlichen Neuronen und kann Biosensor-Signale lokal verarbeiten. Die Technologie könnte für Gehirn-inspiriertes Computing und direkte Kommunikation mit biologischen Gehirnzellen eingesetzt werden.[6][7][8]
Literatur
[Bearbeiten | Quelltext bearbeiten]- F. Caccavo, D. J. Lonergan, D. R. Lovley, M. Davis, J. F. Stolz, M. J. McInerney: Geobacter sulfurreducens sp. nov., a hydrogen- and acetate-oxidizing dissimilatory metal-reducing microorganism. In: Applied and environmental microbiology. Band 60, Nummer 10, Oktober 1994, S. 3752–3759, PMID 7527204, PMC 201883 (freier Volltext).
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Mikrobe baut stromleitende Proteinnetze – Bakterienfäden erweisen sich als ähnlich gute Elektronenüberträger wie Metalle. Auf: scinexx.de vom 8. August 2011.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b F. Caccavo, D. J. Lonergan, D. R. Lovley, M. Davis, J. F. Stolz, M. J. McInerney: Geobacter sulfurreducens sp. nov., a hydrogen- and acetate-oxidizing dissimilatory metal-reducing microorganism. In: Applied and environmental microbiology. Band 60, Nummer 10, Oktober 1994, S. 3752–3759, PMID 7527204, PMC 201883 (freier Volltext).
- ↑ Derek R. Lovley, John F. Stolz, Gordon L. Nord, Elizabeth J. P. Phillips: Anaerobic production of magnetite by a dissimilatory iron-reducing microorganism. In: Nature. 330, 1987, S. 252, doi:10.1038/330252a0.
- ↑ D. R. Lovley, S. J. Giovannoni, D. C. White, J. E. Champine, E. J. Phillips, Y. A. Gorby, S. Goodwin: Geobacter metallireducens gen. nov. sp. nov., a microorganism capable of coupling the complete oxidation of organic compounds to the reduction of iron and other metals. In: Archives of microbiology. Band 159, Nummer 4, 1993, S. 336–344, PMID 8387263.
- ↑ a b IUMS: Validation of the Publication of New Names and New Combinations Previously Effectively Published Outside the IJSB: List No. 54. In: International Journal of Systematic Bacteriology. 45, 1995, S. 619, doi:10.1099/00207713-45-3-619.
- ↑ Malvankar NS, Vargas M, Nevin KP, Franks AE, Leang C, Kim BC, Inoue K, Mester T, Covalla SF, Johnson JP, Rotello VM, Tuominen MT, Lovley DR: Tunable metallic-like conductivity in microbial nanowire networks. In: Nat Nanotechnol. Vom 7. August 2011. doi:10.1038/nnano.2011.119. PMID 21822253
- ↑ Scientists create tiny devices that work like the human brain In: The Independent, 20. April 2020. Abgerufen am 17. Mai 2020 (englisch).
- ↑ Researchers unveil electronics that mimic the human brain in efficient learning In: phys.org. Abgerufen am 17. Mai 2020 (englisch).
- ↑ Tianda Fu, Xiaomeng Liu, Hongyan Gao, Joy E. Ward, Xiaorong Liu, Bing Yin, Zhongrui Wang, Ye Zhuo, David J. F. Walker, J. Joshua Yang, Jianhan Chen, Derek R. Lovley, Jun Yao: Bioinspired bio-voltage memristors. In: Nature Communications. 11. Jahrgang, Nr. 1, 20. April 2020, S. 1861, doi:10.1038/s41467-020-15759-y, PMID 32313096, PMC 7171104 (freier Volltext), bibcode:2020NatCo..11.1861F.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Personen
- Datenbanken
- LPSN, Stichwort „Geobacter“ – http://www.bacterio.net/geobacter.html
- NCBI, Taxonomy browser, Stichwort „Geobacter sulfurreducens“ – https://www.ncbi.nlm.nih.gov/Taxonomy/Browser/wwwtax.cgi?id=35554