Kaliumhexafluorosilicat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
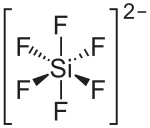
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Kaliumhexafluorosilicat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | K2[SiF6] | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 220,27 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Kaliumhexafluorosilicat ist eine anorganische chemische Verbindung des Kaliums aus der Gruppe der Hexafluorosilicate und das Kaliumsalz der Hexafluorokieselsäure.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]Kaliumhexafluorosilicat kommt natürlich in Form der Minerale Hieratit und Demartinit vor.[6]
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Kaliumhexafluorosilicat kann durch Reaktion von Hexafluoridokieselsäure mit Kaliumhydroxid oder Kaliumchlorid gewonnen werden.[7]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Kaliumhexafluorosilicat ist ein weißer Feststoff, der schwer löslich in Wasser ist. Er zersetzt sich bei Erhitzung oder in heißem Wasser[8], wobei Fluorwasserstoff und Siliciumtetrafluorid entstehen.[1] Er ist ohne Zersetzung schmelzbar unter Zusatz von Kaliumfluorid. Er besitzt eine kubische Kristallstruktur mit der Raumgruppe Fm3m (Raumgruppen-Nr. 225). Es ist auch noch eine zweite Modifikation mit der Raumgruppe P63mc (Raumgruppen-Nr. 186) bekannt.[3][2]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Kaliumhexafluorosilicat wird bei der Herstellung von Porzellan und auch für die Konservierung von Holz verwendet. Es ist an der Herstellung von Keramik, Aluminium und Magnesiumschmelzen beteiligt und dient darüber hinaus als Zwischenprodukt bei der Herstellung von optischem Glas.[9]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h Eintrag zu Kaliumhexafluorosilikat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- ↑ a b J. H. Loehlin: Redetermination of the structure of potassium hexafluorosilicate, K2SiF6. In: Acta Crystallographica Section C Crystal Structure Communications. Band 40, Nr. 3, 15. März 1984, S. 570–570, doi:10.1107/s0108270184004893.
- ↑ a b R. Blachnik: Taschenbuch für Chemiker und Physiker Band 3: Elemente, anorganische Verbindungen und Materialien, Minerale. Springer-Verlag, 2013, ISBN 978-3-642-58842-6, S. 524 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. CRC Press, 2016, ISBN 978-1-4398-1462-8, S. 324 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Eintrag zu Alkalihexafluorosilikate(K) im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 21. November 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ mineralienatlas.de: Mineralienatlas Lexikon - Hieratit, abgerufen am 21. November 2016
- ↑ Jane E. Macintyre: Dictionary of Inorganic Compounds. CRC Press, 1992, ISBN 978-0-412-30120-9, S. 3217 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ D. Menz, W. Wilde, L. Kolditz, K. Heide: Dynamisch thermische analyse der Zersetzung von K2SiF6. In: Journal of Fluorine Chemistry. 24 (3), 1984, S. 345–354, doi:10.1016/S0022-1139(00)81323-8.
- ↑ Datenblatt Potassium hexafluorosilicate, 99.999% (metals basis) bei Alfa Aesar, abgerufen am 21. November 2016 (Seite nicht mehr abrufbar).

![{\displaystyle \mathrm {2\ KCl+H_{2}[SiF_{6}]\longrightarrow K_{2}[SiF_{6}]+2\ HCl} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/7eda1bd53038b26e50362d745cc445f26b9d9e8b)