Magnesiumsulfat
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
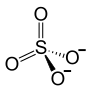
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Magnesiumsulfat | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Kurzbeschreibung |
farbloser, hygroskopischer Feststoff[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||||||||
| Dichte | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
gut in Wasser löslich: 300 g·l−1 (20 °C) (MgSO4) [2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten |
| |||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||

Magnesiumsulfat (MgSO4) ist neben Magnesiumhydrogensulfat (Mg(HSO4)2)[3] eines der beiden Magnesiumsalze der Schwefelsäure. Das auch als Mineral Epsomit auftretende Magnesiumsulfat-Heptahydrat (MgSO4·7 H2O) erhielt des bitteren Geschmacks wegen den Trivialnamen Bittersalz.
-
Magnesiumsulfat
Vorkommen
[Bearbeiten | Quelltext bearbeiten]In der Natur kommt Magnesiumsulfat überwiegend als Kieserit, ein Monohydrat, vor. Daneben kommen weitere Magnesiumsulfate als Mineralien mit unterschiedlichem Wasseranteil vor: Pentahydrit (Pentahydrat), Hexahydrit (Hexahydrat), Epsomit (Heptahydrat).
Herstellung
[Bearbeiten | Quelltext bearbeiten]Magnesiumsulfat lässt sich aus Magnesium und Schwefelsäure nach folgender Reaktionsgleichung herstellen:
Weiterhin entsteht es bei der Umsetzung von Magnesiumoxid oder Magnesiumhydroxid mit Schwefelsäure und anschließender Abdampfung des Wassers bzw. Trocknung:
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Magnesiumsulfat ist ein farbloser, geruchloser, stark hygroskopischer Feststoff mit bitterem Geschmack. Es existieren mehrere Hydrate, von denen das wichtigste das Magnesiumsulfat-Heptahydrat MgSO4 · 7 H2O (Synonym: Bittersalz; Mineral Epsomit) ist.


Epsomit bildet farblose Kristalle, die ein rhombisch pseudotetragonales Kristallgitter ausbilden. Die Kristalle blühen oft in faserigen Aggregaten aus und bilden Stalaktiten. Epsomit ist gut wasserlöslich und hat eine Dichte von 1,68 g/cm³.
Aufgrund seiner calciumantagonistischen Eigenschaft bewirkt Magnesiumsulfat eine periphere Muskelerschlaffung. Charles H. Peck und Samuel J. Meltzner hatten es 1916[4] auch zur Erzielung einer zentralen Narkose intravenös eingesetzt.[5]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Düngemittel
[Bearbeiten | Quelltext bearbeiten]- Magnesiumsulfat wird als Magnesiumquelle für Pflanzen in Düngemitteln verwendet. Reines Bittersalz wird unter anderem im Obstbau eingesetzt, speziell aber auch, um ein Braunwerden der Nadeln von Nadelgehölzen zu verhindern. Magnesiumsulfat trägt zu einem sauren Bodenmilieu bei, welches von Koniferen im Allgemeinen bevorzugt wird. Üblich ist ein Eintrag von 50 g/m² im Frühjahr oder Spätherbst. Bei großen Bäumen werden bis zu 200 g/m² aufgebracht.
Trocknungsmittel
[Bearbeiten | Quelltext bearbeiten]- Wegen seines hygroskopischen Charakters wird es in der organischen Chemie zur Trocknung von Stoffen benutzt. Dazu gibt man zu der zu trocknenden Flüssigkeit so viel wasserfreies Magnesiumsulfat, bis neu zugesetztes Magnesiumsulfat in der Flüssigkeit feinkörnig bleibt und nicht mehr verklumpt. Das Magnesiumsulfat kann anschließend abfiltriert werden.
Medizinische Anwendung
[Bearbeiten | Quelltext bearbeiten]- In der Medizin findet es schon lange Zeit als Abführmittel Verwendung. Der Pflanzenanatom Nehemiah Grew extrahierte das Bittersalz, welches er 1695[6] als Magnesiumsulfat identifizierte, erstmals aus Mineralwasser.[7]
- In der Geburtshilfe wird MgSO4 als Mittel der Wahl für die Therapie und Prophylaxe von Eklampsie-assoziierten Krampfanfällen verwendet.
- Magnesiumsulfat findet Anwendung in sogenannten Instant-Hot-Packs zur Erzeugung von (therapeutischer) Wärme bis zu 40 °C.[8]
- Magnesiumsulfat wird in der Medizin auch für Gallenfluss-Tests verwendet (siehe Choleretikum).[9]
- Zur Therapie einer Torsades-de-pointes-Tachykardie wird Magnesiumsulfat intravenös verabreicht (Off-Label-Use).[10]
- Magnesiumsulfat findet Anwendung in der Behandlung eines akuten Asthmaanfalls und auch beim akuten Herzinfarkt.[11]
Weitere Verwendung
[Bearbeiten | Quelltext bearbeiten]- MgSO4 wird in Floating-Anlagen verwendet, um eine hochgesättigte Sole herzustellen, auf der ein Körper liegen kann, ohne unterzutauchen.
- Magnesiumsulfat-Lösung wird als Elektrolyt-Ersatz- bzw. -Regenerations-Lösung für Bleiakkumulatoren verwendet.
- Als Bestandteil künstlicher Speisesalze, z. B. Pansalz, zur Einsparung von Natriumchlorid.
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu MAGNESIUM SULFATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2020.
- ↑ a b c d e f g h i j Eintrag zu Magnesiumsulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 19. Dezember 2019. (JavaScript erforderlich)
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Magnesiumhydrogensulfat: CAS-Nr.: 10028-26-9, EG-Nr.: 233-073-4, ECHA-InfoCard: 100.030.055, PubChem: 11769948, ChemSpider: 9944631, Wikidata: Q27278236.
- ↑ Charles H. Peck. Samuel J. Meltzer: Anaesthesia in human beings by intravenous injections of magnesium sulphate. In: Journal of the American Medical Association. Band 67, 1916, S. 1131 ff.
- ↑ H. Orth, I. Kis: Schmerzbekämpfung und Narkose. In: Franz Xaver Sailer, Friedrich Wilhelm Gierhake (Hrsg.): Chirurgie historisch gesehen. Anfang – Entwicklung – Differenzierung. Dustri-Verlag, Deisenhofen bei München 1973, ISBN 3-87185-021-7, S. 1–32, hier: S. 16.
- ↑ Nehemiah Grew: Tractatus de Salis Cathartici Amari in Aquis Ebeshamensibus et hujusmodi aliis contenti, natura et usu. London 1695 (Digitalisat).
- ↑ Barbara I. Tshisuaka: Grew, Nehemiah. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 510.
- ↑ C. Schmuck, B. Engels, T. Schirmeister, R. Fink: Chemie für Mediziner. Pearson Studium, Hallbergmoos 2008, ISBN 978-3-8273-7286-4, S. 164
- ↑ Anatomisch-therapeutisch-chemische Klassifikation mit Tagesdosen. Amtliche Fassung des ATC-Index mit DDD-Angaben für Deutschland im Jahre 2011. S. 160.
- ↑ Thomas Ziegenfuß: Notfallmedizin. 5. Auflage. S. 299
- ↑ Thomas Ziegenfuß: Notfallmedizin. 5. Auflage. S. 330




