Nitrofurane
Nitrofurane sind eine Gruppe chemischer Verbindungen bestehend aus den Derivaten des 2-Nitrofurans.[1] Es gibt zahlreiche Vertreter, wie etwa das gegen Harnwegserkrankungen eingesetzte Nitrofurantoin (siehe unten).[2] Oft werden sie international mit der Vorsilbe Nitrofuran- oder mit deren abgekürzten Formen Nifur- und Fur- benannt.[1] Im Laufe der 1940er-Jahre wurde die fungizide und bakterizide Wirkung der Nitrofurane entdeckt. Nitrofurane werden therapeutisch als Antibiotika und Antiprotozoika verwendet. Wenige Vertreter der Nitrofurane wurden in Ostasien kurzzeitig zur Lebensmittelkonservierung eingesetzt, diese Praxis wurde allerdings wegen mutagener Eigenschaften eingestellt.[1]
Synthese
[Bearbeiten | Quelltext bearbeiten]Ausgehend vom industriell aus pflanzlichen Materialien gewonnenen Furfural (1) wird zunächst unter Zugabe von Nitriersäure in einer regioselektiven elektrophilen aromatischen Substitution der 5-Nitrofurfurylaldehyd (2) hergestellt:[3]
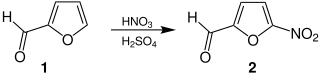
Das aus der Nitrierung gewonnene Nitrofuran 2 kann nun – gegebenenfalls nach Verlängerung der Seitenkette – unter Zugabe entsprechender Hydrazide oder deren Salze zu einem Großteil der pharmazeutisch relevanten Nitrofurane weiterverarbeitet werden. Das einfachste Beispiel hierfür ist die Synthese von Nitrofural (4) ausgehend von dem Hydrochlorid 3:[4]

Verwendung
[Bearbeiten | Quelltext bearbeiten]Nitrofurane werden therapeutisch als Antibiotika und Antiprotozoika verwendet. Ihre Verwendung bei lebensmittelliefernden Tieren ist in der EU seit vielen Jahren verboten (Furaltadon, Nitrofurantoin und Nitrofurazon seit 1993, Furazolidon seit 1995, Nifursol seit 2003).[5]
Nitrofurantoin dient der Bekämpfung von Escherichia coli-Bakterien, als Mittel gegen Harnwegsinfekte, sowie als Oberflächenantiseptikum.[1][6]
-
Strukturformel von Nitrofurantoin
-
Escherichia coli-Bakterien
Nitrofural (anderer Name: Nitrofurazon) kann zur Behandlung von komplizierten Wundinfektionen und Hauterkrankungen als Oberflächenantiseptikum eingesetzt werden.[1][4]
-
Strukturformel von Nitrofural
-
Nitrofural ist ein gelbes Pulver
Nifurtoinol kann zur Bekämpfung des für die Giardiasis verantwortlichen Geißeltierchens Giardia intestinalis und zur Behandlung von Harnwegsinfektionen eingesetzt werden.[7][8]
-
Strukturformel von Nifurtoinol
-
Erreger der Giardiasis
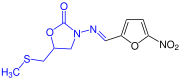
Nifuratel wirkt als Antiprotozoikum bei Infektionen mit Trichomonaden. Es hat eine fungizide Wirkung gegenüber Monilinia (Fruchtmumie).[9]
-
Strukturformel von Nifuratel
Nifurtimox ist relevant in der Behandlung von Protozoeninfektionen wie der Chagas-Krankheit bzw. anderen Trypanosomiasen.[8][10]
-
Strukturformel von Nifurtimox
-
Behandlung der Chagas-Krankheit
Weitere Vertreter:
-
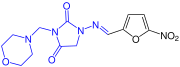
Furaltadon: früher Verwendung in der Tiermedizin[14]
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Nitrofurane – bei Nutztieren EU-weit verbotene Tierarzneimittel, auf der Website des Bayerischen Landesamts für Gesundheit und Lebensmittelsicherheit (LGL)
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e Jürgen Falbe, Manfred Regitz (Hrsg.): Römpp Chemie Lexikon, 9. Auflage, Georg Thieme Verlag, Stuttgart 1990, ISBN 3-13-734909-5, S. 3019.
- ↑ Ernst Mutschler, Gerd Geisslinger, Heyo Klaus Kroemer, Sabine Menzel, Peter Ruth: Mutschler Arzneimittelwirkungen: Lehrbuch der Pharmakologie, der klinischen Pharmakologie und Toxikologie. 10. Auflage. WVG, Wissenschaftliche Verlagsgesellschaft, Stuttgart 2013, ISBN 978-3-8047-2898-1, S. 792.
- ↑ Jonathan Clayden, Nick Greeves, Stuart Warren: Organische Chemie. Springer-Verlag, Berlin Heidelberg 2013, ISBN 978-3-642-34715-3, S. 808–809.
- ↑ a b Axel Kleemann; Jürgen Engel; Bernhard Kutscher; Dietmar Reichert: Pharmaceutical Substances – Syntheses, Patents and Applications of the most relevant APIs. 5. Auflage, Georg Thieme Verlag KG, 2009, ISBN 978-3-13-558405-8, S. 980.
- ↑ EFSA CONTAM Panel (EFSA Panel on Contaminants in the Food Chain): Scientific Opinion on nitrofurans and their metabolites in food. EFSA Journal 2015; Band 13, Nr. 6. doi:10.2903/j.efsa.2015.4140
- ↑ Axel Kleemann; Jürgen Engel; Bernhard Kutscher; Dietmar Reichert: Pharmaceutical Substances – Syntheses, Patents and Applications of the most relevant APIs. 5. Auflage. Georg Thieme Verlag, 2009, ISBN 978-3-13-558405-8, S. 981.
- ↑ a b J. M. Wright, L. A. Dunn, P. Upcroft, J. A. Upcroft: Efficacy of antigiardial drugs. In: Expert Opinion on Drug Safety. Band 2, Nummer 6, November 2003, S. 529–541, PMID 14585063.
- ↑ a b c Jürgen Falbe, Manfred Regitz (Hrsg.): Römpp Chemie Lexikon, 9. Auflage, Georg Thieme Verlag, Stuttgart 1990, ISBN 3-13-734909-5, S. 3001.
- ↑ a b Jürgen Falbe, Manfred Regitz (Hrsg.): Römpp Chemie Lexikon, 9. Auflage, Georg Thieme Verlag, Stuttgart 1990, ISBN 3-13-734709-2, S. 1461.
- ↑ Fact sheet der WHO zur Chagas-Krankheit; abgerufen am 26. Juni 2017.
- ↑ Anne Delsarte, Michel Faway, Jean-Marie Frère, Jacques Coyette, Claire-Michèlle Calber-Bacq, Ernst Heinen: Nifurzide, a Nitrofuran Antiinfectious Agent: Interaction with Escherichia coli Cells. In: Antimicrobial Agents and Chemotherapy., Volume 19, No. 3, S. 477–486, PMID 7018391, doi:10.1128/aac.19.3.477.
- ↑ G. N. Dutta, L. A. Devriese, P. F. van Assche: Susceptibility of clostridia from farm animals to 21 antimicrobial agents including some used for growth promotion. In: The Journal of Antimicrobial Chemotherapy. Vol. 12 (4) 1983, S. 347–356; PMID 6643330.
- ↑ Vandana Kalia, Rajni Miglani, Kedar P. Purnapatre, Tarun Mathur, Smita Singhal, Seema Khan, Sreedhara R. Voleti, Dilip J. Upadhyay, Kulvinder Singh Saini, Ashok Rattan, V. Samuel Raj: Mode of Action of Ranbezolid against Staphylococci and Structural Modeling Studies of Its Interaction with Ribosomes. In: Antimicrobial Agents and Chemotherapy. Vol. 53 (4) 2009, S. 1427–1433; PMID 19075051.
- ↑ Gesundheitliche Bewertung von Nitrofuranen in Lebensmitteln, BfR, 2002 (PDF-Datei) auf bfr.bund.de
- ↑ P. Männistö, P. Karttunen: Pharmacokinetics of furagin, a new nitrofurantoin congener, on human volunteers. In: International Journal of Clinical Pharmacology and Biopharmacy. 17 (6), 1979, S. 264–270; PMID 468451.
- ↑ History: 1970s, Consumers Union of Japan; abgerufen am 22. Juni 2017.









![Nifuroxazid: Verwendung als Darm-Antiseptikum[8]](http://upload.wikimedia.org/wikipedia/commons/thumb/d/d6/Strukturformel_Nifuroxazid_V3.svg/180px-Strukturformel_Nifuroxazid_V3.svg.png)
![Furazolidon: Behandlung von Durchfall, Cholera, Trichomonaden und Salmonellen-Vergiftungen.[9][7]](http://upload.wikimedia.org/wikipedia/commons/thumb/f/f9/Strukturformel_Furazolidon_V3.svg/180px-Strukturformel_Furazolidon_V3.svg.png)
![Nitrovin: ehemals als antibiotischer Wachstumsförderer eingesetzt[12]](http://upload.wikimedia.org/wikipedia/commons/thumb/e/eb/Strukturformel_Nitrovin_V3.svg/180px-Strukturformel_Nitrovin_V3.svg.png)
![Ranbezolid: wirksam gegenüber Staphylokokken.[13]](http://upload.wikimedia.org/wikipedia/commons/thumb/8/82/Strukturformel_Ranbezolid_V3.svg/180px-Strukturformel_Ranbezolid_V3.svg.png)
![Furaltadon: früher Verwendung in der Tiermedizin[14]](http://upload.wikimedia.org/wikipedia/commons/thumb/0/01/Strukturformel_Furaltadon_V4.svg/180px-Strukturformel_Furaltadon_V4.svg.png)
![Furazidin: Behandlung von Harnwegsinfektionen.[15]](http://upload.wikimedia.org/wikipedia/commons/thumb/4/4c/Strukturformel_Furazidin_V5.svg/180px-Strukturformel_Furazidin_V5.svg.png)
![Furylfuramid: Bis in die 1970er-Jahre Konservierungsmittel in Japan.[16]](http://upload.wikimedia.org/wikipedia/commons/thumb/5/57/Strukturformel_Furylfuramid_V3.svg/180px-Strukturformel_Furylfuramid_V3.svg.png)