Propargylalkohol
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Propargylalkohol | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C3H4O | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit leicht geranienartigem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 56,06 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,948 g·cm−3 (20 °C)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
115 °C[2] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| pKS-Wert |
13,6 (25 °C)[3] | |||||||||||||||
| Löslichkeit |
mischbar mit Wasser, Ethanol, Diethylether, Pyridin, Benzol, Trichlormethan[2][1] | |||||||||||||||
| Brechungsindex |
1,432 (20 °C)[4] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Propargylalkohol (nach IUPAC-Nomenklatur: Prop-2-in-1-ol) ist eine organisch-chemische Verbindung aus der Stoffgruppe der Alkinole. Es ist ein Zwischenprodukt der Chemischen Industrie.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Propargylalkohol wird großtechnisch nach dem Reppe-Verfahren (Ethinylierung) hergestellt. Dabei reagiert Acetylen im großen Überschuss mit Formaldehyd unter Kupfer(I)-acetylid-Katalyse bei Temperaturen zwischen 95 und 150 °C und Drücken von 2 bis 3 bar zu Propargylalkohol.[1][7]

Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Die entzündliche, farblose Flüssigkeit hat einen charakteristischen Geruch. Mit einem Flammpunkt von 33 °C[2] können sich mit der Luft ab dieser Temperatur explosionsfähige Gemische bilden. Der Explosionsbereich liegt zwischen 2,8 Vol.‑% (66 g/m3) als untere Explosionsgrenze (UEG) und 78 Vol.‑% (1817 g/m3) als obere Explosionsgrenze (OEG).[2] Der Dampf ist schwerer als Luft. Die Zündtemperatur beträgt 365 °C.[8] Der Stoff fällt somit in die Temperaturklasse T2. Unter dem Einfluss von Hitze, Licht, Oxidationsmitteln und Peroxiden kann Propargylalkohol polymerisiert werden. Mit Oxidationsmitteln können heftige Reaktionen unter Hitzeentwicklung stattfinden. Eine Überschreitung des Arbeitsplatzgrenzwertes ist durch den Geruch nicht feststellbar.
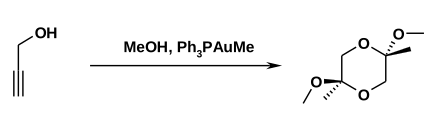
Propargylalkohol kann in Gegenwart von Goldkatalysatoren und Methanol zu einem cyclischen dimeren Bisketal umgesetzt werden, wobei mit 93%iger Ausbeute das trans-Isomer entsteht.[9]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Propargylalkohol wird unter anderem als Korrosionsinhibitor für Stahl (gegen den Angriff von Säuren), als Stabilisator für Chloralkane sowie als Zwischenprodukt für organische Synthesen eingesetzt.[1]
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d Eintrag zu Prop-2-in-1-ol. In: Römpp Online. Georg Thieme Verlag, abgerufen am 19. Januar 2019.
- ↑ a b c d e f g h i j k l Eintrag zu 2-Propin-1-ol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Januar 2024. (JavaScript erforderlich)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Dissociation Constants of Organic Acids and Bases, S. 8-43.
- ↑ Datenblatt Propargyl alcohol bei Sigma-Aldrich, abgerufen am 10. Februar 2023 (PDF).
- ↑ Eintrag zu Prop-2-yn-1-ol im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 19. Januar 2019. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 107-19-7 bzw. Propargylalkohol), abgerufen am 2. November 2015.
- ↑ Patentanmeldung DE19903213A1: Verfahren zur Herstellung von Propargylalkohol. Angemeldet am 27. Januar 1999, veröffentlicht am 3. August 2000, Anmelder: Linde AG, Erfinder: Nicole Schödel.
- ↑ E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen – Band 1: Brennbare Flüssigkeiten und Gase, Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003.
- ↑ J.H. Teles, S. Brode, M. Chabana: Cationic Gold(I) Complexes: Highly Efficient Catalysts for the Addition of Alcohols to Alkynes in Angew. Chem., Int. Ed. 37 (1998) 1415–1418, doi:10.1002/(SICI)1521-3773(19980605)37:10<1415::AID-ANIE1415>3.0.CO;2-N.




