Reelin
| Reelin | ||
|---|---|---|
| ||
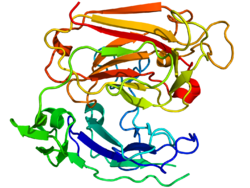
| Bändermodell des Reelin-Fragments aus Maus (AS 1222–1597) nach PDB 2DDU | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 3435 Aminosäuren; 386 kDa | |
| Isoformen | 2 | |
| Bezeichner | ||
| Gen-Namen | RELN ; RL | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 3.4.21.-, Serinprotease | |
| Vorkommen | ||
| Übergeordnetes Taxon | Euteleostomi | |
| Orthologe | ||
| Mensch | Maus | |
| Entrez | 5649 | 19699 |
| Ensembl | ENSG00000189056 | ENSMUSG00000042453 |
| UniProt | P78509 | Q148P9 |
| Refseq (mRNA) | NM_005045 | NM_011261 |
| Refseq (Protein) | NP_005036 | NP_035391 |
| Genlocus | Chr 7: 102.9 – 103.42 Mb | Chr 5: 21.4 – 21.86 Mb |
| PubMed-Suche | 5649 | 19699
|
Reelin ist ein Glykoprotein, das im Säugetier-ZNS an der Differenzierung und Migration von Neuronen beteiligt ist.
Entscheidende Bedeutung hat es zum Beispiel für die Reifung des Hippocampus, bei dem die scharfe Schichtung verschiedener Neurone essentiell für dessen Funktionalität ist. Dort wird es von Cajal-Rezius-Zellen gebildet. Für Reelin sind bisher zwei Rezeptoren bekannt, die man bisher nur aus dem Lipid-Stoffwechsel kannte. Der eine ist der Apolipoproteinrezeptor 2 (APOER2) und der andere der Rezeptor des Very Low Density Lipoproteins (VLDLR). Über Unterschiede der beiden weiß man noch sehr wenig.
Bei Reelin-Knock-Out-Mäusen (Reeler-Mäuse), zwar lebensfähig, sieht man in Schnitten des Hippocampus und des Neocortex deutlich die ungelenkte Zellmigration, die in Co-Kulturen mit Reelin-produzierenden Hippocampi teilweise wieder gelenkt werden kann.

Klinische Bedeutung
[Bearbeiten | Quelltext bearbeiten]Störungen der Reelin-Verfügbarkeit werden in Zusammenhang gebracht mit folgenden Erkrankungen:
- Norman-Roberts-Syndrom[1]
- Schizophrenie[2]
- Bipolare Störung[2]
- Autismus[2]
- Temporallappenepilepsie[3]
- Alzheimer-Krankheit[4][5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu Lissenzephalie-Syndrom Typ Norman-Roberts. In: Orphanet (Datenbank für seltene Krankheiten)
- ↑ a b c K. Ishii, K. I. Kubo, K. Nakajima: Reelin and Neuropsychiatric Disorders. In: Frontiers in cellular neuroscience. Bd. 10, 2016, S. 229, doi:10.3389/fncel.2016.00229, PMID 27803648, PMC 5067484 (freier Volltext) (Review)
- ↑ E. Dazzo, M. Fanciulli, E. Serioli, G. Minervini, P. Pulitano, S. Binelli, C. Di Bonaventura, C. Luisi, E. Pasini, S. Striano, P. Striano, G. Coppola, A. Chiavegato, S. Radovic, A. Spadotto, S. Uzzau, A. La Neve, A. T. Giallonardo, O. Mecarelli, S. C. Tosatto, R. Ottman, R. Michelucci, C. Nobile: Heterozygous reelin mutations cause autosomal-dominant lateral temporal epilepsy. In: American Journal of Human Genetics. Bd. 96, Nr. 6, Juni 2015, S. 992–1000, doi:10.1016/j.ajhg.2015.04.020, PMID 26046367, PMC 4457960 (freier Volltext).
- ↑ Johann Grolle: Alzheimer: Wie ein Mediziner in Hamburg Gene entschlüsselt, die vor Alzheimer schützen. In: Der Spiegel. 19. Mai 2023 (spiegel.de [abgerufen am 6. Juni 2023]).
- ↑ A. Botella-López, F. Burgaya, R. Gavín, M. S. García-Ayllón, E. Gómez-Tortosa, J. Peña-Casanova, J. M. Ureña, J. A. Del Río, R. Blesa, E. Soriano, J. Sáez-Valero: Reelin expression and glycosylation patterns are altered in Alzheimer's disease. In: Proceedings of the National Academy of Sciences. Bd. 103, Nr. 14, April 2006, S. 5573–5578, doi:10.1073/pnas.0601279103, PMID 16567613, PMC 1414634 (freier Volltext).
Literatur
[Bearbeiten | Quelltext bearbeiten]Förster, E. et al. (2006): Laminating the hippocampus. In: Nat. Rev. Neurosci. 7(4):259-267. PMID 16543914 doi:10.1038/nrn1882 PDF