Αιθυλομεθυλαιθέρας
| Αιθυλομεθυλαιθέρας | |||
|---|---|---|---|
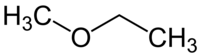
| |||
| |||
| Γενικά | |||
| Όνομα IUPAC | Μεθοξυαιθάνιο | ||
| Άλλες ονομασίες | Αιθυλομεθυλαιθέρας Αιθυλομεθυλοξείδιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C3H8O | ||
| Μοριακή μάζα | 60,1 amu | ||
| Σύντομος συντακτικός τύπος |
CH3CH2OCH3 | ||
| Συντομογραφίες | EtΟMe, EME | ||
| Αριθμός CAS | 540-67-0 | ||
| SMILES | CCOC | ||
| PubChem CID | 10903 | ||
| Δομή | |||
| Ισομέρεια | |||
| Ισομερή θέσης | 2 Προπανόλη-1 Προπανόλη-2 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -139 °C | ||
| Σημείο βρασμού | 7,6 °C | ||
| Ιξώδες | 0,224 cP (25 °C) | ||
| Εμφάνιση | Άχρωμο αέριο | ||
| Χημικές ιδιότητες | |||
| Επικινδυνότητα | |||

| |||
| Εξαιρετικά εύφλεκτος (F+) | |||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
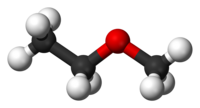
Ο αιθυλομεθυλαιθέρας (EthylMethylEther, EME) ή μεθυξυαιθάνιο ή αιθυλομεθυλοξείδιο είναι οργανική ένωση με μοριακό τύπο C3H8O και ημισυντακτικό τύπο CH3CH2OCH3, που γράφεται επίσης συντομογραφικά EtOMe. Πιο συγκεκριμένα, ανήκει στους αιθέρες. Η χημικά καθαρή ένωση, στις κανονικές συνθήκες περιβάλλοντος (θερμοκρασία 25 °C, πίεση 1 atm), είναι άχρωμο αέριο. Έχει τα ακόλουθα δύο (2) ισομερή θέσης:
- 1-προπανόλη με σύντομο συντακτικό τύπο CH3CH2CH2OH.
- 2-προπανόλη ή ισοπροπανόλη με σύντομο συντακτικό τύπο CH3CH(OH)CH3.
Παραγωγή[Επεξεργασία | επεξεργασία κώδικα]
Αλκυλίωση αλκολικού άλατος[Επεξεργασία | επεξεργασία κώδικα]
Μπορεί να παραχθεί με αιθυλίωση μεθανολικού άλατος (π.χ. CH3ONa) με αλαιθάνιο (CH3CH2X) ή μεθυλίωση αιθανολικού άλατος (π.χ. CH3CH2ONa) με αλομεθάνιο (CH3X) [1]:
ή
Χημικές ιδιότητες και παράγωγα[Επεξεργασία | επεξεργασία κώδικα]
Ως βάση κατά Λιούις, μπορεί να αντιδρά με οξέα κατά Λιούις σχηματίζοντας άλατα, ενώ αντιδρά βίαια με οξειδωτικά μέσα.
Οξείδωση[Επεξεργασία | επεξεργασία κώδικα]
Υπό την επίδραση φωτός (hv) και ατμοσφαιρικού οξυγόνου σχηματίζει ασταθή και εκρηκτικά υπεροξείδια[2], κυρίως 1-μεθοξυαιθυλυδροϋπεροξείδιο:
Επίδραση οξέων[Επεξεργασία | επεξεργασία κώδικα]
Με τη επίδραση οξέων, κλασσικών ή κατά Lewis παράγει διάφορα οξώνια, δηλαδή ασταθή και πολύ δραστικά παράγωγα του τρισθενή O+[3]:
Υδρόλυση[Επεξεργασία | επεξεργασία κώδικα]
1. Με επίδραση νερού, σε όξινο περιβάλλον, υδρολύεται προς ισομοριακό μείγμα μεθανόλης κσι αιθανόλης[4]:
2. Με επίδραση ψυχρού υδροϊωδίου (HI) παράγεται σχεδόν ισομοριακό μείγμα μεθανόλης, ιωδομεθανίου, αιθανόλης και ιωδαιθανίου:
3. Με επίδραση θερμού υδροϊωδίου (HI) παράγεται ισομοριακό μείγμα ιωδομεθανίου, ιωδαιθανίου και νερού:
Μετάθεση Wittig[Επεξεργασία | επεξεργασία κώδικα]
Με επίδραση αλκυλολιθίου (π.χ. μεθυλολιθίου) έχουμε τη μετάθεση Wittig, με την οποία παράγεται 2-προπανόλη και αλκάνιο (μεθάνιο αν είχε χρησιμοποιηθεί μεθυλολίθιο)[5]:
Επίδραση καρβενίων[Επεξεργασία | επεξεργασία κώδικα]
Με παρεμβολή μεθυλενίου, παράγεται μεθυλοπροπυλαιθέρας, διαιθυλαιθέρας και ισοπροπυλομεθυλαιθέρας[6]:
Θέματα ασφαλείας[Επεξεργασία | επεξεργασία κώδικα]
Είναι εξαιρετικά εύφλεκτος και η εισπνοή του μπορεί να προκαλέσει ασφυξία ή ζάλη.
Αναφορές και σημειώσεις[Επεξεργασία | επεξεργασία κώδικα]
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.198, §8.3.1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.200, §8.5.1.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.200, §8.5.2.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.201, §8.5.3.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.201, §8.5.4.
- ↑ Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 155, §6.7.3, R = CH3CH2OCH2.
Πηγές[Επεξεργασία | επεξεργασία κώδικα]
- Γ. Βάρβογλη, Ν. Αλεξάνδρου, Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη, «Χημεία Οργανικών Ενώσεων», παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, Μτφ. Α. Βάρβογλη, 1999
- Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982
- Δημήτριου Ν. Νικολαΐδη: Ειδικά μαθήματα Οργανικής Χημείας, Θεσσαλονίκη 1983.
| ||||||||||||||||||||



![{\displaystyle \mathrm {CH_{3}CH_{2}OCH_{3}+H^{+}{\xrightarrow {}}[(CH_{3}CH_{2})(CH_{3})OH]^{+}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/8191196a492c2071dd9ce23694c274e001398d53)
![{\displaystyle \mathrm {CH_{3}CH_{2}OCH_{3}+BF_{3}{\xrightarrow {}}[(CH_{3}CH_{2})(CH_{3})O][BF_{3}]{\xrightarrow {+RF}}[(CH_{3}CH_{2})(CH_{3})O(R)][BF_{4}]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/4c283fa47bab0723c73592704ca17c90098ffd05)




