Αιμολυτικό ουραιμικό σύνδρομο
| Αιμολυτικό ουραιμικό σύνδρομο | |
|---|---|
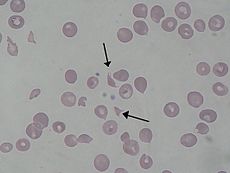 Σχιστοκύτταρα όπως παρατηρούνται σε άτομο με αιμολυτικό-ουραιμικό σύνδρομο | |
| Ειδικότητα | Παιδιατρική, νεφρολογία |
| Συμπτώματα | Πρώιμα: Αιματηρή διάρροια, έμετος, πυρετός Αργότερα: ελλατωμένος αριθμός αιμοπετάλιων, ελαττωμένος αριθμός ερυθρών αιμοσφαίριων, νεφρική ανεπάρκεια |
| Αίτια | Λοίμωξη από E coli O157:H7, shigella, σαλμονέλα |
| Παράγοντες κινδύνου | Νεαρή ηλικία, γυναίκα, ανοσοκατεσταλμένη ή υπάρχουσα νεφρική, ουροποιητική ή κατώτερη γαστρεντερική νόσο (επειδή αυτά είναι τα συστήματα που εμπλέκονται στη νόσο) |
| Διαγνωστική μέθοδος | Εξετάσεις αίματος (για την παρακολούθηση των επιπέδων των αιμοπεταλίων, των ερυθρών αιμοσφαιρίων και των λευκών αιμοσφαιρίων), εξετάσεις κοπράνων (ειδικά για τον έλεγχο μικροσκοπικών ή μακροσκοπικών επιπέδων φρέσκου ή παλιού αίματος), ανάλυση ούρων (για την παρακολούθηση της νεφρικής λειτουργίας, όπως η ουρία του αίματος) |
| Θεραπεία | Υποστηρικτική φροντίδα, αιμοκάθαρση, στεροειδή, μεταγγίσεις αίματος, πλασμαφαίρεση |
| Πρόγνωση | 1,5 ανά 100.000 ανά έτος |
| Θνησιμότητα | <5% κίνδυνος θανάτου |
| Ταξινόμηση | |
Το αιμολυτικό-ουραιμικό σύνδρομο (Hemolytic–uremic syndrome ή HUS) είναι μια διαταραχή του αίματος που χαρακτηρίζεται από ελαττωμένο αριθμό ερυθρών αιμοσφαιρίων, οξεία νεφρική βλάβη και ελαττωμένο αριθμό αιμοπετάλιων.[1][2] Τα αρχικά συμπτώματα περιλαμβάνουν συνήθως αιματηρή διάρροια, πυρετό, έμετο και αδυναμία.[1] Στη συνέχεια, εμφανίζονται νεφρικά προβλήματα και ελαττωμένος αριθμός αιμοπετάλιων καθώς η διάρροια εξελίσσεται.[1] Τα παιδιά προσβάλλονται συχνότερα, αλλά τα περισσότερα αναρρώνουν χωρίς μόνιμη βλάβη στην υγεία τους, αν και ορισμένα μπορεί να έχουν σοβαρές και μερικές φορές απειλητικές για τη ζωή επιπλοκές. Οι επιπλοκές μπορεί να περιλαμβάνουν νευρολογικά προβλήματα και καρδιακή ανεπάρκεια.[1]
Οι περισσότερες περιπτώσεις εμφανίζονται μετά από λοιμώδη διάρροια που οφείλεται σε έναν συγκεκριμένο στέλεχος του κολοβακτηρίου E. coli που ονομάζεται O157:H7. Άλλες αιτίες περιλαμβάνουν άλλα είδη βακτηρίων όπως ο πνευμονικός στρεπτόκοκκος, Σιγκέλλα, σαλμονέλα και ορισμένα φάρμακα.[1][1][2] Ο υποκείμενος μηχανισμός τυπικά περιλαμβάνει την παραγωγή της τοξίνης Shiga από τα βακτήρια.[1] Το άτυπο αιμολυτικό ουραιμικό σύνδρομο (aHUS) οφείλεται συχνά σε γενετική μετάλλαξη και εμφανίζεται διαφορετικά.[1] Ωστόσο, και τα δύο μπορεί να οδηγήσουν σε εκτεταμένη φλεγμονή και πολλαπλούς θρόμβους αίματος σε μικρά αιμοφόρα αγγεία, μια κατάσταση γνωστή ως θρομβωτική μικροαγγειοπάθεια.[3]
Η θεραπεία περιλαμβάνει υποστηρικτική φροντίδα και μπορεί να περιλαμβάνει αιμοκάθαρση, χορήγηση στεροειδών, μεταγγίσεις αίματος ή πλασμαφαίρεση[1] Περίπου 1,5 ανά 100.000 άτομα επηρεάζονται ετησίως από το σύνδρομο αυτό.[4] Λιγότερο από το 5% αυτών που πάσχουν από την πάθηση πεθαίνουν. Από τα υπόλοιπα άτομα, έως και το 25% έχει μόνιμα νεφρικά προβλήματα. Το HUS ορίστηκε για πρώτη φορά ως σύνδρομο το 1955.[5]
Σημάδια και συμπτώματα
[Επεξεργασία | επεξεργασία κώδικα]Μετά την κατανάλωση μολυσμένων τροφίμων, τα πρώτα συμπτώματα μόλυνσης μπορεί να εμφανιστούν οποιαδήποτε στιγμή από 1 έως 10 ημέρες αργότερα, αλλά συνήθως μετά από 3 έως 4 ημέρες.[6] Τα πρώιμα συμπτώματα μπορεί να περιλαμβάνουν διάρροια (η οποία είναι συχνά αιματηρή), κράμπες στο στομάχι, ήπιο πυρετό ή έμετο που οδηγεί σε αφυδάτωση και ολιγουρία.[6] Το σύνδρομο αναπτύσσεται συνήθως περίπου 5-10 ημέρες μετά τα πρώτα συμπτώματα, αλλά μπορεί να χρειαστούν έως και 3 εβδομάδες για να εκδηλωθεί και να εμφανιστεί σε μια περίοδο που η διάρροια βελτιώνεται. Τα σχετικά συμπτώματα και σημεία περιλαμβάνουν λήθαργο, μειωμένη παραγωγή ούρων, αίμα στα ούρα, νεφρική ανεπάρκεια, ελαττωμένα αιμοπετάλια (τα οποία χρειάζονται για την πήξη του αίματος) και καταστροφή των ερυθρών αιμοσφαιρίων (μικροαγγειοπαθητική αιμολυτική αναιμία). Υψηλή αρτηριακή πίεση, ίκτερος, επιληπτικές κρίσεις και αιμορραγία στο δέρμα μπορεί επίσης να εμφανιστούν. Σε ορισμένες περιπτώσεις, υπάρχουν εμφανείς νευρολογικές αλλαγές.[7][8]
Τα άτομα που πάσχουν παρουσιάζουν συνήθως τα συμπτώματα της θρομβωτικής μικροαγγειοπάθειας (TMA), τα οποία μπορεί να περιλαμβάνουν κοιλιακό άλγος, χαμηλό αριθμό αιμοπεταλίων,[9] αυξημένη γαλακτική αφυδρογονάση LDH, (ένα ένζυμο που απελευθερώνεται από κατεστραμμένα κύτταρα και επομένως είναι δείκτης κυτταρικής βλάβης)[10] μειωμένη απτοσφαιρίνη (ενδεικτικό της διάσπασης των ερυθρών αιμοσφαιρίων), αναιμία (χαμηλός αριθμός ερυθρών αιμοσφαιρίων), σχιστοκύτταρα (κατεστραμμένα ερυθρά αιμοσφαίρια), αυξημένη κρεατινίνη ( προϊόν που δημιουργείται από το μεταβολισμό των μυών και αποβάλλεται από τους νεφρούς),[11] πρωτεϊνουρία (ενδεικτικό νεφρικής βλάβης),[12] σύγχυση, κόπωση, οίδημα, ναυτία/έμετος, και διάρροια. Επιπλέον, οι ασθενείς με άτυπο αιμολυτικό ουραιμικό σύνδρομο παρουσιάζουν τυπικά μια απότομη έναρξη συμπτωμάτων όπως οξεία νεφρική ανεπάρκεια, υπέρταση, έμφραγμα του μυοκαρδίου (καρδιακή προσβολή), εγκεφαλικό, πνευμονικές επιπλοκές, παγκρεατίτιδα (φλεγμονή του παγκρέατος), ηπατική νέκρωση (θάνατος ηπατικών κυττάρων ή ιστών), εγκεφαλοπάθεια (εγκεφαλική δυσλειτουργία), επιληπτικές κρίσεις, και κώμα .[13] Η ανεπάρκεια νευρολογικών, καρδιακών, νεφρικών και γαστρεντερικών οργάνων, καθώς και ο θάνατος, μπορεί να συμβεί απρόβλεπτα ανά πάσα στιγμή, είτε πολύ γρήγορα είτε μετά από παρατεταμένη συμπτωματική ή ασυμπτωματική εξέλιξη της νόσου.[14]
Παθογένεση
[Επεξεργασία | επεξεργασία κώδικα]
Το σύνδρομο προκαλείται από την εισβολή βακτηρίων που παράγουν τοξίνες Shiga, με τον πιο κοινό τύπο να είναι το βακτήριο E. coli που παράγει Shiga-toxin (STEC).[15] Το E. coli μπορεί να παράγει σιγατοξίνη-1, σιγατοξίνη-2 ή και τα δύο με τα βακτήρια που παράγουν σιγατοξίνη-2 να είναι πιο μολυσματικά και να είναι πολύ πιο πιθανό να προκαλέσουν το σύνδρομο.[15] Μόλις καταποθούν, τα βακτήρια μετακινούνται στα έντερα όπου παράγουν τις τοξίνες Shiga. Τα βακτήρια και οι τοξίνες βλάπτουν τη βλεννογόνο επένδυση των εντέρων, και έτσι μπορούν να εισέλθουν στην κυκλοφορία του αίματος.[15] Η τοξίνη Shiga εισέρχεται στη μεσεντερική μικροαγγείωση που καλύπτει τα έντερα όπου απελευθερώνει φλεγμονώδεις κυτοκίνες συμπεριλαμβανομένων των IL-6, IL-8, TNFa και IL-1β. Αυτές οδηγούν σε φλεγμονή και αγγειακό τραυματισμό με μικροθρόμβους που παρατηρούνται στο σύνδρομο. Επίσης, καταστρέφει περαιτέρω τον εντερικό φραγμό που οδηγεί σε διάρροια (συνήθως αιματηρή) και περαιτέρω είσοδο της τοξίνης Shiga από τα έντερα στην κυκλοφορία του αίματος.[15]
Μόλις η τοξίνη Shiga εισέλθει στην κυκλοφορία, μπορεί να ταξιδέψει σε όλο το σώμα και να προκαλέσει ευρεία γκάμα βλαβών των τελικών οργάνων και πλήθος συμπτωμάτων που παρατηρούνται με το αιμολυτικό ουραιμικό σύνδρομο. Η τοξίνη Shiga εισέρχεται στα κύτταρα δεσμεύοντας το γλοβοτριαοσυλοκεραμίδιο (Gb3) που βρίσκεται στις κυτταρικές μεμβράνες και σε όλο το σώμα συμπεριλαμβανομένης της επιφάνειας του σπειραματικού ενδοθηλίου του νεφρού. Η τοξίνη Shiga εισέρχεται στο κύτταρο μέσω του Gb3 και ενδοκυττάρωσης, στη συνέχεια μεταφέρεται στο σωμάτιο Golgi όπου η φουρίνη διασπά την υπομονάδα Α της τοξίνης Shiga.[15] Στη συνέχεια μεταφέρεται στο ενδοπλασματικό δίκτυο όπου διασπάται περαιτέρω, αφήνοντας ελεύθερη την υπομονάδα Α1 της τοξίνης Shiga. Η υπομονάδα Α1 της τοξίνης Shiga αναστέλλει την υπομονάδα 28s του ριβοσωμικού rRNA και αυτό οδηγεί σε αναστολή της παραγωγής πρωτεΐνης από τα ριβοσώματα.[15] Με την αναστολή της πρωτεϊνικής σύνθεσης του κυττάρου από την τοξίνη Shiga, το κύτταρο καταστρέφεται.[15] Αυτό οδηγεί σε αγγειακό τραυματισμό (συμπεριλαμβανομένων των νεφρών όπου συγκεντρώνεται το Gb3). Ο αγγειακός τραυματισμός διευκολύνει τον σχηματισμό αγγειακών μικροθρόμβων που είναι χαρακτηριστικά της Θρομβωτικής θρομβοπενικής πορφύρας (TTP). Το TTP οδηγεί σε παγίδευση αιμοπεταλίων (και θρομβοπενία), καταστροφή ερυθρών αιμοσφαιρίων (και αναιμία) και βλάβη των τελικών οργάνων που παρατηρείται χαρακτηριστικά και με το αιμολυτικό ουραιμικό σύνδρομο. Η παρουσία σχιστοκυττάρων είναι ένα βασικό εύρημα που βοηθά στη διάγνωση του συνδρόμου.
Η Shiga-τοξίνη προκαλεί ενεργοποίηση αιμοπεταλίων, λευκοκυττάρων και ενδοθηλιακών κυττάρων με αποτέλεσμα συστηματική αιμόλυση, φλεγμονή και θρόμβωση.
Ο αριθμός των αιμοπεταλίων μειώνεται καθώς προσκολλώνται στους θρόμβους που βρίσκονται στα μικρά αγγεία.[16] Όπως και στη σχετική πάθηση TTP, η μειωμένη ροή αίματος μέσω των στενωμένων αιμοφόρων αγγείων του μικροαγγειακού συστήματος οδηγεί σε μειωμένη ροή αίματος στα ζωτικά όργανα και μπορεί να αναπτυχθεί ισχαιμία.[17] Οι νεφροί και το κεντρικό νευρικό σύστημα (εγκέφαλος και νωτιαίος μυελός) είναι τα μέρη του σώματος που εξαρτώνται περισσότερο από την υψηλή ροή αίματος, και επομένως είναι τα πιο πιθανά όργανα που επηρεάζονται. Ωστόσο, σε σύγκριση με τη Θρομβωτική θρομβοπενική πορφύρας , οι νεφροί τείνουν να επηρεάζονται πιο σοβαρά στο Αιμολυτικό ουραιμικό σύνδρομο και το κεντρικό νευρικό σύστημα επηρεάζεται λιγότερο συχνά.
Το σύνδρομο εμφανίζεται μετά από το 3–7% όλων των σποραδικών λοιμώξεων από E. coli O157:H7 και έως περίπου το 20% ή περισσότερο των επιδημικών λοιμώξεων.[18] Τα παιδιά και οι έφηβοι προσβάλλονται συνήθως και ένας λόγος θα μπορούσε να είναι ότι τα παιδιά έχουν περισσότερους υποδοχείς Gb3 από τους ενήλικες. Τα βοοειδή, οι χοίροι, τα ελάφια και άλλα θηλαστικά δεν έχουν υποδοχείς GB3, αλλά μπορεί να είναι ασυμπτωματικοί φορείς βακτηρίων που παράγουν τοξίνες Shiga. Μερικοί άνθρωποι μπορεί επίσης να είναι ασυμπτωματικοί φορείς.
Σε μεγάλο βαθμό, οι νεφροί μπορεί να εμφανίσουν αποσπασματική ή διάχυτη νέκρωση του φλοιού τους. Ιστολογικά, τα σπειράματα εμφανίζουν πυκνά και μερικές φορές σχισμένα τριχοειδικά τοιχώματα που οφείλονται σε μεγάλο βαθμό στο ενδοθηλιακό οίδημα.[19]
Το σύνδρομο επηρεάζει συχνότερα βρέφη και μικρά παιδιά, αλλά εμφανίζεται και σε ενήλικες. Η πιο κοινή μορφή μετάδοσης είναι η κατάποση όχι επαρκώς μαγειρεμένου κρέατος, μη παστεριωμένων φρούτων και χυμών, μολυσμένων προϊόντων, επαφή με μη χλωριούχο νερό και μετάδοση από άτομο σε άτομο σε παιδικούς σταθμούς ή εγκαταστάσεις μακροχρόνιας φροντίδας.[13]
Πρόληψη
[Επεξεργασία | επεξεργασία κώδικα]Η επίδραση των αντιβιοτικών στην τοξίνη shiga που παράγει E. coli είναι ασαφής.[1]
Θεραπεία
[Επεξεργασία | επεξεργασία κώδικα]Η θεραπεία περιλαμβάνει υποστηρικτική φροντίδα και μπορεί να περιλαμβάνει αιμοκάθαρση, χορήγηση στεροειδών, μεταγγίσεις αίματος και πλασμαφαίρεση.[1] Η πρώιμη ενδοφλέβια θεραπεία δηλαδή η χορήγηση θρεπτικών συστατικών και ενυδάτωσης απευθείας στην κυκλοφορία του αίματος σχετίζεται με καλύτερα αποτελέσματα, συμπεριλαμβανομένων μικρότερης διάρκειας παραμονής στο νοσοκομείο και μείωση του κινδύνου αιμοκάθαρσης.[15] Τα εμπειρικά αντιβιοτικά δεν ενδείκνυνται σε όσους είναι ανοσοεπαρκείς και μπορεί να επιδεινώσουν τα συμπτώματα.
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 Cody, Ellen M.; Dixon, Bradley P. (2019-02). «Hemolytic Uremic Syndrome» (στα αγγλικά). Pediatric Clinics of North America 66 (1): 235–246. doi:. https://linkinghub.elsevier.com/retrieve/pii/S0031395518301494.
- ↑ 2,0 2,1 Salvadori, Maurizio (2013). «Update on hemolytic uremic syndrome: Diagnostic and therapeutic recommendations» (στα αγγλικά). World Journal of Nephrology 2 (3): 56. doi:. ISSN 2220-6124. PMID 24255888. PMC PMC3832913. http://www.wjgnet.com/2220-6124/full/v2/i3/56.htm.
- ↑ Benz, Kerstin; Amann, Kerstin (2010-05). «Thrombotic microangiopathy: new insights:» (στα αγγλικά). Current Opinion in Nephrology and Hypertension 19 (3): 242–247. doi:. ISSN 1062-4821. http://journals.lww.com/00041552-201005000-00004.
- ↑ Noris, Marina; Remuzzi, Giuseppe (2009-10-22). «Atypical Hemolytic–Uremic Syndrome» (στα αγγλικά). New England Journal of Medicine 361 (17): 1676–1687. doi:. ISSN 0028-4793. http://www.nejm.org/doi/abs/10.1056/NEJMra0902814.
- ↑ Gasser, C.; Gautier, E.; Steck, A.; Siebenmann, R. E.; Oechslin, R. (1955-09-20). «[Hemolytic-uremic syndrome: bilateral necrosis of the renal cortex in acute acquired hemolytic anemia»]. Schweizerische Medizinische Wochenschrift 85 (38-39): 905–909. ISSN 0036-7672. PMID 13274004. https://pubmed.ncbi.nlm.nih.gov/13274004/.
- ↑ 6,0 6,1 «Symptoms | E. coli | CDC». www.cdc.gov (στα Αγγλικά). 2 Φεβρουαρίου 2021. Ανακτήθηκε στις 12 Φεβρουαρίου 2024.
- ↑ Boyer, Olivia; Niaudet, Patrick (2011). «Hemolytic Uremic Syndrome: New Developments in Pathogenesis and Treatment» (στα αγγλικά). International Journal of Nephrology 2011: 1–10. doi:. ISSN 2090-2158. PMID 21876803. PMC PMC3159990. Αρχειοθετήθηκε από το πρωτότυπο στις 2024-05-19. https://web.archive.org/web/20240519145307/https://www.hindawi.com/journals/ijn/2011/908407/. Ανακτήθηκε στις 2024-02-12.
- ↑ Nathanson, Sylvie; Kwon, Thérésa; Elmaleh, Monique; Charbit, Marina; Launay, Emma Allain; Harambat, Jérôme; Brun, Muriel; Ranchin, Bruno και άλλοι. (2010-07). «Acute Neurological Involvement in Diarrhea-Associated Hemolytic Uremic Syndrome» (στα αγγλικά). Clinical Journal of the American Society of Nephrology 5 (7): 1218. doi:. ISSN 1555-905X. https://journals.lww.com/cjasn/fulltext/2010/07000/acute_neurological_involvement_in.10.aspx.
- ↑ Loirat, Chantal; Noris, Marina; Fremeaux-Bacchi, Véronique (2008-11). «Complement and the atypical hemolytic uremic syndrome in children» (στα αγγλικά). Pediatric Nephrology 23 (11): 1957–1972. doi:. ISSN 0931-041X. PMID 18594873. PMC PMC6904381. http://link.springer.com/10.1007/s00467-008-0872-4.
- ↑ Caprioli, Jessica; Noris, Marina; Brioschi, Simona; Pianetti, Gaia; Castelletti, Federica; Bettinaglio, Paola; Mele, Caterina; Bresin, Elena και άλλοι. (2006-08-15). «Genetics of HUS: the impact of MCP, CFH, and IF mutations on clinical presentation, response to treatment, and outcome» (στα αγγλικά). Blood 108 (4): 1267–1279. doi:. ISSN 0006-4971. PMID 16621965. PMC PMC1895874. https://ashpublications.org/blood/article/108/4/1267/22428/Genetics-of-HUS-the-impact-of-MCP-CFH-and-IF.
- ↑ Ariceta, Gema; Besbas, Nesrin; Johnson, Sally; Karpman, Diana; Landau, Daniel; Licht, Christoph; Loirat, Chantal; Pecoraro, Carmine και άλλοι. (2009-04-01). «Guideline for the investigation and initial therapy of diarrhea-negative hemolytic uremic syndrome» (στα αγγλικά). Pediatric Nephrology 24 (4): 687–696. doi:. ISSN 1432-198X. https://doi.org/10.1007/s00467-008-0964-1.
- ↑ Sellier-Leclerc, Anne-Laure; Fremeaux-Bacchi, Veronique; Dragon-Durey, Marie-Agnès; Macher, Marie-Alice; Niaudet, Patrick; Guest, Geneviève; Boudailliez, Bernard; Bouissou, Franc[COMBINING CEDILLA]ois και άλλοι. (2007-08). «Differential Impact of Complement Mutations on Clinical Characteristics in Atypical Hemolytic Uremic Syndrome» (στα αγγλικά). Journal of the American Society of Nephrology 18 (8): 2392. doi:. ISSN 1046-6673. https://journals.lww.com/jasn/fulltext/2007/08000/differential_impact_of_complement_mutations_on.26.aspx.
- ↑ 13,0 13,1 Noris, Marina; Remuzzi, Giuseppe (2005-04). «Hemolytic Uremic Syndrome» (στα αγγλικά). Journal of the American Society of Nephrology 16 (4): 1035–1050. doi:. ISSN 1046-6673. https://journals.lww.com/00001751-200504000-00030.
- ↑ Mache, Christoph J.; Acham-Roschitz, Birgit; Frémeaux-Bacchi, Veronique; Kirschfink, Michael; Zipfel, Peter F.; Roedl, Siegfried; Vester, Udo; Ring, Ekkehard (2009-08). «Complement Inhibitor Eculizumab in Atypical Hemolytic Uremic Syndrome» (στα αγγλικά). Clinical Journal of the American Society of Nephrology 4 (8): 1312–1316. doi:. ISSN 1555-9041. PMID 19556379. PMC PMC2723971. https://journals.lww.com/01277230-200908000-00005.
- ↑ 15,0 15,1 15,2 15,3 15,4 15,5 15,6 15,7 Freedman, Stephen B.; van de Kar, Nicole C.A.J.; Tarr, Phillip I. (2023-10-12). Ingelfinger, Julie R., επιμ. «Shiga Toxin–Producing Escherichia coli and the Hemolytic–Uremic Syndrome» (στα αγγλικά). New England Journal of Medicine 389 (15): 1402–1414. doi:. ISSN 0028-4793. http://www.nejm.org/doi/10.1056/NEJMra2108739.
- ↑ Hemolytic Uremic Syndrome in Emergency Medicine: Practice Essentials, Pathophysiology, Epidemiology. 2023-06-30. https://emedicine.medscape.com/article/779218-overview.
- ↑ Boyer, Olivia; Niaudet, Patrick (2011). «Hemolytic Uremic Syndrome: New Developments in Pathogenesis and Treatment». International Journal of Nephrology 2011: 908407. doi:. ISSN 2090-214X. PMID 21876803. PMC 3159990. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3159990/.
- ↑ (στα αγγλικά) Escherichia coli O157:H7. doi:. https://zenodo.org/records/1259827.
- ↑ Internet Archive (2003). Robbins basic pathology. Philadelphia, PA : Saunders. ISBN 978-0-7216-9274-6.