Λοιμώδης ενδοκαρδίτιδα
| Λοιμώδης ενδοκαρδίτιδα | |
|---|---|
 Εκβλάστηση μιτροειδούς βαλβίδας σε λοιμώδη ενδοκαρδίτιδα | |
| Ειδικότητα | Καρδιολογία και λοιμωξιολογία |
| Συμπτώματα | φλεγμονή[1], πυρετός, Πετέχεια, heart murmur και αναιμία |
| Ταξινόμηση | |
| ICD-10 | I33 |
| ICD-9 | 421.0-421.1 |
| MedlinePlus | 000681 |
| MeSH | D004696 |
Η λοιμώδης ενδοκαρδίτιδα είναι μια μορφή ενδοκαρδίτιδας, δηλαδή φλεγμονής του ενδοκάρδιου και των καρδιακών βαλβίδων, που προκαλείται από λοιμώδεις παράγοντες.
Οι καρδιακές βαλβίδες δεν έχουν δική τους αιμάτωση. Αυτό έχει ως αποτέλεσμα οι ανοσιακοί αμυντικοί μηχανισμοί (όπως τα λευκά αιμοσφαίρια) να μην έχουν πρόσβαση σε αυτές μέσω της αιματικής ροής. Αν ένας μικροοργανισμός (όπως τα βακτήρια) προσεγγίσει την επιφάνεια μιας βαλβίδας και σχηματίσει μια εκβλάστηση, η ανοσιακή απάντηση του ξενιστή είναι ελαττωμένη. Η έλλειψη αιματικής παροχής στις βαλβίδες έχει επιπτώσεις και στη θεραπεία, καθώς ούτε τα φάρμακα έχουν πρόσβαση στην προσβεβλημένη βαλβίδα.
Φυσιολογικά το αίμα έχει ομαλή ροή όταν περνά διαμέσου των βαλβίδων. Αν όμως έχουν καταστραφεί, π.χ. από ρευματικό πυρετό, αυξάνεται η πιθανότητα μικροβιακής προσβολής.[2]
Ταξινόμηση
[Επεξεργασία | επεξεργασία κώδικα]Ανάλογα με τη χρονική εξέλιξη
[Επεξεργασία | επεξεργασία κώδικα]Ιστορικά, η λοιμώδης ενδοκαρδίτιδα διακρίνεται κλινικά σε οξεία και υποξεία[2] (επειδή χωρίς θεραπεία οι ασθενείς με υποξεία νόσο τείνουν να ζουν περισσότερο σε αντίθεση με αυτούς που πάσχουν από οξεία). Αυτή η ταξινόμηση αναφέρεται τόσο στην εξέλιξη όσο και στη σοβαρότητα της νόσου.
- Η υποξεία βακτηριακή ενδοκαρδίτιδα συχνά οφείλεται σε στρεπτόκοκκους χαμηλής λοιμογόνου δράσης και προκαλεί νόσο ήπιας έως μέτριας βαρύτητας, που εξελίσσεται αργά για εβδομάδες και μήνες και σπάνια προσβάλλει αιματογενώς εξωκαρδιακές θέσεις.
- Η οξεία βακτηριακή ενδοκαρδίτιδα είναι κεραυνοβόλος νόσος που εξελίσσεται μέσα σε μέρες ή eβδομάδες και συνήθως οφείλεται σε χρυσίζοντα σταφυλόκοκκο (Staphylococcus aureus), που έχει πολύ ισχυρότερη λοιμογόνο δράση και ικανότητα πρόκλησης νόσου, ενώ συχνά προκαλεί μεταστατική λοίμωξη.[2]
Αυτή η ορολογία τίθεται πλέον υπό αμφισβήτηση, επειδή οι συσχετισμοί της (σε σχέση με τους οργανισμούς και την πρόγνωση) δεν τεκμηριώνονται κλινικά. Προτιμώνται οι όροι σύντομης επώασης (δηλαδή κάτω από 6 εβδομάδες) και μακράς επώασης (πάνω από 6 εβδομάδες).[3]
Ανάλογα με τα αποτελέσματα από τις καλλιέργειες
[Επεξεργασία | επεξεργασία κώδικα]Η λοιμώδης ενδοκαρδίτιδα μπορεί να ταξινομηθεί επίσης ως ενδοκαρδίτιδα με θετική καλλιέργεια και με αρνητική καλλιέργεια αίματος. Η ενδοκαρδίτιδα με αρνητική καλλιέργεια μπορεί να οφείλεται σε μικροοργανισμούς που απαιτούν μεγαλύτερο χρονικό διάστημα μέχρι να ταυτοποιηθούν στο εργαστήριο (τέτοιοι μικροοργανισμοί αποκαλούνται απαιτητικοί διότι απαιτούν ειδικό περιβάλλον για να αναπτυχθούν) ή να μην οφείλονται σε μικροβιακό παράγοντα, όπως στην μαραντική ενδοκαρδίτιδα. Στα παθογόνα που προκαλούν ενδοκαρδίτιδα με αρνητική καλλιέργεια περιλαμβάνονται: Aspergillus sp., Brucella sp., Coxiella burnetii, Chlamydia sp. και βακτήρια της ομάδας HACEK (Haemophilus spp., Actinobacillus actinomycetemcomitans, Cardiobacterium hominis, Eikenella spp. και Kingella kingae). Ένα άλλο αίτιο ενδοκαρδίτιδας με αρνητική καλλιέργεια, ακόμη και οφειλόμενη σε συνήθη μικρόβια, είναι η προηγηθείσα αντιμικροβιακή θεραπεία.
Ανάλογα με την καρδιακή πλευρά
[Επεξεργασία | επεξεργασία κώδικα]Η ενδοκαρδίτιδα διακρίνεται επίσης από την πλευρά της καρδιάς που προσβάλλει:
- Στους χρήστες ενδοφλέβιων ναρκωτικών ή αλλων φαρμάκων μπορεί να εισαχθούν μικρόβια, τα οποία ταξιδεύουν στη δεξιά καρδιά προσβάλλοντας τυπικά την τριγλώχινα βαλβίδα. Τις περισσότερς φορές αίτιο είναι ο Staphylococcus aureus.[2]
- Στους υπόλοιπους ασθενείς, χωρίς ιστορικό ενδοφλέβιας έκθεσης, η ενδοκαρδίτιδα αφορά πιο συχνά την αριστερή καρδιά.[2]
Ανάλογα με το είδος της λοίμωξης
[Επεξεργασία | επεξεργασία κώδικα]Μια άλλη μορφή ενδοκαρδίτιδας ειναι η ενδονοσοκομειακή, η οποία υφίσταται όταν διαγιγνώσκεται ενδοκαρδίτιδα σε ασθενή που έτυχε νοσοκομειακής περίθαλψης έως ένα μήνα πριν το συμβάν και είναι συνήθως επακόλουθο μόλυνσης ενδαγγειακών καθετήρων, γραμμών ολικής παρεντερικής διατροφής, βηματοδότη κλπ.[4]
Ανάλογα με τον τύπο της βαλβίδας
[Επεξεργασία | επεξεργασία κώδικα]Τέλος, σημαντική στην κλινική πράξη είναι η διάκριση μεταξύ ενδοκαρδίτιδας φυσικής βαλβίδας και ενδοκαρδίτιδας προσθετικής βαλβίδας. Η ενδοκαρδίτιδα προσθετικής βαλβίδας μπορεί να είναι πρώιμη (<60 μέρες από την εγχείρηση της βαλβίδας) ή όψιμη (>60 μέρες από την εγχείρηση της βαλβίδας).
- Η πρώιμη ενδοκαρδίτιδα προσθετικής βαλβίδας οφείλεται συνήθως σε διεγχειρητική ή μετεγχειρητική μικροβιακή επιμόλυνση, που είναι συνήθως ενδονοσοκομιακή.
- Η όψιμη ενδοκαρδίτιδα προσθετικής βαλβίδας οφείλεται συνήθως σε μικρόβια της κοινότητας.[4]
Σημεία και συμπτώματα
[Επεξεργασία | επεξεργασία κώδικα]- Πυρετός: πυρετός παρατηρείται στο 97% των ασθενών, αδιαθεσία και καταβολή δυνάμεων στο 90% των ασθενών.[5]
- Νέο ή επιδεινωμένο καρδιακό φύσημα, απώλεια βάρους και βήχας παρατηρείται στο 35% των ασθενών.[5]
- Αγγειακά φαινόμενα: σηπτικές εμβολές (που προκαλούν θρομβοεμβολικά φαινόμενα όπως έμφρακτο του βρεγματικού λοβού του εγκεφάλου ή γάγγραινα των δακτύλων), βλάβες Janeway (ανώδυνες αιμορραγικές δερματικές βλάβες στις παλάμες και τα πέλματα), ενδοκράνια αιμορραγία, υπωνύχιες αιμορραγίες, έμφρακτο νεφρού και έμφρακτο σπλήνα.
- Ανοσολογικά φαινόμενα: σπειραματονεφρίτιδα, που επιτρέπει στο αίμα και τα λευκώματα να αποβάλλονται στα ούρα,[2] οζίδια του Osler (επώδυνες υποδόριες βλάβες στις ράγες των δακτύλων), κηλίδες του Roth στον αμφιβληστροειδή, θετικός ρευματοειδής παράγοντας στον ορό.
- Άλλα σημεία που μπορεί να παρατηρούνται είναι νυχτερινοί ιδρώτες, ρίγη, αναιμία, σπληνομεγαλία και πληκτροδακτυλία.
Αιτιολογία
[Επεξεργασία | επεξεργασία κώδικα]Σε ένα υγιές άτομο, μια βακτηριαιμία (όπου τα βακτήρια εισέρχονται στην κυκλοφορία μέσω μιας αμυχής ή πληγής) μπορεί φυσιολογικά να αντιμετωπιστεί γρήγορα χωρίς δυσμενείς επιπτώσεις. Όταν όμως μια καρδιακή βαλβίδα είναι αλλοιωμένη και καλυμμένη από θρόμβο αίματος, δίνει έδαφος στα βακτήρια να προσκολληθούν και να αναπτύξουν λοίμωξη.
Στο παρελθόν αποδόθηκε στην βακτηριαιμία που προκαλείται από οδοντιατρικές επεμβάσεις (στην πλειονότητα των περιπτώσεων οφειλόμενη σε πρασινίζοντα στρεπτόκοκκο, που αποτελεί φυσιολογική χλωρίδα της στοματικής κοιλότητας), όπως καθαρισμός ή εξαγωγή δοντιού, μεγαλύτερη κλινική σημασία από ότι έχει στην πραγματικότητα. Παρ' όλα αυτά είναι σημαντικό ο οδοντίατρος ή ο υγιεινολόγος στόματος να ενημερώνεται για τυχόν καρδιακά προβλήματα πριν ξεκινήσει μια θεραπεία. Αντιβιοτικά χορηγούνται σε ασθενείς με συγκεκριμένα καρδιακά προβλήματα ως προφύλαξη, παρόλο που αυτή η πρακτική έχει αλλάξει στις ΗΠΑ, με τις νέες κατευθυντήριες οδηγίες της Αμερικανικής Καρδιολογικής Εταιρίας του 2007,[6] όπως και στο Ηνωμένο Βασίλειο από το Μάρτιο του 2008, λόγων των νέων οδηγιών της NICE. Δεν υπάρχουν επαρκή στοιχεία που να υποστηρίζουν την γενικευμένη αντιβιοτική προφύλαξη για τις οδοντιατρικές θεραπείες, γεγονός που αντανακλάται στις πρόσφατες κατευθυντήριες οδηγίες, που την επιφυλάσσουν μόνο στους ασθενείς υψηλού κινδύνου. Καθημερινό βούρτσισμα και χρήση οδοντικού νήματος μπορεί ομοίως να προκαλέσει βακτηριαιμία.
Μια άλλη αιτιολογική ομάδα σχετίζεται με την είσοδο μεγάλου αριθμού μικροβίων στην αιματική κυκλοφορία. Ο ορθοκολικός καρκίνος (Streptococcus bovis), οι σοβαρές λοιμώξεις της ουροφόρας οδού (κυρίως από εντερόκοκκο) και η ενδοφλέβια χορήγηση φαρμάκων (St. aureus) είναι τα κύρια αίτια. Με την είσοδο τόσο μεγάλου πληθυσμού βακτηρίων ακόμη και μια φυσική καρδιακή βαλβίδα μπορεί να προσβληθεί. Ένας ισχυρά λοιμογόνος μικροοργανισμός (όπως ο St. aureus) ευθύνεται συνήθως για τη λοίμωξη φυσικών καρδιακών βαλβίδων.
Στους χρήστες ενδοφλέβιων ναρκωτικών προσβάλλονται συνήθως οι δεξιές βαλβίδες, καθώς το αίμα από τις φλέβες όπου γίνεται η έγχυση οδηγείται στη δεξιά καρδιά. Στη ρευματική καρδιακή νόσο η λοίμωξη αφορά την αορτική και την μιτροειδή βαλβίδα, στην αριστερή πλευρά της καρδιάς.
Άλλοι παράγοντες κινδύνου για ανάπτυξη ενδοκαρδίτιδας είναι η λευκοπενία, η ανοσοανεπάρκεια ή ανοσοκαταστολή, οι κακοήθεις νόσοι, ο σακχαρώδης διαβήτης και η κατάχρηση αλκοόλ.[2]
Παθογένεια
[Επεξεργασία | επεξεργασία κώδικα]Όπως προαναφέρθηκε, η ανώμαλη αιματική ροή γύρω από τις βαλβίδες αποτελεί παράγοντα κινδύνου για την εγκατάσταση ενδοκαρδίτιδας. Η βλάβη των βαλβίδων μπορεί να οφείλεται σε συγγενή διαμαρτία, να είναι αποτέλεσμα χειρουργικής επέμβασης, αυτοάνοσων μηχανισμών ή απλά συνέπεια μεγάλης ηλικίας. Το προσβεβλημένο τμήμα της καρδιακής βαλβίδας καλύπτεται από αιματικό θρόμβο, μια κατάσταση που ειναι γνωστή ως μη μικροβιακή θρομβωτική ενδοκαρδίτιδα (ΜΜΘΕ). Η ανώμαλη αιματική ροή και μέσω αυτής η ενδοκαρδίτιδα είναι πιο συχνή σε περιοχές με υψηλές πιέσεις. Συνεπώς, οι μεσοκοιλιακές επικοινωνίες είναι πιο ευάλωτες από ότι οι μεσοκολπικες επικοινωνίες. Το αλλοιωμένο ενδοθήλιο προάγει επίσης την εναπόθεση αιμοπεταλίων και ινώδους, πάνω στα οποία μπορούν να προσκολληθούν τα μικρόβια. Οι βαλβιδικές αλλοιώσεις είναι ένα πρωτεύον αίτιο τέτοιας βλάβης, όπως και οι ενδοθηλιακές βλάβες λόγω πρόσκρουσης πιδάκων αίματος υψηλής ταχύτητας, συνέπεια μεσοκοιλιακής επικοινωνίας ή παραμονής ανοικτού αρτηριακού πόρου.
Διάγνωση
[Επεξεργασία | επεξεργασία κώδικα]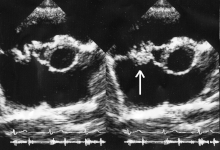
Σε γενικές γραμμές ένας ασθενής πρέπει να πληροί τα κριτήρια του Duke προκειμένου να τεθεί η διάγνωση της λοιμώδους ενδοκαρδίτιδας. [7]
Καθώς τα κριτήρια του Duke βασίζονται σε ηχοκαρδιογραφικά ευρήματα, μελέτες ορίζουν πότε πρέπει να γίνεται ηχοκαρδιογραφικός έλεγχος, χρησιμοποιώντας σημεία και συμπτώματα για να προβλέψουν τη λανθάνουσα ενδοκαρδίτιδα σε ασθενείς που είναι χρήστες ενδοφλέβιων ναρκωτικών[8][9][10] και σε ασθενείς που δεν είναι.[11][12] Δυστυχώς αυτή η μελέτη έχει ηλικία άνω των 20 χρόνων και είναι πιθανό αλλαγές στην επιδημιολογία της ενδοκαρδίτιδας και των βακτηρίων (όπως ο σταφυλόκοκκος) να καθιστούν τις ακόλουθες εκτιμήσεις λανθασμένες.
Σε ασθενείς που δεν είναι χρήστες ενδοφλέβιων ναρκωτικών και έχουν πυρετό στα επείγοντα, υπάρχει κάτω από 5% πιθανότητα λανθάνουσας ενδοκαρδίτιδας. Ο Mellors το 1987 δεν βρήκε καμιά περίπτωση ενδοκαρδίτιδας ούτε σταφυλοκοκκικής βακτηριαιμίας σε 135 ασθενείς με εμπύρετο στην αίθουσα επειγόντων.[12] Το ανώτερο διάστημα εμπιστοσύνης για το 0% σε δείγμα 135 είναι 5%, έτσι για στατιστικούς λόγους και μόνο, θεωρείται ότι υπάρχει 5% πιθανότητα ενδοκαρδίτιδας σε αυτούς τους ασθενείς. Αντίθετα, ο Leibovici παρατήρησε ότι σε 113 μη επιλεγμένους ενήλικες που προσήλθαν στο νοσοκομείο λόγω πυρετού υπήρχαν δύο περιπτώσεις (1,8% με 95% ΔΕ: 0%-7%) ενδοκαρδίτιδας.[11]
Σε ασθενείς που είναι χρήστες ενδοφλέβιων ναρκωτικών και έχουν πυρετό στα επέιγοντα, ο επιπολασμός της ενδοκαρδίτιδας είναι περίπου 10%-15%. Η εκτίμηση αυτή δεν αναιρείται ακόμα και αν ο ιατρός θεωρεί ότι ο ασθενής πάσχει από σύνηθες αίτιο πυρετού.[10] Ο Weisse αναφέρει ότι το 13% σε 121 τέτοιους ασθενείς έπασχε από ενδοκαρδίτιδα.[8] Ο Marantz επίσης αναφέρει επιπολασμό ενδοκαρδίτιδας σε ποσοστό 13% σε αυτούς τους ασθενείς που προσέρχονται με πυρετό στα επείγοντα.[10] Ο Samet αναφέρει μία επίπτωση ενδοκαρδίτιδας 6% σε δείγμα 283 τέτοιων ασθενών, αλλά μετά των αποκλεισμό εκείνων στους οποίους προέκυπτε εξαρχής μείζων νόσος που να δικαιολογεί τον πυρετό (συμπεριλαμβανομένων 11 ασθενών με φανερή ενδοκαρδίτιδα), το ποσοστό ανέρχεται στο 7%.[9]
Σε ασθενείς με σταφυλοκοκκική μικροβιαιμία, μία μελέτη αναφέρει 29% επιπολασμό ενδοκαρδίτιδας σε σταφυλοκοκκική μικροβιαιμία της κοινότητας έναντι 5% σε ενδονοσοκομειακή.[13] Παρ' όλα αυτά μόνο το 2% των στελεχών ήταν ανθεκτικά στη μεθικιλλίνη και άρα αυτά τα ποσοστά μπορεί να είναι χαμηλά σε περιοχές με μεγαλύτερη ανθεκτικότητα.
Ηχοκαρδιογραφία
[Επεξεργασία | επεξεργασία κώδικα]Το διαθωρακικό ηχοκαρδιογράφημα έχει ευαισθησία και ειδικότητα περίπου 65% και 95% αντίστοιχα, όταν ο ιατρός που το διεξάγει θεωρεί ότι υπάρχουν πιθανές ή σχεδόν βέβαιες ενδείξεις ενδοκαρδίτιδας.[14][15]
Τα κριτήρια του Duke
[Επεξεργασία | επεξεργασία κώδικα]Καθιερωμένα το 1994 από την Duke Endocarditis Society και αναθεωρημένα το 2000, τα κριτήρια του Duke αποτελούνται από μείζονα και ελάσσονα κριτήρια που χρησιμοποιούνται για να τεθεί διάγνωση ενδοκαρδίτιδας.[7] Η διάγνωση τίθεται με έναν από τους τρεις τρόπους: όταν εκπληρώνονται 2 μείζονα, 1 μείζον και 3 ελάσσονα ή 5 ελάσσονα κριτήρια.
Μείζονα κριτήρια:
- Θετική καλλιέργεια αίματος σε μικροοργανισμό τυπικό για λοιμώδη ενδοκαρδίτιδα, που ορίζεται ως εξής:
- Τυπικός μικροοργανισμός για λοιμώδη ενδοκαρδίτιδα σε δύο διαφορετικές καλλιέργειες αίματος, όπως:
- Πρασινίζοντες στρεπτόκοκκοι ή
- Streptococcus bovis ή
- Ομάδας HACEK ή
- Staphylococcus aureus ή
- Εξωνοσοκομειακός εντερόκοκκος εν απουσία πρωτογενούς εστίας
- Μικροοργανισμός συμβατός με λοιμώδη ενδοκαρδίτιδα σε συνεχόμενες καλλιέργειες αίματος, που ορίζεται ως εξής:
- 2 θετικές καλλιέργειες αίματος ληφθείσες με διαφορά >12 ωρών ή
- Και τις 3 ή την πλειονότητα εκ τεσσάρων καλλιεργειών αίματος ληφθεισών με διαφορά τουλάχιστον μίας ώρας
- Τουλάχιστον μία θετική καλλιέργεια για Coxiella burnetii ή τίτλος αντισωμάτων IgG της φάσης Ι > 1:1800
- Τυπικός μικροοργανισμός για λοιμώδη ενδοκαρδίτιδα σε δύο διαφορετικές καλλιέργειες αίματος, όπως:
- Ένδειξη προσβολής του ενδοκαρδίου με θετικό ηχοκαρδιογράφημα, που ορίζεται ως εξής:
- Παλλόμενη ενδοκαρδιακή μάζα επί της βαλβίδας ή των υποστηρικτικών δομών, στην πορεία παλινδρομούντων πιδάκων, ή επί εμφυτευμένου υλικού, εν απουσία εναλλακτικής ανατομικής ερμηνείας ή
- Απόστημα ή
- Νέο μερικό ρήγμα στην προσθετική βαλβίδα ή νέα βαλβιδική παλινδρόμηση αίματος (η αύξηση ή μεταβολή προϋπάρχοντος φυσήματος δεν επαρκεί)
Ελάσσονα κριτήρια:
- Προδιαθεσικοί παράγοντες: γνωστή καρδιακή βλάβη ή ενδοφλέβια χρήση ναρκωτικών
- Πυρετός >38°C
- Ενδείξεις εμβολισμού: αρτηριακή εμβολή, πνευμονικά έμφρακτα, βλάβες Janeway, επιπεφυκοτικές αιμορραγίες
- Ανοσολογικά φαινόμενα: σπειραματονεφρίτιδα, οζίδια του Osler
- Θετική καλλιέργεια αίματος (που δεν πληροί μείζον κριτήριο) ή ορολογική ένδειξη λοίμωξης με μικροοργανισμό συμβατό με λοιμώδη ενδοκαρδίτιδα που δεν ικανοποιεί μείζον κριτήριο
Θετικό ηχοκαρδιογράφημα (που δεν ικανοποιεί μείζον κριτήριο)(αυτό το κριτήριο αφαιρέθηκε στα αναθεωρημένα κριτήρια του Duke)
Υπεύθυνοι μικροοργανισμοί
[Επεξεργασία | επεξεργασία κώδικα]Πολλοί μικροοργανισμοί μπορούν να προκαλέσουν λοιμώδη ενδοκαρδίτιδα. Αυτοί γενικά απομονώνονται σε καλλιέργειες δειγμάτων αίματος, όπου κάθε ανάπτυξη μικροβίου ελέγχεται και ταυτοποιείται. Ο όρος βακτηριακή ενδοκαρδίτιδα χρησιμοποιείται συχνά, αντανακλώντας το γεγονός ότι στις περισσότερες περιπτώσεις ενδοκαρδίτιδας το αίτιο είναι βακτηριακό, πλέον όμως προτιμάται ο όρος λοιμώδης ενδοκαρδίτιδα.
Βακτήρια
[Επεξεργασία | επεξεργασία κώδικα]Οι πρασινίζοντες α-αιμολυτικοί στρεπτόκοκκοι, που βρίσκονται στη στοματική κοιλότητα, είναι το σύνηθες αίτιο που απομονώνεται όταν η βακτηριαιμία προκαλείται από οδοντιατρική επέμβαση. Όταν πύλη εισόδου για τη βακτηριαιμία είναι το δέρμα, όπως μόλυνση χειρουργικού τραύματος, καθετηριασμός ή ενδοφλέβια χρήση ναρκωτικών, συνήθης είναι η παρουσία του Staphylococcus aureus. Τρίτο σημαντικό αίτιο ενδοκαρδίτιδας είναι τα βακτήρια του γένους Enterococcus. Αυτά τα μικρόβια εισέρχονται στην κυκλοφορία ως αποτέλεσμα βλάβης στην γαστρεντερική ή στις ουροφόρες οδούς. Οι εντερόκοκκοι αναγνωρίζονται oλοένα και περισσότερο ως αίτια ενδονοσοκομειακής ή ενδοκαρδίτιδας της κοινότητας, ενώ οι α-αιμολυτικοί στρεπτόκοκκοι και ο χρυσίζων σταφυλόκοκκος είναι αίτια κυρίως ενδοκαρδίτιδας της κοινότητας.
Μερικοί οργανισμοί όταν απομονώνονται δίνουν πολύτιμες πληροφορίες για το αίτιο, καθώς τείνουν να είναι ειδικοί για αυτό.
- Η Pseudomonas spp. είναι ένας ανθεκτικός μικροοργανισμός που ζει στο νερό και μπορεί να επιμολύνει ναρκωτικά μετά από επαφή τους με πόσιμο νερό. Η Pseudomonas aeruginosa μπορεί να μολύνει παιδιά μέσω πληγών στα πόδια, ενώ μπορεί να προκαλέσει τόσο ενδοκαρδίτιδα όσο και σηπτική αρθρίτιδα.[16]
- Ο Streptococcus bovis και το Clostridium septicum, που αποτελούν φυσιολογική χλωρίδα του εντέρου, σχετίζονται με κακοήθειες του παχέος εντέρου. Όταν εμφανίζονται ως αιτιολογικοί παράγοντες ενδοκαρδίτιδας, συνήθως διεξάγεται κολονοσκόπηση λόγω του ενδεχομένου αιματογενούς διασποράς βακτηρίων από το κόλον, οφειλόμενης σε κακοήθη κατάρρευση του φραγμού μεταξύ εντερικού αυλού και αιμοφόρων αγγείων.[17]
- Οι οργανισμοί HACEK είναι μια ομάδα βακτηρίων που ζουν στα ούλα και μπορεί να προκαλέσουν λοίμωξη σε χρήστες ενδοφλέβιων ναρκωτικών, αν μολύνουν με σίελο τις βελόνες που χρησιμοποιούν. Μπορεί επίσης να υπάρχει ιστορικό κακής στοματικής υγιεινής ή προϋπάρχουσα βαλβιδική νόσος.[18]
- Λιγότερο συχνά έχουν αναφερθεί βακτήρια που είναι αιτιολογικοί παράγοντες λοιμώδους ενδοκαρδίτιδας με αρνητικές καλλιέργειες αίματος. Τέτοια βακτήρια πρoσδιορίζονται ορολογικά, με καλλιέργεια βαλβιδικού ιστού, πτυέλων, πλευριτικού υγρού και εμβόλων και με την αλυσιδωτή αντίδραση πολυμεράσης (PCR) ή/και με αλληλούχιση της 16S υπομονάδας του ριβοσωμικού RNA. Στα βακτήρια αυτά ανήκουν ο Streptococcus mitis, η Bartonella, τα Chlamydophila psittaci και η Coxiella.[19] Τα προπιονοβακτηρίδια είναι φυσιολογική χλωρίδα του δέρματος, αλλά έχουν ενοχοποιηθεί για θανάτους μετά από πυογόνο λοίμωξη.[20] Τα Abiotrophia αποτελούν ξεχώριστο γένος gram θετικών κόκκων που ταξινομούνται ως στρεπτόκοκκοι με διαφορετικές θρεπτικές απαιτήσεις. Αυτοί οι μικροοργανισμοί είναι υπεύθυνοι για το 1%-2% των περιπτώσεων λοιμώδους ενδοκαρδίτιδας. [21] Το Tropheryma whipplei, υπεύθυνο για την Νόσο του Whipple που προσβάλλει το λεπτό έντερο, μπορεί να προκαλέσει ενδοκαρδίτιδα και χωρίς γαστρεντερική συμμετοχή.[22] Η Granulicatella elegans είναι άλλο ένα σπάνιο αποδεδειγμένο μικροβιακό αίτιο.[23] To Citrobacter koseri, Gram αρνητικό δυνητικά αναερόβιο βακτήριο που συνήθως προσβάλλει ανοσοκατεσταλμένα άτομα, έχει βρεθεί και σε ανοσοεπαρκή ενήλικα.[24] Η Neisseria bacilliformis βρέθηκε σε ασθενή με δίπτυχη αορτική βαλβίδα.[25]
Μύκητες και Ιοί
[Επεξεργασία | επεξεργασία κώδικα]Η Candida albicans, ένας ζυμομύκητας, σχετίζεται με ενδοκαρδίτιδα σε χρήστες ενδοφλέβιων ναρκωτικών και σε ανοσοκατεσταλμένους. Άλλοι μύκητες που υποστηρίζεται ότι προκαλούν ενδοκαρδίτιδα είναι το Histoplasma capsulatum και ο Aspergillus.[19] Ένα άλλο αποδεδειγμένο αίτιο είναι το Trichosporon asahii. [26]
Οι ιογενείς λοιμώξης της καρδιάς συνήθως σχετίζονται με ιογενή μυοκαρδίτιδα ή περικαρδίτιδα. Η ύπαρξη ιογενούς ενδοκαρδίτιδας αμφισβητείται, αλλά υπάρχουν μερικά στοιχεία που δείχνουν ότι μπορεί να συμβεί.[27]
Θεραπεία
[Επεξεργασία | επεξεργασία κώδικα]Χορηγούνται υψηλές δόσεις αντιβιοτικών ενδοφλεβίως, ώστε να επιτυγχάνεται η μέγιστη διάχυση της δραστικής ουσίας μέσα στις εκβλαστήσεις από το αίμα που γεμίζει τις καρδιακές κοιλότητες. Αυτό είναι απαραίτητο, διότι ούτε οι καρδιακές βαλβίδες ούτε οι εκβλαστήσεις που βρίσκονται σε αυτές αρδεύονται από αγγειακό δίκτυο. Η χορήγηση αντιβιοτικών συνεχίζεται για μεγάλο χρονικό διάστημα, συνήθως για 2 ως 6 εβδομάδες. Τα ειδικά φαρμακευτικά σχήματα διαφέρουν ανάλογα με την ταξινόμηση της ενδοκαρδίτιδας ως οξείας ή υποξείας (στην περίπτωση οξείας ενδοκαρδίτιδας καθίσταται αναγκαία η κάλυψη και για Staphylococcus aureus με αντισταφυλοκοκκική πενικιλλίνη (π.χ. οξακιλλίνη) ή εναλλακτικά βανκομυκίνη, πέρα από την κάλυψη για αρνητικούς κατά Gram μικροοργανισμούς). Η μυκητιασική ενδοκαρδίτιδα απαιτεί ειδική αντιμυκητιασική θεραπεία, με φάρμακα όπως η αμφοτερικίνη Β.
Στην οξεία ενδοκαρδίτιδα, λόγω της κεραυνοβόλου φλεγμονής, ξεκινά εμπειρική αντιβιοτική θεραπεία αμέσως μετά τη λήψη δειγμάτων αίματος για καλλιέργεια. Αυτή συνήθως περιλαμβάνει οξακιλλίνη και γενταμυκίνη ενδοφλεβίως, μέχρι να βγουν τα αποτελέσματα της καλλιέργειας και το αντιβιόγραμμα με την ευαισθησία του μικροοργανισμού, εκφρασμένη σε Ελάχιστη Ανασταλτική Συγκέντρωση (MIC), οπότε και μπορεί να τροποποιηθεί η θεραπεία για το συγκεκριμένο παθογόνο αίτιο. Η χορήγηση γενταμυκίνης ως ρουτίνα για την αντιμετώπιση της σταφυλοκοκκικής ενδοκαρδίτιδας έχει τεθεί υπό αμφισβήτηση, εξαιτίας έλλειψης στοιχείων που να υποστηρίζουν τη χρήση της καθώς και συχνών επιπλοκών.[28]
Στην υποξεία ενδοκαρδίτιδα η αντιμικροβιακή θεραπεία βασίζεται στον υπεύθυνο οργανισμό, απαιτώντας τα αποτελέσματα του αντιβιογράμματος. Έτσι η άμεση θεραπεία εστιάζεται κυρίως στη συμπτωματική αντιμετώπιση.
Το πιο κοινό αίτιο λοιμώδους ενδοκαρδίτιδας είναι ο πρασινίζων στρεπτόκοκκος (Streptococcus viridans), που είναι πολύ ευαίσθητος στην πενικιλλίνη. Απαιτούνται υψηλές δόσεις κρυσταλλικής πενικιλλίνης (G) ενδοφλεβίως κάθε 4 ώρες για 2 εβδομάδες και ακόμα παραμένει το φάρμακο εκλογής. Η αντιβιοτική θεραπεία καθορίζεται από το αντιβιόγραμμα.
Μια άλλη αγωγή που ακολουθείται είναι η θεραπεία σύντομης διάρκειας[29] που διαρκεί 2 εβδομάδες και περιλαμβάνει χορήγηση βενζυλικής πενικιλλίνης (G) ενδοφλεβίως, η οποία είναι επαρκής για την αντιμετώπιση της ενδοκαρδίτιδας από Streptococcus viridans και Streptococcus bovis, εφόσουν πληρούνται οι παρακάτω προϋποθέσεις: ‣ Ενδοκαρδίτιδα φυσικής και όχι προσθετικής βαλβίδας ‣ MIC ≤ 0,1mg/L ‣ Απουσία επιβαρυντικών προγνωστικών παραγόντων, όπως καρδιακή ανεπάρκεια, ανεπάρκεια αορτικής βαλβίδας ή διαταραχές της καρδιακής αγωγιμότητας. ‣ Απουσία θρομβοεμβολικών φαινομένων ‣ Απουσία εκβλαστήσεων με διάμετρο >5mm ‣ Κλινική απάντηση μέσα σε 7 μέρες
Ο χειρουργικός καθαρισμός και η αντικατάσταση της προσβεβλημένης βαλβίδας με προσθετική είναι αναγκαία σε ασθενείς, στους οποίους δεν επιτυγχάνεται κάθαρση του αίματος από το μικροβιακό αίτιο μετά από αντιβιοτική θεραπεία ή σε ασθενείς που αναπτύσσουν καρδιακή ανεπάρκεια λόγω της καταστροφής μιας βαλβίδας από τη λοίμωξη. Άλλες ενδείξεις χειρουργικής επέμβασης είναι:[29] ‣ Ασταθής προσθετική βαλβίδα ‣ Επαναλαμβανόμενες σηπτικές εμβολές, μυκωτικό ανεύρυσμα ‣ Μεγάλες εκβλαστήσεις ‣ Σχηματισμός αποστήματος ‣ Πρόωρη σύγκλειση μιτροειδούς ‣ Gram αρνητική λοίμωξη
Η λοιμώδης ενδοκαρδίτιδα σχετίζεται με θνητότητα 25%.[29]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ (Αγγλικά) οντολογία των ασθενειών. 27 Μαΐου 2016. purl
.obolibrary .org /obo /doid .owl. Ανακτήθηκε στις 30 Νοεμβρίου 2020. - ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 Mitchell RS· Kumar V· Robbins SL· Abbas AK· Fausto N (2007). Robbins Basic Pathology (8th έκδοση). Saunders/Elsevier. σελίδες 406–8. ISBN 1-4160-2973-7.
- ↑ Morris AM (January 2006). «How best to deal with endocarditis». Curr Infect Dis Rep 8 (1): 14–22. doi:. PMID 16448596.
- ↑ 4,0 4,1 Kasper DL· Brunwald E· Fauci AS· Hauser S· Longo DL· Jameson JL (Μαΐου 2005). Harrison's Principles of Internal Medicine. McGraw-Hill. σελίδες 731–40. ISBN 0-07-139140-1. OCLC 54501403 56437106 56801936 56967424.
- ↑ 5,0 5,1 Amal Mattu· Deepi Goyal· Barrett, Jeffrey W.· Joshua Broder· DeAngelis, Michael· Peter Deblieux· Gus M. Garmel· Richard Harrigan· David Karras· Anita L'Italien· David Manthey (2007). Emergency medicine: avoiding the pitfalls and improving the outcomes. Malden, Mass: Blackwell Pub./BMJ Books. σελίδες 63. ISBN 1-4051-4166-2.
- ↑ Wilson W, Taubert KA, Gewitz M, et al. (October 2007). «Prevention of infective endocarditis: guidelines from the American Heart Association». Circulation 116 (15): 1736–54. doi:. PMID 17446442. http://circ.ahajournals.org/cgi/pmidlookup?view=long&pmid=17446442.
- ↑ 7,0 7,1 Durack D, Lukes A, Bright D (1994). «New criteria for diagnosis of infective endocarditis: utilization of specific echocardiographic findings. Duke Endocarditis Service». Am J Med 96 (3): 200–9. doi:. PMID 8154507.
- ↑ 8,0 8,1 Weisse A, Heller D, Schimenti R, Montgomery R, Kapila R (1993). «The febrile parenteral drug user: a prospective study in 121 patients». Am J Med 94 (3): 274–80. doi:. PMID 8452151. https://archive.org/details/sim_american-journal-of-medicine_1993-03_94_3/page/274.
- ↑ 9,0 9,1 Samet J, Shevitz A, Fowle J, Singer D (1990). «Hospitalization decision in febrile intravenous drug users». Am J Med 89 (1): 53–7. doi:. PMID 2368794. https://archive.org/details/sim_american-journal-of-medicine_1990-07_89_1/page/53.
- ↑ 10,0 10,1 10,2 Marantz P, Linzer M, Feiner C, Feinstein S, Kozin A, Friedland G (1987). «Inability to predict diagnosis in febrile intravenous drug abusers». Ann Intern Med 106 (6): 823–8. PMID 3579068. https://archive.org/details/sim_annals-of-internal-medicine_1987-06_106_6/page/823.
- ↑ 11,0 11,1 Leibovici L, Cohen O, Wysenbeek A (1990). «Occult bacterial infection in adults with unexplained fever. Validation of a diagnostic index». Arch Intern Med 150 (6): 1270–2. doi:. PMID 2353860.
- ↑ 12,0 12,1 Mellors J, Horwitz R, Harvey M, Horwitz S (1987). «A simple index to identify occult bacterial infection in adults with acute unexplained fever». Arch Intern Med 147 (4): 666–71. doi:. PMID 3827454.
- ↑ Kaech C, Elzi L, Sendi P, et al. (2006). «Course and outcome of Staphylococcus aureus bacteraemia: a retrospective analysis of 308 episodes in a Swiss tertiary-care centre». Clin Microbiol Infect 12 (4): 345–52. doi:. PMID 16524411.
- ↑ Shively B, Gurule F, Roldan C, Leggett J, Schiller N (1991). «Diagnostic value of transesophageal compared with transthoracic echocardiography in infective endocarditis». J Am Coll Cardiol 18 (2): 391–7. doi:. PMID 1856406. https://archive.org/details/sim_journal-of-the-american-college-of-cardiology_1991-08_18_2/page/391.
- ↑ Erbel R, Rohmann S, Drexler M, et al. (1988). «Improved diagnostic value of echocardiography in patients with infective endocarditis by transoesophageal approach. A prospective study». Eur Heart J 9 (1): 43–53. PMID 3345769.
- ↑ «Topics in Infectious Diseases Newsletter, August 2001, Pseudomonas aeruginosa». Αρχειοθετήθηκε από το πρωτότυπο στις 24 Ιουλίου 2008. Ανακτήθηκε στις 17 Μαΐου 2011.
- ↑ Chew SSB, Lubowski DZ (2001). «Clostridium septicum and malignancy». ANZ Journal of Surgery 71 (11): 647–649. doi:. PMID 11736823. https://archive.org/details/sim_anz-journal-of-surgery_2001-11_71_11/page/647.[νεκρός σύνδεσμος]
- ↑ Mirabelle Kelly, MD (7 Ιουνίου 2005). «HACEK Group Infections».
- ↑ 19,0 19,1 Lamas CC, Eykyn SJ.vv” Blood culture negative endocarditis: analysis of 63 cases presenting over 25 years.” Heart. 2003 March; 89(3): 258–262. PMCID: PMC1767579.
- ↑ Clayton JJ, Baig W, et. al. “Endocarditis caused by Propionibacterium species: a report of three cases and a review of clinical features and diagnostic difficulties. J Med Microbiol. 2006 Aug;55(Pt 8):981-7.PMID:16849716.
- ↑ Sharaf MA, Shaikh N. “Abiotrophia endocarditis: case report and review of the literature.” Can J Cardiol. 2005 Dec;21(14):1309-11. PMID 16341303. .
- ↑ Dreier J, Szabados F, et al. “Tropheryma whipplei Infection of an acellular porcine heart valve bioprosthesis in a patient who did not have intestinal Whipple's disease.” J Clin Microbiol. 2004 Oct;42(10):4487-93. PMID:15472298.
- ↑ Casalta JP, Habib G, et al, “Molecular diagnosis of Granulicatella elegans on the cardiac valve of a patient with culture-negative endocarditis.” J Clin Microbiol. 2002 May;40(5):1845-7. PMID 11980974.
- ↑ Dzeing-Ella A, Szwebel TA, et al,. “Infective endocarditis due to Citrobacter koseri in an immunocompetent adult.” J Clin Microbiol. 2009 Dec;47(12):4185-6. Epub 2009 Oct 7. PMID 19812281.
- ↑ Masliah-Planchon J, Breton G, et al. “Endocarditis due to Neisseria bacilliformis in a patient with a bicuspid aortic valve.” J Clin Microbiol. 2009 Jun;47(6):1973-5. Epub 2009 Apr 22. PMID 19386832.
- ↑ {{Izumi K, Hisata Y, Hazama S. “A rare case of infective endocarditis complicated by Trichosporon asahii fungemia treated by surgery.” Ann Thorac Cardiovasc Surg. 2009 Oct;15(5):350-3. PMID 19901894.}}
- ↑ Silver, Malcolm D.· Bloom, Sherman· Lie, J. T. (1997). Diagnostic criteria for cardiovascular pathology: acquired diseases. Philadelphia: Lippincott-Raven. σελίδες 114. ISBN 0-397-51630-4.
- ↑ Cosgrove SE, Vigliani GA, Campion M, et al. (2009). «Initial low‐dose gentamicin for Staphylococcus aureus bacteremia and endocarditis is nephrotoxic». Clin Infect Dis 48 (6): 713–721. doi:. PMID 19207079.
- ↑ 29,0 29,1 29,2 Hunter JG· Boon NA· Davidson S· Colledge NR· Walker B (2006). Davidson's Principles & Practice of Medicine. Elsevier/Churchill Livingstone. σελίδες 629–33. ISBN 0-443-10057-8. OCLC 65765046.