Λυσίνη
| Λυσίνη | |
|---|---|

| |
| |
| Γενικά | |
| Όνομα IUPAC | Λυσίνη 2,6-διαμινοεξανοϊκό οξύ |
| Χημικά αναγνωριστικά | |
| Χημικός τύπος | C6H14N2O2 |
| Μοριακή μάζα | 146,19 amu |
| Συντομογραφίες | lys ή K |
| Αριθμός CAS | 70-54-2 (DL) 56-87-1 (L) 923-27-3 (D) |
| SMILES | C(CCN)CC(C(=O)O)N |
| InChI | 1S/C6H14N2O2/c7-4-2-1-3-5(8)6(9)10/h5H,1-4,7-8H2,(H,9,10) Κλειδί: KDXKERNSBIXSRK-UHFFFAOYSA-N |
| PubChem CID | 866 |
| ChemSpider ID | 843 5747 (L) |
| Φυσικές ιδιότητες | |
| Διαλυτότητα στο νερό |
1,5 kg/m³ |
| Χημικές ιδιότητες | |
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |
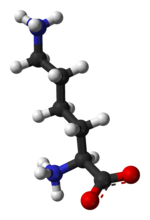
Η λυσίνη[1] είναι ένα από τα 22 πρωτεϊνογόνα αμινοξέα. Στο επίπεδο της μοριακής γενετικής, τα κωδικόνιά της είναι AAA και AAG. Είναι ένα απαραίτητο αμινοξύ για τον άνθρωπο. Χημικώς είναι ένα α,ε-διαμινοξύ με σύντομο συντακτικό τύπο: H2NCH2CH2CH2CH2CH(NH2)COOH. Η λυσίνη είναι ένα από τα «βασικά αμινοξέα». Τα υπόλοιπα δύο (2) είναι η ιστιδίνη και η αργινίνη. Η ε-αμινομάδα της συμμετέχει συχνά σε δεσμούς υδρογόνου και ως γενική βάση στην κατάλυση. Ακόμη, κοινές μετα-μεταφραστικές τροποποιήσεις συμπεριλαμβάνουν τη μεθυλίωση της ε-αμινομάδας, δίνοντας μεθυλολυσίνη, διμεθυλολυσίνη και τριμεθυλολυσίνη. Η τελευταία εμφανίζεται στην καλμοδουλίνη. Άλλες μετα-μεταφραστικές τροποποιήσεις της λυσίνης συμπεριλαμβάνουν ακετυλίωση και ουβικιτινίωση. Το κολλαγόνο περιέχει υδροξυλυσίνη, που παράγεται από τη λυσίνη με τη χρήση του ενζύμου υδροξυλάση της λυσίνης. O-γλυκοσυλίωση της υδροξυλυσίνης συμβαίνει στο ενδοπλασματικό δίκτυο ή στο σωμάτιο Golgi και χρησιμοποιείται για να επισημάνει ορισμένες πρωτεΐνες για απέκκριση από το κύτταρο.
Παραγωγή
[Επεξεργασία | επεξεργασία κώδικα]Η συνθετική ρακεμική λυσίνη είναι γνωστή για μακρύ χρονικό διάστημα[2]. Μια πρακτική συνθετική οδός ξεκινά από την καπρολακτάμη[3]. βιομηχανικά, η L-λυσίνη συνήθως παράγεται με μια ζυμωτική διεργασία χρησιμοποιώντας το Corynebacterium glutamicum. Η παγκόσμια ετήσια παραγωγή της ξεπερνά τους 600.000 τόννους[4].
Βιοσύνθεση
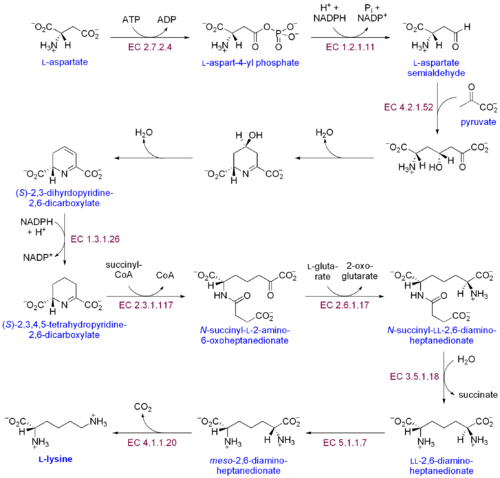
[Επεξεργασία | επεξεργασία κώδικα]Ως ένα απαραίτητο αμινοξύ, η λυσίνη δεν συντίθεται από τα ζώα, οπότε πρέπει να εισαχθεί από την τροφή τους ως λυσίνη ή ως πρωτεΐνες που περιέχουν λυσίνη. Σε φυτά και βακτήρια, συντίθεται από το ασπαργανικό οξύ, με τα ακόλουθα βιοσυνθετικά στάδια[5]:
- Το L-ασπαργανικό οξύ αρχικά μετατρέπεται σε L-ασπαγανυλ-4-φωσφορικό οξύ, από το ένζυμο ασπαργανοκινάση. Το ATP χρειάζεται ως ενεργειακή πηγή γι' αυτό το στάδιο.
- Το ένζυμο δεϋδρογονάση της ημιαλδεΰδης του β-ασπαργανικού οξέος μετατρέπει το L-ασπαγανυλ-4-φωσφορικό οξύ σε β-ασπαργανυλο-4-ημιαλδεΰδη.
- Το ένζυμο διυδροδιπικολινική συνθετάση προσθέτει μια ομάδα πυροσταφυλικού οξέος στη β-ασπαργανυλο-4-ημιαλδεΰδη, ενώ δύο μόρια νερού αφαιρούνται. Αυτό προκαλεί κυκλοποίηση και δίνει 2,3-διυδροδιπικολινικό οξύ.
- Το 2,3-διυδροδιπικολινικό οξύ ανάγεται σε 2,3,4,5-τετραϋδροδιπικολινικό οξύ από το ένζυμο αναγωγάση του διυδροδιπικολινικού οξέος. Η αντίδραση αυτή απαιτεί και ένα μόριο NADPH.
- Το ένζυμο N-ακετυλοτρανσφεράση ανοίγει το δακτύλιο και δίνει N-ηλεκτρινυλο-L-2-αμινο-6-οξοεπτανοδιονικό οξύ. Δύο μόρια νερού και ένα μόριο ηλεκτρυλο-CoA καταναλώνονται σε αυτήν την αντίδραση.
- Το N-ηλεκτρινυλο-L-2-αμινο-6-οξοεπτανοδιονικό οξύ μετατρέπεται σε N-ηλεκτρινυλο-LL-2,6-διαμινεπτανοδιονικό οξύ. Η αντίδραση αυτή καταλύεται από το ένζυμο ηλεκτρινυλοδιαμινοπιμηλικοαμινοτρανσφεράση. Ένα μόριο γλουταρικού οξέος καταναλώνεται σ' αυτήν την αντίδραση, ενώ παράγεται ένα οξοοξύ ως παραπροϊόν.
- Το N-ηλεκτρινυλο-LL-2,6-διαμινεπτανοδιονικό οξύ μετατρέπεται σε LL-2,6-διαμινοεπτανοδιικό οξύ, από το ένζυμο ηλεκτρινυλοδιαμινοπιμηλικοδεηλεκτρινυλάση. Ένα μόριο νερού καταναλώνεται σε αυτήν την αντίδραση, ενώ παράγεται ηλεκτρικό οξύ ως ένα παραπροϊόν.
- Το LL-2,6-διαμινοεπτανοδιικό οξύ μετατρέπεται σε μεσο-2,6-διαμινοεπτανοδιικό οξύ από το ένζυμο διαμινοπιμηλικοεπιμεράση.
- Τελικά, το μεσο-2,6-διαμινοεπτανοδιικό οξύ μετατρέπεται σε L-λυσίνη από το ένζυμο διαμινοπιπιμηλικοδεκαρβοξυλάση.
Μεταβολισμός
[Επεξεργασία | επεξεργασία κώδικα]Η λυσίνη καταβολίζεται στα θηλαστικά δίνοντας ακευτυλοσυνένζυμο Α, μέσω μιας αρχικής τρανσαμίνωσης με το α-κετογλουταρικό οξύ. Τα βακτήρια αποσυνθέτουν τη λυσίνη παίρνοντας καδαβερίνη με αποκαρβοξυλίωση.
Η αλλυσίνη είναι ένα παράγωγο της λυσίνης, που χρησιμοποιείται για την παραγωγή της ελαστίνης και του κολλαγόνου. Παράγεται με τη δράση του ενζύμου οξειδάση της λυσίνης στην εξωκυτταρική μήτρα και είναι απαραίτητη για τον σχηματισμό ενδομοριακών δεσμών που σταθεροποιούν το κολλαγόνο και την ελαστίνη.
Παραγωγή λυσίνης
[Επεξεργασία | επεξεργασία κώδικα]Η λυσίνη κατά κύριο λόγο παράγεται από ζύμωση με χρήση στελεχών του γένους Corynebacteria, ειδικότερα τα glutamicum Corynebacterium. Η παραγωγή της λυσίνης περιλαμβάνει μια διαδικασία πολλαπλών βημάτων, συμπεριλαμβανομένων ζύμωσης, διαχωρισμού των κυττάρων με φυγοκέντρηση ή υπερδιήθηση, διαχωρισμό των προϊόντων και καθαρισμό, εξάτμιση και ξήρανση. Λόγω της μεγάληs σημασίας της L-Λυσίνης, γίνονται συνεχώς προσπάθειες προκειμένου να βελτιωθεί η διαδικασία ζύμωσης (π.χ. αύξηση των εγγενών χαρακτηριστικών της παραγωγικότητας του μικροοργανισμού από την κλασική μεταλλαξιγένεση και της γενετικής μηχανικής) και την εξέλιξη της διαδικασίας (π.χ. επίδραση της συνεχόμενης ανάδευσης και την προμήθεια οξυγόνου, θερμοκρασία, pH και CO), καθώς και τη βελτιστοποίηση των μέσων (π.χ. επίδραση της αρχικής και λειτουργικης συγκεντρωσης της ζάχαρης, σημαντικά θρεπτικα συστατικά και τα πρόσθετα) όσο και την προς τα κάτω μεταποίηση (π.χ. χρωματογραφία ιονικής ανταλλαγής) καθώς και σίτιση κατά τη διάρκεια της καλλιέργειας όπου χρησιμοποιούνται για την παραγωγή της L-λυσίνης και άλλα L-αμινοξέα, που λειτουργούν σε δεξαμενή ανάμειξης ή ζύμωσης αναδευτήρα αέρα.
Παραπομπές και σημειώσεις
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Δείτε τις εναλλακτικές ονομασίες και επίσημες συντομογραφίες στον παρακείμενο πίνακα πληροφοριών χημικής ένωσης.
- ↑ Braun, J. V. "Synthese des inaktiven Lysins aus Piperidin" Berichte der deutschen chemischen Gesellschaft 1909, Volume 42, p 839-846. doi:10.1002/cber.190904201134.
- ↑ Eck, J. C.; Marvel, C. S. "dl-Lysine Hydrochlorides" Organic Syntheses, Collected Volume 2, p.374 (1943). http://www.orgsyn.org/orgsyn/pdfs/CV2P0374.pdf Αρχειοθετήθηκε 2007-09-27 στο Wayback Machine..
- ↑ ^ Pfefferle, W.; Möckel, B.; Bathe, B.; Marx, A. (2003). "Biotechnological manufacture of lysine". Advances in biochemical engineering/biotechnology. Advances in Biochemical Engineering/Biotechnology 79: 59–112. doi:10.1007/3-540-45989-8_3. ISBN 978-3-540-43383-5. PMID 12523389.
- ↑ Lysine biosynthesis and catabolism, Purdue University
| Αυτό το λήμμα σχετικά με τη βιοχημεία χρειάζεται επέκταση. Μπορείτε να βοηθήσετε την Βικιπαίδεια επεκτείνοντάς το. |