Οξεία μυελογενής λευχαιμία
| Οξεία μυελογενής λευχαιμία | |
|---|---|
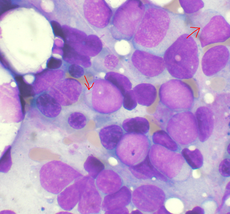 Αναρρόφηση μυελού των οστών που υποδηλώνει οξεία μυελογενή λευχαιμία. | |
| Ειδικότητα | ογκολογία και αιματολογία |
| Συμπτώματα | κόπωση, απώλεια σωματικού βάρους, ανορεξία, αναιμία, Αιμορραγία και σπληνομεγαλία |
| Ταξινόμηση | |
| ICD-10 | C92.0 |
| ICD-9 | 205.0 |
| ICD-O | M9861/3 |
| OMIM | 602439 |
| DiseasesDB | 203 |
| eMedicine | med/34 |
| MeSH | D015470 |
Η οξεία μυελογενής λευχαιμία (ΟΜΛ) είναι καρκίνος των κυττάρων της λευκής σειράς, που χαρακτηρίζεται από ραγδαία ανάπτυξη των λευκών αιμοσφαιρίων που συσσωρεύονται στο μυελό των οστών και εμποδίζουν την αιμοποίηση. Η ΟΜΛ είναι η πιο κοινή οξεία λευχαιμία που προσβάλει ενήλικες και η επίπτωσή της αυξάνεται με την ηλικία. Παρόλο που η ΟΜΛ είναι σχετικά σπάνια ασθένεια, υπεύθυνη περίπου για το 1,2% θανάτων λόγω καρκίνου στις ΗΠΑ,[1] η συχνότητα εμφάνισής της αναμένεται να αυξάνεται με την αύξηση της ηλικίας του πληθυσμού.
Τα συμπτώματα της ΟΜΛ προκαλούνται από την αντικατάσταση των φυσιολογικών κυττάρων του μυελού των οστών με λευχαιμικά κύτταρα, γεγονός που προκαλεί ελάττωση στον αριθμό των ερυθρών αιμοσφαιρίων, των αιμοπεταλίων και των φυσιολογικών λευκών αιμοσφαιρίων. Τα συμπτώματα περιλαμβάνουν κόπωση, δύσπνοια, εύκολη πρόκληση μελανιασμάτων και αιμορραγιών, καθώς και αυξημένο κίνδυνο λοίμωξης. Πολλοί παράγοντες κινδύνου και χρωμοσωμικές ανωμαλίες έχουν αναγνωριστεί, αλλά η συγκεκριμενοποίηση της αιτίας δεν έχει επιτευχθεί. Όπως και στην οξεία λεμφογενή λευχαιμία, η ΟΜΛ εξελίσσεται ραγδαία και τυπικά είναι θανατηφόρος μέσα σε διάστημα λίγων βδομάδων ή μηνών, αν δεν αντιμετωπιστεί.
Η ΟΜΛ έχει πολλούς υποτύπους και η θεραπεία και πρόγνωσή της ποικίλει ανάλογα με τους τύπους αυτούς. Η πενταετής επιβίωση κυμαίνεται μεταξύ 15-70% και το ποσοστό υποτροπής μεταξύ 33-78%, ανάλογα με τον τύπο. Η ΟΜΛ αρχικά αντιμετωπίζεται με χημειοθεραπεία που στοχεύει στην επίτευξη ύφεσης της ασθένειας. Στη συνέχεια οι ασθενείς μπορεί να υποβληθούν σε επιπρόσθετη χημειοθεραπεία ή μεταμόσχευση αρχέγονων αιμοποιητικών κυττάρων. Πρόσφατες έρευνες σχετικά με τη γενετική βάση της ΟΜΛ έχουν αποφέρει στη δημιουργία διαγνωστικών τεστ που μπορούν να προβλέψουν ποιο φάρμακο ή φάρμακα θα έχουν τη μεγαλύτερη αποτελεσματικότητα στον συγκεκριμένο ασθενή, καθώς και πόσο υπολογίζεται ότι θα επιβιώσει.
Ταξινόμηση
[Επεξεργασία | επεξεργασία κώδικα]Τα δύο πιο συνηθισμένα σχήματα για την ταξινόμηση της ΟΜΛ, είναι το παλαιότερο Γαλλο-Αμερικανο-Βρετανικό σύστημα και το νεότερο του Παγκόσμιου Οργανισμού Υγείας.
Παγκόσμιος Οργανισμός Υγείας
[Επεξεργασία | επεξεργασία κώδικα]Ο Παγκόσμιος Οργανισμός Υγείας(ΠΟΥ) ταξινομεί την ΟΜΛ επιχειρώντας η ταξινόμησή του αυτή να είναι πιο χρήσιμη κλινικά και να παρέχει πιο ουσιαστικές προγνωστικές πληροφορίες από το παλαιότερο σύστημα ταξινόμησης. Καθεμία από τις κατηγορίες του ΠΟΥ περιέχει πολυάριθμες αναλυτικές υποκατηγορίες που αφορούν τον αιματολόγο και τον ογκολόγο. Παρόλα αυτά οι περισσότερες κλινικά σημαντικές πληροφορίες του συστήματος του ΠΟΥ περιλαμβάνονται απευθείας στην κατηγοριοποίηση σε κάποια από τις παρακάτω υποκατηγορίες.
Οι τύπο της ΟΜΛ σύμφωνα με τον ΠΟΥ είναι οι εξής:[2]
| Ονομασία | Περιγραφή | ICD-O |
|---|---|---|
| ΟΜΛ με χαρακτηριστικές γενετικές ανωμαλιες | Περιλαμβάνει:
Ασθενείς με ΟΜΛ σε αυτή την κατηγορία γενικά έχουν μεγάλη πιθανότητα υποτροπής και καλύτερη πρόγνωση σε σύγκριση με άλλους τύπους ΟΜΛ. |
Πολλαπλή |
| ΟΜΛ με πολλαπλή δυσπλασία | Αυτή η κατηγορία περιλαμβάνει ασθενείς που είχαν μυελοδυσπλαστικό σύνδρομο (ΜΔΣ) ή μυελοϋπερπλαστική νόσο που εξελίχθηκε σε ΟΜΛ. Αυτή η κατηγορία ΟΜΛ παρουσιάζεται συνηθέστερα σε ηλικιωμένους ασθενείς και έχει συνήθως τη χειρότερη πρόγνωση. | M9895/3 |
| ΟΜΛ και ΜΔΣ, θεραπειοσχετιζόμενη | Η κατηγορία αυτή περιλαμβάνει ασθενείς που είχαν προηγούμενη χημειοθεραπεία και/είτε ακτινοθεραπεία και κατόπιν ανέπτυξαν ΟΜΛ ή ΜΔΣ. Αυτές οι λευχαιμίες μπορεί να χαρακτηρίζονται από συγκεκριμένες χρωμοσωμικές ανωμαλίες και συχνά έχουν κακή πρόγνωση. | M9920/3 |
| ΟΜΛ χωρίς ιδιαίτερα κριτήρια | Περιλαμβάνει τύπους ΟΜΛ που δε συμπεριλαμβάνονται στις παραπάνω κατηγορίες. | M9861/3 |
Οξείες λευχαιμίες με αμφίβολη προέλευση (γνωστές και ως μεικτού φαινοτύπου λευχαιμίες) συμβαίνουν είτε όταν τα λευχαιμικά κύτταρα δε μπορούν να κατηγοριοποιηθούν ως μυελοειδή ή λεμφοειδή, είτε όταν και οι δύο τύποι κυττάρων είναι παρόντες.
Γαλλο-Αμερικανο-Βρετανικό σύστημα
[Επεξεργασία | επεξεργασία κώδικα]Το παλαιότερο αυτό σύστημα χωρίζει την ΟΜΛ σε 8 υποτύπους Μ0 έως Μ7, βασιζόμενο στον τύπο του κυττάρου από το οποίο αναπτύσσεται η λευχαιμία και στο στάδιο της ασθένειας. Αυτό γίνεται με την εξέταση της εμφάνισης των κακοηθών κυττάρων κάτω από οπτικό μικροσκόπιο ή χρησιμοποιώντας κυτταρογενετική ώστε να προσδιοριστεί η πιθανή χρωμοσωμική ανωμαλία. Οι τύποι έχουν ποικίλες προγνώσεις και συμπεριφορές στη θεραπευτική αγωγή. Παρόλο που η κατηγοριοποίηση του ΠΟΥ μπορεί να είναι πιο χρήσιμη, το παλαιότερο σύστημα χρησιμοποιείται ακόμα ευρέως.
Οι οκτώ τύποι του Γαλλο-Αμερικανο-Βρετανικού συστήματος:[3]
| Τύπος | Ονομασία | Κυτταρογενετική | Ποσοστό ενηλίκων ασθενών με ΟΜΛ |
|---|---|---|---|
| M0 | ελάχιστα διαφοροποιημένη οξεία μυελογενής λευχαιμία | 5%[4] | |
| M1 | oξεία μυελογενής λευχαιμία χωρίς ωρίμανση | 15%[4] | |
| M2 | οξεία μυελογενής λευχαιμία με κοκκιοκυτταρική ωρίμανση | t(8;21)(q22;q22), t(6;9) | 25%[4] |
| M3 | προμυελοκυτταρική ή οξεία προμυελοκυτταρική λευχαιμία (ΟΠΛ) | t(15;17) | 10%[4] |
| M4 | οξεία μυελομονοκυτταρική λευχαιμία | inv(16)(p13q22), del(16q) | 20%[4] |
| M4eo | μυελομονοκυτταρική μαζί με ηωσινοφιλία του μυελού των οστών | inv(16), t(16;16) | 5%[4] |
| M5 | οξεία μονοβλαστική λευχαιμία (M5a) ή οξεία μονοκυτταρική λευχαιμία (M5b) | del (11q), t(9;11), t(11;19) | 10%[4] |
| M6 | οξεία ερυθροειδής λευχαιμία, που περιλαμβάνει την ερυθρολευχαιμία (M6a) και την πολύ σπάνια αμιγή ερυθροειδή λευχαιμία (M6b) | 5%[4] | |
| M7 | οξεία μεγακαρυωκυτταροβλαστική λευχαιμία | t(1;22) | 5%[4] |
| M8 | οξεία βασεοφιλική λευχαιμία | Ασυνήθεις |
Ασυνήθεις φαινότυποι ΟΜΛ
[Επεξεργασία | επεξεργασία κώδικα]Οι μορφολογική τύποι ΟΜΛ περιλαμβάνουν και πολλούς πάρα πολύ σπάνιους τύπους που δεν περιλαμβάνονται στο παλαιότερο σύστημα ταξινόμησης. Όλοι αυτοί εκτός από την οξεία δενδριτική λευχαιμία περιλαμβάνονται στην κατηγοριοποίηση του ΠΟΥ. Η λίστα που ακολουθεί δείχνει αυτούς τους τύπους.
- Οξεία βασεοφιλική αναιμία
- Οξεία ηωσινοφιλική λευχαιμία
- Μαστοκυτταρική λευχαιμία
- Οξεία μυελοειδής δενδριτικοκυτταρική λευχαιμία
- Οξεία πανμυέλωση με μυελοΐνωση
- Μυελογενές σάρκωμα.
Σημεία και συμπτώματα
[Επεξεργασία | επεξεργασία κώδικα]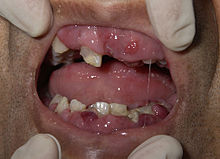
Τα περισσότερα σημεία και συμπτώματα της ΟΜΛ προκαλούνται από της αντικατάσταση των φυσιολογικών κυττάρων του αίματος με λευχαιμικά κύτταρα. Η έλλειψη λευκών αιμοσφαιρίων κάνει τον ασθενή ευάλωτο σε λοιμώξεις και ενώ τα ίδια τα λευχαιμικά κύτταρα προέρχονται από προγονικά κύτταρα των λευκών, δεν έχουν αμυντικές ικανότητες.[5] Μείωση στον αριθμό των ερυθρών αιμοσφαιρίων (αναιμία) μπορεί να προκαλέσει κούραση, ωχρότητα και δύσπνοια. Έλλειψη αιμοπεταλίων οδηγεί σε εύκολο σχηματισμό μωλώπων και αιμορραγιών από μικροτραύματα.
Τα πρώτα συμπτώματα της ΟΜΛ είναι συνήθως πολλά και μη καθορισμένα και μπορεί να προσομοιάζουν εκείνα της γρίπης ή άλλων κοινών ασθενειών. Κάποια γενικευμένα συμπτώματα περιλαμβάνουν πυρετό, κόπωση, απώλεια βάρους ή απώλεια όρεξης, δύσπνοια, αναιμία, ευκολία πρόκλησης μωλώπων και αιμορραγιών, πετέχειες, πόνο στα οστά και τις αρθρώσεις και επίμονες ή συχνές λοιμώξεις.[5]
Σπληνομεγαλία (διόγκωση του σπλήνα) μπορεί να συμβεί στην ΟΜΛ, αλλά είναι συνήθως ήπια και ασυμπτωματική. Λεμφαδενοπάθειες είναι σπάνιες στην ΟΜΛ σε αντίθεση με την οξεία λεμφοβλαστική αναιμία. Το δέρμα συμπεριλαμβάνεται στο 10% των περιπτώσεων με τη μορφή χλωρόματος. Σπανιότερα το Σύνδρομο του Sweet, ένα παρανεοπλασματικό σύνδρομο, μια φλεγμονή του δέρματος, μπορεί να παρουσιαστεί στην ΟΜΛ.[5]
Μερικοί ασθενείς με ΟΜΛ μπορεί να βιώνουν πρήξιμο των ούλων λόγω της διείσδυσης των λευχαιμικών κυττάρων στον ουλώδη ιστό. Σπανιότερα, το πρώτο σημάδι της λευχαιμίας μπορεί να είναι η ανάπτυξη συμπαγούς λευχαιμικής μάζας ή όγκου έξω από τον μυελό των οστών, που ονομάζεται χλώρωμα. Κάποιες φορές ο ασθενής παρουσιάζεται ασυμπτωματικός και η λευχαιμία βρίσκεται τυχαία σε αιματολογική εξέταση ρουτίνας.[6]
Αίτια
[Επεξεργασία | επεξεργασία κώδικα]Έχει αναγνωριστεί ένας αριθμός παραγόντων κινδύνου που σχετίζονται με τον κίνδυνο εμφάνισης ΟΜΛ: άλλες διαταραχές στο αίμα, έκθεση σε χημικά, ιονίζουσα ακτινοβολία και γενετικοί παράγοντες.
Προλευχαιμία
[Επεξεργασία | επεξεργασία κώδικα]Προλευχαιμικές διαταραχές στο αίμα όπως μυελοδυσλαστικό σύνδρομο (ΜΔΣ) ή μυελοϋπερπλαστική νόσος μπορεί να εξελιχθούν σε ΟΜΛ. Το ακριβές ρίσκο εξαρτάται από τον τύπο ΟΜΛ/ΜΔΣ.[7]
Έκθεση σε χημικά
[Επεξεργασία | επεξεργασία κώδικα]Έκθεση σε χημειοθεραπεία και συγκεκριμένα σε αλκυλιωτικό αντινεοπλασματικό παράγοντα, μπορεί να αυξήσει τον κίνδυνο εμφάνισης ΟΜΛ. Ο κίνδυνος είναι μέγιστος περίπου 3-5 χρόνια μετά τη χημειοθεραπεία.[8] Άλλοι χημειοθεραπευτικοί παράγοντες, συγκεκριμένα ποδοφιλοτοξίνη και ανθρακυκλίνες, έχουν επίσης συνδεθεί με την θεραπειοσχετιζόμενη λευχαιμία (δες παραπάνω). Αυτές οι θεραπειοσχετιζόμενες (θεραπειο-επαγώμενες ορθότερα) λευχαιμίες σχετίζονται συχνά με συγκεκριμένες χρωμοσωμικές ανωμαλίες στα λευχαιμικά κύτταρα.[9]
Η επαγγελματική έκθεση σε χημικές ουσίες όπως βενζόλιο και άλλοι οργανικοί διαλύτες είναι αμφιλεγόμενη ως αιτία πρόκλησης ΟΜΛ. Το βενζόλιο και πολλά παράγωγά του είναι γνωστά καρκινογόνα in vitro. Ενώ κάποιες έρευνες εντοπίζουν συσχέτιση μεταξύ επαγγελματικής έκθεσης σε βενζόλιο και αυξημένου κινδύνου εμφάνισης ΟΜΛ,[10] κάποιες άλλες ότι το καταλογιζόμενο ρίσκο, αν υπάρχει, είναι ελάχιστο.[11]
Ακτινοβολία
[Επεξεργασία | επεξεργασία κώδικα]Έκθεση σε ιονίζουσα ακτινοβολία μπορεί να αυξήσει τον κίνδυνο εμφάνισης ΟΜΛ. Επιζώντες των ατομικών βομβών είχαν αυξημένα ποσοστά ΟΜΛ,[12] όπως και οι ακτινολόγοι που εκτέθηκαν σε υψηλά επίπεδα Χ ακτινοβολίας πριν την υιοθέτηση των σύγχρονων μεθόδων ακτινοπροστασίας.[13]
Γενετική
[Επεξεργασία | επεξεργασία κώδικα]Κληρονομικός αυξημένος κίνδυνος εμφάνισης ΟΜΛ φαίνεται ότι υπάρχει. Υπάρχουν πολυάριθμες αναφορές πολλαπλών περιπτώσεων ΟΜΛ που αναπτύχθηκαν σε οικογένειες σε ποσοστό υψηλότερο από την προβλεπόμενη πιθανότητα για το κάθε μέλος ατομικά.[14][15][16][17] Ο κίνδυνος ανάπτυξης ΟΜΛ αυξάνεται στο τριπλάσιο σε συγγενείς πρώτου βαθμού ασθενών με ΟΜΛ.[18]
Πολλές συγγενείς ανωμαλίες και παθήσεις μπορεί να αυξήσουν τον κίνδυνο εμφάνισης λευχαιμίας, η πιο συνηθισμένη από τις οποίες είναι ίσως το Σύνδρομο Down, που συνδέεται με δεκαπλάσιο έως δεκαοκταπλάσιο κίνδυνο εμφάνισης ΟΜΛ.[19]
Διάγνωση
[Επεξεργασία | επεξεργασία κώδικα]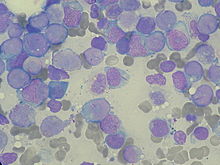
Το πρώτο στοιχείο για τη διάγνωση της ΟΜΛ είναι συνήθως ένα μη φυσιολογικό αποτέλεσμα σε μια εξέταση αίματος ρουτίνας. Παρόλο που οι μεγάλες τιμές λευκών αιμοσφαιρίων είναι το σύνηθες εύρημα και οι λευχαιμικές βλάστες μερικές φορές είναι ορατές, η ΟΜΛ μπορεί να παρουσιάζεται και με απομονωμένες μειωμένες τιμές σε αιμοπετάλια, ερυθρά αιμοσφαίρια ή και ακόμα με μικρό αριθμό λευκών αιμοσφαιρίων (λευκοπενία). [20] Πιθανή διάγνωση ΟΜΛ μπορεί να γίνει με επίχρισμα περιφερικού αίματος όταν οι λευκοβλάστες κυκλοφορούν στα αγγεία. Η οριστική διάγνωση όμως απαιτεί βιοψία του μυελού των οστών.
Ο μυελός ή το αίμα εξετάζονται με οπτικό μικροσκόπιο και με κυτταρομετρία ροής για να διαγνωσθεί η παρουσία λευχαιμίας και να γίνει η διαφοροδιάγνωση της ΟΜΛ από τους άλλους τύπους λευχαιμιών, όπως και για να προσδιοριστεί ο τύπος της. Το δείγμα μυελού ή αίματος συνήθως ελέγχεται και για χρωμοσωμικές μετατοπίσεις με μεθόδους κυτταρογενετικής ή τεχνική FISH (fluorescent in situ hybridization). Γενετικές εξετάσεις μπορεί να ακολουθήσουν ώστε να προσδιοριστούν οι συγκεκριμένες μεταλλάξεις στα κύτταρα όπως είναι στα γονίδια των FLT3, nucleophosmin, KIΤ, που μπορεί να επηρεάσουν την πορεία και την κατάληξη της νόσου.[21]
Οι χημικοί δείκτες - χρωστικές στο επίχρισμα αίματος και μυελού είναι χρήσιμοι για το διαχωρισμό της ΟΜΛ από την οξεία λεμφοβλαστική αναιμία και για το προσδιορισμό του τύπου της ΟΜΛ. Ο συνδυασμός της μυελοϋπεροξειδάσης ή της μαύρης χρωστικής του Σουδάν και μιας μη ειδικής χρωστικής εστεράσης θα αποδώσουν τις επιθυμητές πληροφορίες στις περισσότερες περιπτώσεις. Οι αντιδράσεις της μυελοϋπεροξειδάσης ή της μαύρης χρωστικής του Σουδάν είναι οι πιο χρήσιμες για να προσδιοριστεί η το είδος της λευχαιμίας και ο τύπος της. Η μη ειδική χρωστική εστεράσης χρησιμοποιείται για να αναγνωριστούν μονοκυτταρικά συστατικά στις ΟΜΛ και για να ξεχωρίσουμε μια μερικώς διαφοροποιημένη λευχαιμική μονοβλάστη από την οξεία λεμφοβλαστική αναιμία.[2]
Η διάγνωση και κατηγοριοποίηση της ΟΜΛ μπορεί να είναι δυσχερής και θα πρέπει να πραγματοποιείται από πιστοποιημένο αιματοπαθολόγο ή αιματολόγο. Στις απλές περιπτώσεις, η παρουσία συγκεκριμένων μορφολογικών χαρακτηριστικών (όπως είναι οι ράβδοι Auer) ή μια συγκεκριμένη ροή στην κυτταρομετρία είναι ικανά ευρήματα για να διαφοροδιαγνωσθεί η ΟΜΛ από τις άλλες λευχαιμίες. Σε απουσία όμως τέτοιων χαρακτηριστικών η διάγνωση μπορεί να είναι πολύ πιο δύσκολη.[22]
Σύμφωνα με τα ευρέως χρησιμοποιούμενα κριτήρια του ΠΟΥ, η διάγνωση της ΟΜΛ γίνεται αποδεικνύοντας πως σε περισσότερο από το 20% του αίματος ή/και του μυελού των οστών εντοπίζονται λευχαιμικές μυελοβλάστες. [23]Υπάρχει επίσης και η κατάταξη του Γαλλο-Αμερικανο-Βρετανικού συστήματος που είναι πιο αυστηρή, απαιτώντας ποσοστό βλαστών τουλάχιστον 30% σε μυελό των οστών ή περιφερικό αίμα για τη διάγνωση ΟΜΛ.[24] Η ΟΜΛ πρέπει να διαφοροποιείται προσεκτικά από "προλευχαιμικές" καταστάσεις όπως είναι το μυελοδυσπλαστικό σύνδρομο ή το μυελοϋπερπλαστικό σύνδρομο, τα οποία αντιμετωπίζονται με διαφορετική αγωγή.
Επειδή η οξεία προμυελοκυτταρική λευχαιμία (ΟΠΛ) έχει τις υψηλότερες πιθανότητες ίασης και απαιτεί μια μοναδική αγωγή, είναι πολύ σημαντικό να διαγνωσθεί ή να αποκλειστεί έγκαιρα αυτός ο υποτύπος λευχαιμίας. Τεχνική FISH σε επίχρισμα αίματος ή μυελού των οστών γίνεται συχνά για αυτόν το σκοπό, καθώς εύκολα αναγνωρίζει την χρωμοσωμική μετάθεση (t[15;17]) που χαρακτηρίζει την ΟΜΛ.[25]
Παθοφυσιολογία
[Επεξεργασία | επεξεργασία κώδικα]Το κακοήθες κύτταρο στην ΟΜΛ είναι η μυελοβλάστη. Σε κανονική αιμοποίηση, η μυελοβλάστη είναι ανώριμο πρόδρομο των μυελοειδών λευκών αιμοσφαιρίων: μια κανονική μυελοβλάστη θα ωριμάσει σταδιακά σε ώριμο λευκό αιμοσφαίριο. Ωστόσο, στην ΟΜΛ μια μυελοβλάστη συσσωρεύει γενετικές μεταλλάξεις, οι οποίες «αποκλείουν» το κύτταρο στην ανώριμη μορφή και εμποδίζουν τη διαφοροποίηση.[26] Μια τέτοια μετάλλαξη από μόνη της δεν προκαλεί λευχαιμία, ωστόσο, όταν αυτή η «παύση της διαφοροποίησης» συνδυάζεται με άλλες μεταλλάξεις οι οποίες διαταράσσουν τα γονίδια που ελέγχουν το πολλαπλασιασμό, το αποτέλεσμα είναι η ανεξέλεγκτη ανάπτυξη ενός ανώριμου κλώνου κυττάρων που αποτελεί την οντότητα της ΟΜΛ.[27]
Ένα μεγάλο μέρος της ποικιλομορφίας και της ετερογένειας της ΟΜΛ πηγάζει από το γεγονός ότι ο λευχαιμικός μετασχηματισμός μπορεί να εμφανιστεί σε μια σειρά από διάφορα βήματα κατά μήκος του μονοπατιού της διαφοροποίησης.[28] Σύγχρονα συστήματα ταξινόμησης για την ΟΜΛ αναγνωρίζουν ότι τα χαρακτηριστικά και η συμπεριφορά των λευχαιμικών κυττάρων (και της λευχαιμίας) μπορεί να εξαρτάται από το στάδιο κατά το οποίο η διαφοροποίηση είχε σταματήσει.
Ειδικές κυτταρογενετικές ανωμαλίες μπορούν να βρεθούν σε πολλούς ασθενείς με ΟΜΛ. Τα είδη των χρωμοσωμικών ανωμαλιών πολλές φορές έχουν προγνωστική σημασία.[29] Οι χρωμοσωμικές μετατοπίσεις κωδικοποιούν πρωτεΐνεςσύντηξης, συνήθωςπαραγόντων μεταγραφής των οποίων οι ιδιότητες μεταβάλλονται και μπορούν να προκαλέσουν την διακοπή διαφοροποίησης."[30]Για παράδειγμα, στην οξεία προμυελοκυτταρική λευχαιμία, η t (15, 17) μετατόπιση παράγει την πρωτεΐνη σύντηξης PML-RARα, που συνδέεται με το ρετινοϊκό οξύ του υποδοχέα στους προαγωγείς των διαφόρων ειδικευμένων για μυελοειδή γονιδίων και αναστέλλει τη μυελοειδή διαφοροποίηση .[31]
Τα κλινικά σημεία και συμπτώματα λόγω ΟΜΛ απορρέουν από τη συνεχή αύξηση των λευχαιμικών κυττάρων, τα οποία τείνουν να εκτοπίσουν και να παρεμποδίσουν την ανάπτυξη των φυσιολογικών κυττάρων του μυελού των οστών.[32] Αυτό οδηγεί σε ουδετεροπενία, αναιμία και θρομβοπενία. Τα συμπτώματα της ΟΜΛ πολλές φορές οφείλονται στο χαμηλό αριθμό αυτών στοιχείων του αίματος. Σε σπάνιες περιπτώσεις, οι ασθενείς μπορεί να αναπτύξουν χλώρωμα ή στερεούς όγκους των λευχαιμικών κυττάρων έξω από το μυελό των οστών, οι οποίοι μπορούν να προκαλέσουν διάφορα συμπτώματα ανάλογα με τη θέση τους.[5]
Θεραπεία
[Επεξεργασία | επεξεργασία κώδικα]Η πρώτης γραμμής θεραπεία της ΟΜΛ αποτελείται κυρίως από τη χημειοθεραπεία, και χωρίζεται σε δύο φάσεις: επαγωγής και εδραίωσης. Ο στόχος της θεραπείας επαγωγής είναι να επιτευχθεί πλήρης ύφεση με μείωση του αριθμού των λευχαιμικών κυττάρων σε μη ανιχνεύσιμο επίπεδο. Στους στόχους της θεραπείας εδραίωσης είναι η εξάλειψη κάθε υπολειπόμενης μη ανιχνεύσιμης ασθένειας και να επιτευχθεί μια θεραπεία.[33]Μεταμόσχευση αιμοποιητικών βλαστικών κυττάρων είναι συνήθως απαραίτητη, αν η χημειοθεραπεία εφόδου αποτύχει ή μετά από υποτροπές των ασθενών, αν και η μεταμόσχευση επίσης, μερικές φορές χρησιμοποιείται ως πρώτης γραμμής θεραπεία για ασθενείς με υψηλού κινδύνου νόσο.
Επαγωγή
[Επεξεργασία | επεξεργασία κώδικα]Όλες οι υποκατηγορίες FAB εκτός Μ3 συνήθως παίρνουν χημειοθεραπεία εφόδου με κυταραβίνης (ara-C) και μια ανθρακυκλίνη (όπως δαουνορουβικίνη ή idarubicin).[34] Αυτή η χημειοθεραπεία εφόδου είναι γνωστή ως "7 +3" (ή "3+ 7" ), διότι η κυταραβίνη, παρέχεται ως συνεχής έγχυση IV για επτά συνεχείς ημέρες, ενώ η ανθρακυκλίνη δίνεται για τρεις διαδοχικές ημέρες ως πάτημα IV. Έως 70% των ασθενών θα επιτύχει τη διαγραφή με αυτό το πρωτόκολλο.[35] Άλλα εναλλακτικά σχήματα επαγωγής, συμπεριλαμβανομένης της υψηλής δόσης κυταραβίνης μόνη της ή με δοκιμαζόμενους παράγοντες, μπορούν επίσης να χρησιμοποιηθούν.[36][37] Λόγω των τοξικών επιδράσεων των θεραπειών, συμπεριλαμβανομένων της μυελοκαταστολής και του αυξημένου κίνδυνου λοίμωξης, η χημειοθεραπεία εφόδου δεν μπορεί να προσφέρεται για πολύ ηλικιωμένους, και οι επιλογές μπορεί να περιλαμβάνουν λιγότερο έντονη χημειοθεραπεία ή παρηγορητική φροντίδα.
Ο υπότυπος Μ3 της AML, γνωστός και ως οξεία προμυελοκυτταρική λευχαιμία, θεραπεύεται με το φάρμακο ATRA (all-trans-ρετινοϊκό οξύ) σε συνδυασμό με χημειοθεραπεία εφόδου, συνήθως μια ανθρακυκλίνη.[38][39][40] Ιδιαίτερη προσοχή πρέπει να δοθεί για αποφυγή της διάχυτης ενδοαγγειακής πίεσης, περιπλέκοντας την αντιμετώπιση των ΝΚΠ, όταν τα προμυελοκύτταρα απελευθερώσουν το περιεχόμενο των κοκκίων τους στην περιφερική κυκλοφορία. Η ΟΜΛ είναι κατ 'εξοχήν ιάσιμη με καλά τεκμηριωμένα θεραπευτικά πρωτοκόλλα.
Ο στόχος της φάσης επαγωγής είναι να καταλήξει σε πλήρη ύφεση. Πλήρης ύφεση δεν σημαίνει ότι η νόσος έχει θεραπευτεί, αλλά περισσότερο σημαίνει ότι δεν μπορεί να ανιχνευθεί με τις διαθέσιμες διαγνωστικές μεθόδους.[34] Πλήρης ύφεση επιτυγχάνεται σε περίπου 50% -75% των νεοδιαγνωσθέντων ενηλίκων, αν και αυτό μπορεί να ποικίλλει ανάλογα τους προγνωστικούς παράγοντες που περιγράφονται παραπάνω.[41] Η διάρκεια της ύφεσης εξαρτάται από τα προγνωστικά χαρακτηριστικά της αρχικής λευχαιμίας. Σε γενικές γραμμές, όλες οι υφέσεις θα αποτύχουν χωρίς επιπλέον θεραπεία .[42]
Εδραίωση
[Επεξεργασία | επεξεργασία κώδικα]Ακόμη και μετά την επίτευξη πλήρης υποχώρησης, τα λευχαιμικά κύτταρα πιθανόν να παραμείνουν σε αριθμό μικρό, πολύ μικρό για να ανιχνευθεί με τις τρέχουσες διαγνωστικές τεχνικές. Εάν δεν δοθεί περαιτέρω συντήρηση ή θεραπεία σταθεροποίησης, σχεδόν όλοι οι ασθενείς τελικά θα υποτροπιάσουν.[43] Ως εκ τούτου, επιπλέον θεραπεία είναι απαραίτητη για την εξάλειψη των μη ανιχνεύσιμων επίπεδων της νόσου και την πρόληψη της υποτροπής - δηλαδή, για να επιτευχθεί μια θεραπεία.
Το συγκεκριμένο είδος θεραπείας αποκατάστασης είναι εξατομικευμένο βάση προγνωστικούς παράγοντες του ασθενούς (βλέπε παραπάνω) και τη γενική υγεία. Για την καλή πρόγνωση για λευχαιμίες (δηλαδή inv (16), t (8? 21), και t (15? 17)), οι ασθενείς υποβάλλονται συνήθως σε ένα επιπλέον κύκλο 3-5 επισκέψεων εντατικής χημειοθεραπείας, που είναι γνωστή ως χημειοθεραπεία εδραίωσης.[44][45] Για τους ασθενείς που διατρέχουν υψηλό κίνδυνο υποτροπής (π.χ. άτομα με υψηλό κίνδυνο κυτταρογενετικής, υποκείμενη MDS, ή η θεραπεία που σχετίζεται με AMΟΜΛ), η αλλογενής μεταμόσχευση βλαστικών κυττάρων συνιστάται συνήθως αν ο ασθενής είναι σε θέση να ανεχτεί μια μεταμόσχευση και υπάρχει κατάλληλος δότης. Η καλύτερη θεραπεία αποκατάστασης για τις ενδιάμεσου κινδύνου ΟΜΛ (κανονική κυτταρογενετική ή αλλαγές κυτταρογενετικής που δεν εμπίπτουν σε καλή κινδύνου ή σε ομάδες υψηλού κινδύνου) είναι λιγότερο σαφής και εξαρτάται από τη συγκεκριμένη κατάσταση, συμπεριλαμβανομένης της ηλικίας και της γενικής υγείας του ασθενούς, τις προσωπικού αξίες του ασθενούς, και κατά πόσον ένας συμβατός δότης βλαστοκυττάρων είναι διαθέσιμος. .[45]
Για τους ασθενείς που δεν είναι κατάλληλοι για μεταμόσχευση βλαστικών κυττάρων, η ανοσοθεραπεία με συνδυασμό διυδροχλωρική ισταμίνη(Ceplene) και της ιντερλευκίνης-2 (Proleukin) μετά την ολοκλήρωση της εδραίωσης έχει αποδειχθεί ότι μειώνει τον απόλυτο κίνδυνο υποτροπής κατά 14%, οδηγώντας σε 50% αύξηση της πιθανότητας να διατηρηθεί η ύφεση.[46]
Υποτροπιάζουσες ΟΜΛ
[Επεξεργασία | επεξεργασία κώδικα]Για τους ασθενείς με υποτροπιάζουσα οξεία μυελογενή λευχαιμία, η μόνη αποδεδειγμένη δυνητικά θεραπευτική αγωγή είναι ημεταμόσχευση αιμοποιητικών βλαστικών κυττάρων, εάν δεν έχει ήδη πραγματοποιηθεί.[47][48][49] Το 2000, ο κυτταροτοξικός παράγοντας συνδεδεμένος σε μονοκλωνικά αντισώματα γεμτουζουμάμπη οζογαμισίνη (Mylotarg) εγκρίθηκε στις Ηνωμένες Πολιτείες για τους ασθενείς ηλικίας άνω των 60 χρόνων με υποτροπιάζουσα ΟΜΛ που δεν είναι υποψήφιοι για χημειοθεραπεία υψηλών δόσεων.[50]
Οι ασθενείς με υποτροπιάζουσα ΟΜΛ που δεν είναι υποψήφιοι για μεταμόσχευση βλαστικών κυττάρων ή που έχουν υποτροπιάσει μετά από μία μεταμόσχευση βλαστικών κυττάρων, μπορεί να τους προταθεί θεραπεία σε κλινική δοκιμή, όμως είναι περιορισμένες οι συμβατικές θεραπευτικές επιλογές. Παράγοντες υπό έρευνα περιλαμβάνουν κυτταροτοξικά φάρμακα, όπως η κλοφαραβίνη καθώς και στοχευμένες θεραπείες, όπως η φαρνεσυλ-τρανσφεράση αναστολείς, Decitabine, και αναστολείς του MDR1 (πολυανθεκτικών-αντίσταση πρωτεΐνη). Δεδομένου ότι οι θεραπευτικές επιλογές για την υποτροπιάζουσα ΟΜΛ είναι τόσο περιορισμένες, μια άλλη επιλογή που μπορεί να προσφέρθει είναι η ψυχολογική στήριξη.
Για την υποτροπιάζουσα οξεία προμυελοκυτταρική λευχαιμία (APL),το τριοξείδιο του αρσενικού έχει δοκιμαστεί σε δοκιμές και έχει εγκριθεί από την Υπηρεσία Τροφίμων και Φαρμάκων,FDA. Όπως το ATRA,έτσι και το τριοξείδιο του αρσενικού δεν λειτουργεί με τις άλλες υποκατηγορίες της ΟΜΛ..[51]
Πρόγνωση
[Επεξεργασία | επεξεργασία κώδικα]
Η Οξεία Μυελογενής Λευχαιμία είναι μια θεραπεύσιμη ασθένεια. Οι πιθανότητες θεραπείας ενός ασθενή εξαρτώνται από μια πληθώρα προγνωστικών παραγόντων. [52]
Κυτταρογενετική
[Επεξεργασία | επεξεργασία κώδικα]Ο σημαντικότερος προγνωστικός παράγοντας στην Ο.Μ.Λ είναι η κυτταρογενετική ή η χρωμοσωμική δομή των λευχαιμικών κυττάρων. Συγκεκριμένες κυτταρογενετικές ανωμαλίες σχετίζονται με πολύ θετικά αποτελέσματα (για παράδειγμα η (15;17) μετατόπιση στην οξεία προμυελοκυτταρική λευχαιμία). Σχεδόν οι μισοί ασθενείς με Ο.Μ.Λ έχουν "φυσιολογική" κυτταρογενετική και αποτελούν μια ενδιάμεση ομάδα κινδύνου. Ένας αριθμός άλλων κυτταρογενετικών ανωμαλιών είναι γνωστό ότι σχετίζονται με κακή πρόγνωση και υψηλό ρίσκο υποτροπής μετά την θεραπεία.[53][54][55]
Η πρώτη δημοσίευση που ανέφερε την κυτταρογενετική ήταν οι κλινικές δοκιμές του Medical Research Council το 1998.[56]
| Επίπεδο Επικινδυνότητας | Ανωμαλία | Επιβίωση μετά από 5 έτη | Βαθμός Υποτροπής |
|---|---|---|---|
| Καλό | t(8;21), t(15;17), inv(16) | 70% | 33% |
| Μεσαίο | Φυσιολογικό, +8, +21, +22, del(7q), del(9q), Ανώμαλο 11q23, όλες οι άλλες δομικές ή ποσοτικές αλλαγές | 48% | 50% |
| Κακό | -5, -7, del(5q), Abnormal 3q, Complex cytogenetics | 15% | 78% |
Αργότερα, η Νοτιοδυτική Ογκολογική Ομάδα και το Ανατολικό Συνεργατικό Ογκολογικό Συνέδριο[57] και αργότερα, το Συνέδριο Καρκίνου και Λευχαιμίας, δημοσίευσαν άλλες, κυρίως αλληλεπικαλυπτόμενες λίστες κυτταρογενετικής πρόγνωσης στην λευχαιμία. [58]
Μυελοδυσπλαστικό Σύνδρομο
[Επεξεργασία | επεξεργασία κώδικα]Η Ο.Μ.Λ που προκύπτει από ένα προϋπάρχον μυελοδυσπλαστικό σύνδρομο ή μια μυελοϋπερπλαστική ασθένεια (την διαβόητη δευτερεύουσα Ο.Μ.Λ) έχει χειρότερη πρόγνωση, όπως και η σχετιζόμενη με θεραπεία Ο.Μ.Λ, η οποία προκύπτει έπειτα από χημειοθεραπεία για κάποια άλλη προηγούμενη κακοήθεια. Και οι δύο αυτές περιπτώσεις σχετίζονται σε υψηλό βαθμό με δυσμενείς κυτταρογενετικές ανωμαλίες..[59][60][61]
Άλλοι Προγνωστικοί Παράγοντες
[Επεξεργασία | επεξεργασία κώδικα]Σε κάποιες μελέτες, σε ηλικίες μεγαλύτερες των 60 ετών, τα επίπεδα γαλακτικής αφυδρογονάσης επίσης σχετίζονταν με άσχημα αποτελέσματα.[62] Όπως και στις περισσότερες μορφές καρκίνου η κατάσταση απόδοσης (δηλαδή, η γενική φυσική κατάσταση, και τα επίπεδα δραστηριότητας του ασθενούς) παίζει σημαντικό ρόλο στην πρόγνωση.
Οι εσωτερικοί αναδιπλασιασμοί της ακολουθίας FLT3, επίσης συμβάλουν στην κακή πρόγνωση της Ο.Μ.Λ.[63] Η θεραπεία αυτών των ασθενών με πιο επιθετικές μεθόδους, όπως η μεταμόσχευση αρχέγονων κυττάρων στην πρώτη ύφεση, δεν αποδείχθηκε να ενισχύει την μακροπρόθεσμη επιβίωσή τους. Συνεπώς αυτό το προγνωστικό χαρακτηριστικό έχει αβέβαιη κλινική σημασία αυτή τη στιγμή.[64] Οι εσωτερικοί αναδιπλασιασμοί της ακολουθίας FLT3 μπορεί να σχετίζονται με λευκόσταση.[65]
Ερευνητές ελέγχουν την κλινική σημασία των μεταλλάξεων του c-KIT στην Ο.Μ.Λ.[66] Αυτές είναι οι επικρατούσες, αλλά και κλινικά σχετικές λόγω της διαθεσιμότητας αναστολέων τυροσινικής κινάσης, οι οποίοι μπορούν να μπλοκάρουν την δραστηριότητα του c-KIT φαρμακολογικά.
Άλλα γονίδια που ερευνόνται ως προγνωστικοί παράγοντες ή πιθανοί θεραπευτικοί στόχοι περιλαμβάνουν τα CEBPA, BAALC, ERG, και NPM1.
Συνολική Προσδοκία Θεραπείας
[Επεξεργασία | επεξεργασία κώδικα]Ο βαθμός θεραπείας σε κλινικές δοκιμές ποικίλλουν από 20 έως 45%.[67][68] Ωστόσο οι κλινικές μελέτες συχνά αφορούν νεότερους ασθενείς, αλλά και ασθενείς που μπορούν να αντέξουν επιθετικότερες μορφές θεραπείας. Ο συνολικός βαθμός θεραπείας (συμπεριλαμβανομένων των ηλικιωμένων, και αυτών που αδυνατούν να υποστούν επιθετική θεραπεία) είναι πιθανότατα χαμηλότερος. Ο βαθμός θεραπείας για την προμυελοκυτταρική λευχαιμία μπορεί να αγγίξει μέχρι και το 98%. [69]
Επιδημιολογία
[Επεξεργασία | επεξεργασία κώδικα]Η οξεία μυελογενής λευχαιμία είναι μια σχετικά σπάνια μορφή καρκίνου. Στις Ηνωμένες Πολιτείες Αμερικής υπάρχουν περίπου 10.500 νέα περιστατικά κάθε χρόνο και ο μέσος όρος κρουσμάτων ανά χρόνο ήταν σταθερός από το 1995 έως το 2005. Η Ο.Μ.Λ ευθύνεται για το 1.2% των θανάτων λόγω καρκίνου στις Ηνωμένες Πολιτείες.[1]
Η πιθανότητα εμφάνισης Ο.Μ.Λ αυξάνεται με την ηλικία, με την μέση ηλικία διάγνωσης να βρίσκεται στα 63. Η Ο.Μ.Λ αποτελεί το 90% των μορφών οξείας λευχαιμίας σε όλους τους ενήλικες, αλλά είναι πολύ σπάνια σε παιδιά.[1] Ο αριθμός κρουσμάτων της σχετιζόμενης με θεραπεία Ο.Μ.Λ (δηλαδή Ο.Μ.Λ που οφείλεται σε χημειοθεραπεία για κάποια άλλη προηγούμενη ασθένεια) αυξάνεται. Τα ποσοστά της κυμαίνονται σε 10-20% όλων των περιπτώσεων Ο.Μ.Λ.[70] Η Ο.Μ.Λ συναντάται συχνότερα σε άνδρες με αναλογία ανδρών-γυναικών 1,3:1.[71]
Υπάρχει γεωγραφική διαφοροποίηση στα κρούσματα Ο.Μ.Λ. Στους ενήλικες, τα περισσότερα κρούσματα εμφανίζονται σε Βόρεια Αμερική, Ευρώπη και Ωκεανία, ενώ είναι σπανιότερη σε Ασία και Λατινική Αμερική.[72][73] Αντιθέτως η παιδική Ο.Μ.Λ είναι σπανιότερη σε Βόρεια Αμερική, αλλά και στην Ινδία, απ'ότι σε άλλα μέρη της Ασίας.[74] Αυτές οι γεωγραφικές διαφοροποιήσεις πιθανόν να οφείλονται στα διαφορετικά φυλετικά γονίδια, σε περιβαλλοντικούς παράγοντες ή σε συνδυασμό των παραπάνω.
Ιστορικό
[Επεξεργασία | επεξεργασία κώδικα]
Η πρώτη δημοσιευμένη περιγραφή ενός περιστατικού λευχαιμίας στην ιατρική λογοτεχνία, έγινε το 1827, όταν ο Γάλλος φυσιολόγος Alfred-Armand-Louis-Marie Velpeau περιέγραψε έναν εξηντατριάχρονο ανθοπώλη, ο οποίος ανέπτυξε μια ασθένεια, που χαρακτηριζόταν από αδυναμία, πυρετό, πέτρες στα νεφρά και σημαντική διόγκωση του ήπατος και της σπλήνας. Ο Volpeau περιέγραψε την συνοχή του αίματος του ασθενούς "σαν χυλό" και πρότεινε ότι η εμφάνιση του αίματος οφειλόταν στην ύπαρξη λευκών αιμοσφαιρίων.[75] Το 1845 μια σειρά ασθενών, οι οποίοι πέθαναν, με διογκωμένες σπλήνες και και μεταβολές "στο χρώμα και στην συνοχή του αίματος" παρατηρήθηκε από τον παθολογοανατόμο J.H. Bennett. Χρησιμοποίησε τον όρο "λευκοκυτταραιμία" για να περιγράψει την παθολογική αυτή κατάσταση.[76]
Ο όρος "λευχαιμία" επινοήθηκε από τον Ρούντολφ Βίρχοβ, ονομαστό Γερμανό παθολόγο, το 1856. Ως πρωτοπόρος στην χρήση του οπτικού μικροσκοπίου, ο Virchow ήταν ο πρώτος που περιέγραψε το ασυνήθιστα μεγάλο πλήθος λευκών αιμοσφαιρίων στο αίμα, σε ασθενείς με το κλινικό σύνδρομο που περιέγραψαν οι Velpau και Bennett. Καθώς ο Virchow ήταν αβέβαιος για την αιτιολογία του μεγάλου αριθμού λευκών αιμοσφαιρίων στο αίμα, χρησιμοποίησε τον καθαρά περιγραφικό όρο "λευχαιμία" (Ελληνικά: λευκό αίμα) για να αναφερθεί στην κατάσταση αυτή.[77]
Περαιτέρω πρόοδος στην κατανόηση της Ο.Μ.Λ. έγινε με ταχείς ρυθμούς μετά την ανάπτυξη νέων τεχνολογιών. Το 1877 ο Πάουλ Έρλιχ ανέπτυξε την τεχνική της χρώσης ταινιών αίματος, που του επέτρεψε να περιγράψει εις βάθος και με ακριβείς λεπτομέρειες φυσιολογικά και μη φυσιολογικά λευκά αιμοσφαίρια. Ο Βίλχεμ Εμπστάιν εισήγαγε τον όρο "Οξεία λευχαιμία" το 1889 για να διαχωρίσει τις ραγδαία αναπτυσσόμενες και θανατηφόρες μορφές λευχαιμίας, από τις πιο νωχελικές, χρόνιες μορφές λευχαιμίας.[78] Ο όρος "μυελογενής" επινοήθηκε από τον Neumann το 1869, καθώς ήταν ο πρώτος που κατανόησε ότι τα λευκά αιμοσφαίρια παράγονται στον μυελό των οστών, εξ'ου και "μυελογενής, και όχι στον σπλήνα. Η τεχνική εξέτασης του μυελού των οστών για τη διάγνωση της λευχαιμίας περιγράφτηκε πρώτη φορά από τον Mosler το 1879.[79] Τελικά το 1900 ο μυελοβλάστης, που είναι το κακόηθες κύτταρο στην Ο.Μ.Λ παρατηρήθηκε από τον Otto Naegeli, ο οποίος χώρισε τις λευχαιμίες σε "μυελογενείς" και "λεμφοκυτταρικές".[80][81] Το 2008 η Ο.Μ.Λ έγινε η πρώτη ασθένεια, της οποίας το καρκινικό γονιδίωμα έχει πλήρως χαρτογραφηθεί. Γενετικό υλικό από λευχαιμικά κύτταρα συγκρίθηκε με αυτό υγειών δερματικών κυττάρων.[82] Τα λευχαιμικά κύτταρα απέκτησαν μεταλλάξεις σε αρκετά γονίδια, τα οποία μέχρι πρότινος πιστεύονταν να μην σχετίζονται με την ασθένεια.
Εγκυμοσύνη
[Επεξεργασία | επεξεργασία κώδικα]Η λευχαιμία, σπανίως σχετίζεται με την εγκυμοσύνη, επηρεάζοντας μόνο μία σε κάθε 10.000 εγκυμονούσες γυναίκες.[83] Η αντιμετώπισή της εξαρτάται ολοκληρωτικά από το είδος της. Οι οξείες μορφές λευχαιμίας, φυσιολογικά απαιτούν άμεση, επιθετική θεραπεία, παρά το αυξημένο ρίσκο αποβολής του εμβρύου και γενετικών ανωμαλιών, ειδικά εάν γίνεται χημειοθεραπεία, κατά το αναπτυξιακά ευαίσθητο πρώτο τρίμηνο. [83]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ 1,0 1,1 1,2 Jemal A, Thomas A, Murray T, Thun M (2002). «Cancer statistics, 2002». CA Cancer J Clin 52 (1): 23–47. doi:. PMID 11814064. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-01-28. https://web.archive.org/web/20110128054629/http://caonline.amcancersoc.org/cgi/content/full/52/1/23. Ανακτήθηκε στις 2011-11-27.
- ↑ 2,0 2,1 Vardiman JW, Harris NL, Brunning RD (2002). «The World Health Organization (WHO) classification of the myeloid neoplasms». Blood 100 (7): 2292–302. doi:. PMID 12239137. Αρχειοθετήθηκε από το πρωτότυπο στις 2009-12-17. https://web.archive.org/web/20091217161643/http://bloodjournal.hematologylibrary.org/cgi/content/full/100/7/2292. Ανακτήθηκε στις 2011-11-28.
- ↑ Bennett J, Catovsky D, Daniel M, Flandrin G, Galton D, Gralnick H, Sultan C (1976). «Proposals for the classification of the acute leukaemias. French-American-British (FAB) co-operative group». Br J Haematol 33 (4): 451–8. doi:. PMID 188440.
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 4,6 4,7 4,8 Seiter, Karen· Jules, E Harris (20 Μαΐου 2011). «Acute Myeloid Leukemia Staging». Ανακτήθηκε στις 26 Αυγούστου 2011.
- ↑ 5,0 5,1 5,2 5,3 Hoffman, Ronald (2005). Hematology: Basic Principles and Practice (4η έκδοση). St. Louis, Mo.: Elsevier Churchill Livingstone. σελίδες 1074–75. ISBN 0-443-06629-9.
- ↑ Abeloff, Martin (2004). Clinical Oncology (3η έκδοση). St. Louis, Mo.: Elsevier Churchill Livingstone. σελ. 2834. ISBN 0-443-06629-9.
- ↑ Sanz G, Sanz M, Vallespí T, Cañizo M, Torrabadella M, García S, Irriguible D, San Miguel J (1989). «Two regression models and a scoring system for predicting survival and planning treatment in myelodysplastic syndromes: a multivariate analysis of prognostic factors in 370 patients». Blood 74 (1): 395–408. PMID 2752119.
- ↑ Le Beau M, Albain K, Larson R, Vardiman J, Davis E, Blough R, Golomb H, Rowley J (1986). «Clinical and cytogenetic correlations in 63 patients with therapy-related myelodysplastic syndromes and acute nonlymphocytic leukemia: further evidence for characteristic abnormalities of chromosomes no. 5 and 7». J Clin Oncol 4 (3): 325–45. PMID 3950675.
- ↑ Thirman M, Gill H, Burnett R, Mbangkollo D, McCabe N, Kobayashi H, Ziemin-van der Poel S, Kaneko Y, Morgan R, Sandberg A (1993). «Rearrangement of the MLL gene in acute lymphoblastic and acute myeloid leukemias with 11q23 chromosomal translocations». N Engl J Med 329 (13): 909–14. doi:. PMID 8361504.
- ↑ Austin H, Delzell E, Cole P (1988). «Benzene and leukemia. A review of the literature and a risk assessment». Am J Epidemiol 127 (3): 419–39. PMID 3277397.
- ↑ Linet, MS. The Leukemias: Epidemiologic Aspects. Oxford University Press, New York 1985.
- ↑ Bizzozero O, Johnson K, Ciocco A (1966). «Radiation-related leukemia in Hiroshima and Nagasaki, 1946–1964. I. Distribution, incidence and appearance time». N Engl J Med 274 (20): 1095–101. doi:. PMID 5932020.
- ↑ Yoshinaga S, Mabuchi K, Sigurdson A, Doody M, Ron E (2004). «Cancer risks among radiologists and radiologic technologists: review of epidemiologic studies». Radiology 233 (2): 313–21. doi:. PMID 15375227. https://archive.org/details/sim_radiology_2004-11_233_2/page/313.
- ↑ Taylor GM, Birch JM (1996). «The hereditary basis of human leukemia». Στο: Henderson ES, Lister TA, Greaves MF. Leukemia (6th έκδοση). Philadelphia: WB Saunders. σελ. 210. ISBN 0-7216-5381-2.
- ↑ Horwitz M, Goode EL, Jarvik GP (1996). «Anticipation in familial leukemia». Am. J. Hum. Genet. 59 (5): 990–8. PMID 8900225. PMC 1914843. https://archive.org/details/sim_american-journal-of-human-genetics_1996-11_59_5/page/990. Πλήρες κείμενο στο PMC: 1914843
- ↑ Crittenden LB (1961). «An interpretation of familial aggregation based on multiple genetic and environmental factors». Ann. N. Y. Acad. Sci. 91 (3): 769–80. doi:. PMID 13696504. Bibcode: 1961NYASA..91..769C.
- ↑ Horwitz M (1997). «The genetics of familial leukemia». Leukemia 11 (8): 1347–59. doi:. PMID 9264391.
- ↑ Gunz FW, Veale AM (1969). «Leukemia in close relatives--accident or predisposition?». J. Natl. Cancer Inst. 42 (3): 517–24. PMID 4180615. https://archive.org/details/sim_journal-of-the-national-cancer-institute_1969-03_42_3/page/517.
- ↑ Evans D, Steward J (1972). «Down's syndrome and leukaemia». Lancet 2 (7790): 1322. doi:. PMID 4117858.
- ↑ Abeloff, Martin et al. (2004), σελ. 2834.
- ↑ Baldus CD, Mrózek K, Marcucci G, Bloomfield CD (Ιούνιος 2007). «Clinical outcome of de novo acute myeloid leukaemia patients with normal cytogenetics is affected by molecular genetic alterations: a concise review». Br. J. Haematol. 137 (5): 387–400. doi:. PMID 17488484.
- ↑ Abeloff, Martin et al. (2004), σελ. 2835.
- ↑ Harris N, Jaffe E, Diebold J, Flandrin G, Muller-Hermelink H, Vardiman J, Lister T, Bloomfield C (1999). «The World Health Organization classification of neoplastic diseases of the hematopoietic and lymphoid tissues. Report of the Clinical Advisory Committee meeting, Airlie House, Virginia, November, 1997». Ann Oncol 10 (12): 1419–32. doi:. PMID 10643532. https://archive.org/details/sim_annals-of-oncology_1999-12_10_12/page/1419.
- ↑ Amin, H. M.; Yang, Y.; Shen, Y.; Estey, E. H.; Giles, F. J.; Pierce, S. A.; Kantarjian, H. M.; O'Brien, S. M. και άλλοι. (2005). «Having a higher blast percentage in circulation than bone marrow: Clinical implications in myelodysplastic syndrome and acute lymphoid and myeloid leukemias». Leukemia 19 (9): 1567–1572. doi:. PMID 16049515.
- ↑ Grimwade D, Howe K, Langabeer S, Davies L, Oliver F, Walker H, Swirsky D, Wheatley K, Goldstone A, Burnett A, Solomon E (1996). «Establishing the presence of the t(15;17) in suspected acute promyelocytic leukaemia: cytogenetic, molecular and PML immunofluorescence assessment of patients entered into the M.R.C. ATRA trial. M.R.C. Adult Leukaemia Working Party». Br J Haematol 94 (3): 557–73. PMID 8790159. https://archive.org/details/sim_british-journal-of-haematology_1996-09_94_3/page/557.
- ↑ Fialkow PJ (1976). «Clonal origin of human tumors». Biochim. Biophys. Acta 458 (3): 283–321. doi:. PMID 1067873.
- ↑ Fialkow PJ, Janssen JW, Bartram CR (1 Απριλίου 1991). «Clonal remissions in acute nonlymphocytic leukemia: evidence for a multistep pathogenesis of the malignancy» (PDF). Blood 77 (7): 1415–7. PMID 2009365. Αρχειοθετήθηκε από το πρωτότυπο στις 2009-09-23. https://web.archive.org/web/20090923205004/http://bloodjournal.hematologylibrary.org/cgi/reprint/77/7/1415. Ανακτήθηκε στις 2011-11-30.
- ↑ Bonnet D, Dick JE (1997). «Human acute myeloid leukemia is organized as a hierarchy that originates from a primitive hematopoietic cell». Nat. Med. 3 (7): 730–7. doi:. PMID 9212098.
- ↑ Abeloff, Martin και άλλοι (2004), σελ. 2831–32.
- ↑ Greer JP· και άλλοι., επιμ. (2004). Wintrobe's Clinical Hematology (11th έκδοση). Philadelphia: Lippincott, Williams, and Wilkins. σελίδες 2045–2062. ISBN 0-7817-3650-1.
- ↑ Melnick A, Licht JD (15 Μαΐου 1999). «Deconstructing a disease: RARα, its fusion partners, and their roles in the pathogenesis of acute promyelocytic leukemia». Blood 93 (10): 3167–215. PMID 10233871. Αρχειοθετήθηκε από το πρωτότυπο στις 2009-12-17. https://web.archive.org/web/20091217143052/http://bloodjournal.hematologylibrary.org/cgi/content/full/93/10/3167. Ανακτήθηκε στις 2011-11-30.
- ↑ Abeloff, Martin et al. (2004), σελ. 2828.
- ↑ Acute myeloid leukemia Αρχειοθετήθηκε 2009-09-26 στο Wayback Machine. at Mount Sinai Hospital
- ↑ 34,0 34,1 Abeloff, Martin και άλλοι (2004), σελ. 2835–39.
- ↑ Bishop J (1997). «The treatment of adult acute myeloid leukemia». Semin Oncol 24 (1): 57–69. PMID 9045305. https://archive.org/details/sim_seminars-in-oncology_1997-02_24_1/page/57.
- ↑ Weick JK, Kopecky KJ, Appelbaum FR, Head, DR, Kingsbury, LL, Balcerzak, SP, Bickers, JN, Hynes, HE και άλλοι. (15 Οκτωβρίου 1996). «A randomized investigation of high-dose versus standard-dose cytosine arabinoside with daunorubicin in patients with previously untreated acute myeloid leukemia: a Southwest Oncology Group study» (PDF). Blood 88 (8): 2841–51. PMID 8874180. Αρχειοθετήθηκε από το πρωτότυπο στις 2009-09-23. https://web.archive.org/web/20090923205009/http://bloodjournal.hematologylibrary.org/cgi/reprint/88/8/2841. Ανακτήθηκε στις 2011-11-30.
- ↑ Bishop JF, Matthews JP, Young GA, Szer, J, Gillett, A, Joshua, D, Bradstock, K, Enno, A και άλλοι. (1 Μαρτίου 1996). «A randomized study of high-dose cytarabine in induction in acute myeloid leukemia» (PDF). Blood 87 (5): 1710–7. PMID 8634416. Αρχειοθετήθηκε από το πρωτότυπο στις 2009-04-21. https://web.archive.org/web/20090421123351/http://bloodjournal.hematologylibrary.org/cgi/reprint/87/5/1710. Ανακτήθηκε στις 2011-11-30.
- ↑ Huang ME, Ye YC, Chen SR, Chai, JR, Lu, JX, Zhoa, L, Gu, LJ, Wang, ZY (1 Αυγούστου 1988). «Use of all-trans retinoic acid in the treatment of acute promyelocytic leukemia» (PDF). Blood 72 (2): 567–72. PMID 3165295. Αρχειοθετήθηκε από το πρωτότυπο στις 2009-09-23. https://web.archive.org/web/20090923204959/http://bloodjournal.hematologylibrary.org/cgi/reprint/72/2/567. Ανακτήθηκε στις 2011-11-30.
- ↑ Tallman MS, Andersen JW, Schiffer CA, Appelbaum, Frederick R., Feusner, James H., Ogden, Angela, Shepherd, Lois, Willman, Cheryl και άλλοι. (1997). «All-trans-retinoic acid in acute promyelocytic leukemia». N. Engl. J. Med. 337 (15): 1021–8. doi:. PMID 9321529. Αρχειοθετήθηκε από το πρωτότυπο στις 2009-09-25. https://web.archive.org/web/20090925093142/http://content.nejm.org/cgi/content/full/337/15/1021. Ανακτήθηκε στις 2011-11-30.
- ↑ Fenaux P, Chastang C, Chevret S, Sanz, M, Dombret, Η, Archimbaud, E, Fey, M, Rayon, C και άλλοι. (15 Αυγούστου 1999). «A randomized comparison of all transretinoic acid (ATRA) followed by chemotherapy and ATRA plus chemotherapy and the role of maintenance therapy in newly diagnosed acute promyelocytic leukemia. The European APL Group». Blood 94 (4): 1192–200. PMID 10438706. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-10-31. https://web.archive.org/web/20101031140014/http://bloodjournal.hematologylibrary.org/cgi/content/full/94/4/1192. Ανακτήθηκε στις 2011-11-30.
- ↑ Estey E (2002). «Treatment of acute myelogenous leukemia». Oncology (Williston Park) 16 (3): 343–52, 355–6; discussion 357, 362, 365–6. PMID 15046392.
- ↑ Cassileth P, Harrington D, Hines J, Oken M, Mazza J, McGlave P, Bennett J, O'Connell M (1988). «Maintenance chemotherapy prolongs remission duration in adult acute nonlymphocytic leukemia». J Clin Oncol 6 (4): 583–7. PMID 3282032.
- ↑ Cassileth PA, Harrington DP, Hines JD, Oken, MM, Mazza, JJ, McGlave, P, Bennett, JM, O'Connell, MJ (1988). «Maintenance chemotherapy prolongs remission duration in adult acute nonlymphocytic leukemia». J. Clin. Oncol. 6 (4): 583–7. PMID 3282032.
- ↑ Mayer RJ, Davis RB, Schiffer CA, Berg, Deborah T., Powell, Bayard L., Schulman, Philip, Omura, George A., Moore, Joseph O. και άλλοι. (1994). «Intensive postremission chemotherapy in adults with acute myeloid leukemia. Cancer and Leukemia Group B». N. Engl. J. Med. 331 (14): 896–903. doi:. PMID 8078551.
- ↑ 45,0 45,1 Appelbaum FR, Baer MR, Carabasi MH, Coutre, SE, Erba, HP, Estey, E, Glenn, MJ, Kraut, EH και άλλοι. (2000). «NCCN Practice Guidelines for Acute Myelogenous Leukemia». Oncology (Williston Park, N.Y.) 14 (11A): 53–61. PMID 11195419.
- ↑ Brune M, Castaigne S, Catalano J, Gehlsen, K, Ho, AD, Hofmann, WK, Hogge, DE, Nilsson, B και άλλοι. (Ιούλιος 2006). «Improved leukemia-free survival after postconsolidation immunotherapy with histamine dihydrochloride and interleukin-2 in acute myeloid leukemia: results of a randomized phase 3 trial». Blood 108 (1): 88–96. doi:. PMID 16556892. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-03-25. https://web.archive.org/web/20100325091815/http://bloodjournal.hematologylibrary.org/cgi/content/full/108/1/88. Ανακτήθηκε στις 2011-11-30.
- ↑ Abeloff, Martin και άλλοι (2004), σελ. 2840–41.
- ↑ Appelbaum FR (2001). «Editorial: Who should be transplanted for AML?». Leukemia 15 (4): 680–2. doi:. PMID 11368380.
- ↑ Appelbaum FR (2002). «Keynote address: hematopoietic cell transplantation beyond first remission». Leukemia 16 (2): 157–9. doi:. PMID 11840278. http://www.nature.com/leu/journal/v16/n2/full/2402345a.html.
- ↑ Sievers EL, Larson RA, Stadtmauer EA, Estey, E, Löwenberg, B, Dombret, Η, Karanes, C, Theobald, M και άλλοι. (1 Ιουλίου 2001). «Efficacy and safety of gemtuzumab ozogamicin in patients with CD33-positive acute myeloid leukemia in first relapse». J. Clin. Oncol. 19 (13): 3244–54. PMID 11432892. http://jco.ascopubs.org/cgi/content/full/19/13/3244.
- ↑ Soignet SL, Frankel SR, Douer D, Tallman, MS, Kantarjian, Η, Calleja, E, Stone, RM, Kalaycio, M και άλλοι. (15 Σεπτεμβρίου 2001). «United States multicenter study of arsenic trioxide in relapsed acute promyelocytic leukemia». J. Clin. Oncol. 19 (18): 3852–60. PMID 11559723. http://jco.ascopubs.org/cgi/content/full/19/18/3852.
- ↑ Estey E (2001). «Prognostic factors in acute myelogenous leukemia». Leukemia 15 (4): 670–2. doi:. PMID 11368376.
- ↑ Wheatley K, Burnett A, Goldstone A, Gray R, Hann I, Harrison C, Rees J, Stevens R, Walker Η (1999). «A simple, robust, validated and highly predictive index for the determination of risk-directed therapy in acute myeloid leukaemia derived from the MRC AML 10 trial. United Kingdom Medical Research Council's Adult and Childhood Leukaemia Working Parties». Br J Haematol 107 (1): 69–79. doi:. PMID 10520026. https://archive.org/details/sim_british-journal-of-haematology_1999-10_107_1/page/69.
- ↑ Slovak M, Kopecky K, Cassileth P, Harrington D, Theil K, Mohamed A, Paietta E, Willman C, Head D, Rowe J, Forman S, Appelbaum F (15 Δεκεμβρίου 2000). «Karyotypic analysis predicts outcome of preremission and postremission therapy in adult acute myeloid leukemia: a Southwest Oncology Group/Eastern Cooperative Oncology Group Study». Blood 96 (13): 4075–83. PMID 11110676. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-04-10. https://web.archive.org/web/20100410164311/http://bloodjournal.hematologylibrary.org/cgi/content/full/96/13/4075. Ανακτήθηκε στις 2011-11-28.
- ↑ Byrd J, Mrózek K, Dodge R, Carroll A, Edwards C, Arthur D, Pettenati M, Patil S, Rao K, Watson M, Koduru P, Moore J, Stone R, Mayer R, Feldman E, Davey F, Schiffer C, Larson R, Bloomfield C (2002). «Pretreatment cytogenetic abnormalities are predictive of induction success, cumulative incidence of relapse, and overall survival in adult patients with de novo acute myeloid leukemia: results from Cancer and Leukemia Group B (CALGB 8461)». Blood 100 (13): 4325–36. doi:. PMID 12393746. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-04-10. https://web.archive.org/web/20100410164540/http://bloodjournal.hematologylibrary.org/cgi/content/full/100/13/4325. Ανακτήθηκε στις 2011-11-28.
- ↑ Grimwade D, Walker Η, Oliver F, Wheatley, K, Harrison, C, Harrison, G, Rees, J, Hann, I και άλλοι. (1 Οκτωβρίου 1998). «The importance of diagnostic cytogenetics on outcome in AML: analysis of 1,612 patients entered into the MRC AML 10 trial. The Medical Research Council Adult and Children's Leukaemia Working Parties». Blood 92 (7): 2322–33. PMID 9746770. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-01-30. https://web.archive.org/web/20100130014647/http://bloodjournal.hematologylibrary.org/cgi/content/full/92/7/2322. Ανακτήθηκε στις 2011-11-28.
- ↑ Slovak ML, Kopecky KJ, Cassileth PA, Harrington, DH, Theil, KS, Mohamed, A, Paietta, E, Willman, CL και άλλοι. (2000). «Karyotypic analysis predicts outcome of preremission and postremission therapy in adult acute myeloid leukemia: a Southwest Oncology Group/Eastern Cooperative Oncology Group Study». Blood 96 (13): 4075–83. PMID 11110676. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-01-30. https://web.archive.org/web/20100130014647/http://bloodjournal.hematologylibrary.org/cgi/content/full/92/7/2322. Ανακτήθηκε στις 2011-11-28.
- ↑ Byrd J, Mrózek K, Dodge R, Carroll A, Edwards C, Arthur D, Pettenati M, Patil S, Rao K, Watson M, Koduru P, Moore J, Stone R, Mayer R, Feldman E, Davey F, Schiffer C, Larson R, Bloomfield C (2002). «Pretreatment cytogenetic abnormalities are predictive of induction success, cumulative incidence of relapse, and overall survival in adult patients with de novo acute myeloid leukemia: results from Cancer and Leukemia Group B (CALGB 8461)». Blood 100 (13): 4325–36. doi:. PMID 12393746. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-04-10. https://web.archive.org/web/20100410164540/http://bloodjournal.hematologylibrary.org/cgi/content/full/100/13/4325. Ανακτήθηκε στις 2011-11-28.
- ↑ Thirman M, Larson R (1996). «Therapy-related myeloid leukemia». Hematol Oncol Clin North Am 10 (2): 293–320. doi:. PMID 8707757.
- ↑ Rowley J, Golomb H, Vardiman J (1 Οκτωβρίου 1981). «Nonrandom chromosome abnormalities in acute leukemia and dysmyelopoietic syndromes in patients with previously treated malignant disease». Blood 58 (4): 759–67. PMID 7272506. http://bloodjournal.hematologylibrary.org/cgi/content/full/58/4/759.[νεκρός σύνδεσμος]
- ↑ Pedersen-Bjergaard J, Andersen M, Christiansen D, Nerlov C (2002). «Genetic pathways in therapy-related myelodysplasia and acute myeloid leukemia». Blood 99 (6): 1909–12. doi:. PMID 1877259. Αρχειοθετήθηκε από το πρωτότυπο στις 2009-09-23. https://web.archive.org/web/20090923204955/http://bloodjournal.hematologylibrary.org/cgi/content/full/99/6/1909. Ανακτήθηκε στις 2011-11-28.
- ↑ Haferlach T, Schoch C, Löffler Η, Gassmann, W, Kern, W, Schnittger, S, Fonatsch, C, Ludwig, WD και άλλοι. (2003). «Morphologic dysplasia in de novo acute myeloid leukemia (AML) is related to unfavorable cytogenetics but has no independent prognostic relevance under the conditions of intensive induction therapy: results of a multiparameter analysis from the German AML Cooperative Group studies». J. Clin. Oncol. 21 (2): 256–65. doi:. PMID 12525517. http://jco.ascopubs.org/cgi/content/full/21/2/256.
- ↑ Schnittger S, Schoch C, Dugas M, Kern W, Staib P, Wuchter C, Löffler H, Sauerland C, Serve H, Büchner T, Haferlach T, Hiddemann W (2002). «Analysis of FLT3 length mutations in 1003 patients with acute myeloid leukemia: correlation to cytogenetics, FAB subtype, and prognosis in the AMLCG study and usefulness as a marker for the detection of minimal residual disease». Blood 100 (1): 59–66. doi:. PMID 12070009. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-05-15. https://web.archive.org/web/20100515191256/http://bloodjournal.hematologylibrary.org/cgi/content/full/100/1/59. Ανακτήθηκε στις 2011-11-28.
- ↑ Gale RE, Hills R, Kottaridis PD, Srirangan, S, Wheatley, K, Burnett, AK, Linch, DC (2005). «No evidence that FLT3 status should be considered as an indicator for transplantation in acute myeloid leukemia (AML): an analysis of 1135 patients, excluding acute promyelocytic leukemia, from the UK MRC AML10 and 12 trials». Blood 106 (10): 3658–65. doi:. PMID 16076872. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-02-09. https://web.archive.org/web/20110209110028/http://bloodjournal.hematologylibrary.org/cgi/content/full/106/10/3658. Ανακτήθηκε στις 2011-11-28.
- ↑ Thornton KA, Levis M (2007). «Images in clinical medicine. FLT3 Mutation and acute myelogenous leukemia with leukostasis». N. Engl. J. Med. 357 (16): 1639. doi:. PMID 17942876.
- ↑ Paschka P, Marcucci G, Ruppert AS, Mrózek, K, Chen, Η, Kittles, RA, Vukosavljevic, T, Perrotti, D και άλλοι. (2006). «Adverse prognostic significance of KIT mutations in adult acute myeloid leukemia with inv(16) and t(8;21): a Cancer and Leukemia Group B Study». J. Clin. Oncol. 24 (24): 3904–11. doi:. PMID 16921041. http://jco.ascopubs.org/cgi/content/full/24/24/3904.
- ↑ Cassileth PA, Harrington DP, Appelbaum FR, Lazarus, Hillard M., Rowe, Jacob M., Paietta, Elisabeth, Willman, Cheryl, Hurd, David D. και άλλοι. (1998). «Chemotherapy compared with autologous or allogeneic bone marrow transplantation in the management of acute myeloid leukemia in first remission». N. Engl. J. Med. 339 (23): 1649–56. doi:. PMID 9834301. Αρχειοθετήθηκε από το πρωτότυπο στις 2003-02-12. https://web.archive.org/web/20030212235731/http://content.nejm.org/cgi/content/full/339/23/1649. Ανακτήθηκε στις 2011-11-28.
- ↑ Matthews JP, Bishop JF, Young GA, Juneja, S. K., Lowenthal, R. M., Garson, O. M., Cobcroft, R. G., Dodds, A. J. και άλλοι. (2001). «Patterns of failure with increasing intensification of induction chemotherapy for acute myeloid leukaemia». Br. J. Haematol. 113 (3): 727–36. doi:. PMID 11380464. https://archive.org/details/sim_british-journal-of-haematology_2001-06_113_3/page/727.
- ↑ Sanz MA, Lo Coco F, Martín G, Avvisati, G, Rayón, C, Barbui, T, Díaz-Mediavilla, J, Fioritoni, G και άλλοι. (15 Αυγούστου 2000). «Definition of relapse risk and role of nonanthracycline drugs for consolidation in patients with acute promyelocytic leukemia: a joint study of the PETHEMA and GIMEMA cooperative groups». Blood 96 (4): 1247–53. PMID 10942364. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-05-27. https://web.archive.org/web/20100527064934/http://bloodjournal.hematologylibrary.org/cgi/content/full/96/4/1247. Ανακτήθηκε στις 2011-11-28.
- ↑ Leone G, Mele L, Pulsoni A, Equitani F, Pagano L (1 Οκτωβρίου 1999). «The incidence of secondary leukemias». Haematologica 84 (10): 937–45. PMID 10509043. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-10-02. https://web.archive.org/web/20111002154823/http://www.haematologica.org/cgi/reprint/84/10/937. Ανακτήθηκε στις 2011-11-30.
- ↑ Greenlee RT, Hill-Harmon MB, Murray T, Thun M (2001). «Cancer statistics, 2001». CA Cancer J Clin 51 (1): 15–36. doi:. PMID 11577478. Αρχειοθετήθηκε από το πρωτότυπο στις 2010-07-06. https://web.archive.org/web/20100706234501/http://caonline.amcancersoc.org/cgi/content/full/51/1/15. Ανακτήθηκε στις 2011-11-30.
- ↑ Linet MS (1985). «The leukemias: Epidemiologic aspects.». Στο: Lilienfeld AM. Monographs in Epidemiology and Biostatistics. New York: Oxford University Press. σελ. I. ISBN 0-19-503448-1.
- ↑ Aoki K· Kurihars M· Hayakawa N (1992). Death Rates for Malignant Neoplasms for Selected Sites by Sex and Five-Year Age Group in 33 Countries 1953–57 to 1983–87. Nagoya, Japan: University of Nagoya Press, International Union Against Cancer.
- ↑ Bhatia S, Neglia JP (1995). «Epidemiology of childhood acute myelogenous leukemia». J. Pediatr. Hematol. Oncol. 17 (2): 94–100. doi:. PMID 7749772.
- ↑ Hoffman et al. 2005, pg 1071
- ↑ Bennett JH (1845). «Two cases of hypertrophy of the spleen and liver, in which death took place from suppuration of blood». Edinburgh Med Surg J 64: 413.
- ↑ Virchow, R (1856). «Die Leukämie». Στο: Virchow R. Gesammelte Abhandlungen zur Wissenschaftlichen Medizin (στα German). Frankfurt: Meidinger. σελ. 190.
- ↑ Ebstein W (1889). «Über die acute Leukämie und Pseudoleukämie». Deutsch Arch Klin Med 44: 343.
- ↑ Mosler F (1876). «Klinische Symptome und Therapie der medullären Leukämie». Berl Klin Wochenschr 13: 702.
- ↑ Naegeli O (1900). «Über rothes Knochenmark und Myeloblasten». Deutsch Med Wochenschr 26 (18): 287. doi:.
- ↑ Zhen-yi, Wang (2003). «Ham-Wasserman Lecture: Treatment of Acute Leukemia by Inducing Differentiation and Apoptosis». Hematology 2003 (1): 1–13. doi:. PMID 14633774. Αρχειοθετήθηκε από το πρωτότυπο στις 2011-10-03. https://web.archive.org/web/20111003222949/http://asheducationbook.hematologylibrary.org/cgi/content/full/2003/1/1. Ανακτήθηκε στις 2011-11-28.
- ↑ Ley TJ, Mardis ER, Ding L, Fulton, Bob, McLellan, Michael D., Chen, Ken, Dooling, David, Dunford-Shore, Brian H. και άλλοι. (2008). «DNA sequencing of a cytogenetically normal acute myeloid leukaemia genome». Nature 456 (7218): 66–72. doi:. PMID 18987736. PMC 2603574. Bibcode: 2008Natur.456...66L. http://www.nature.com/nature/journal/v456/n7218/abs/nature07485.html.
- ↑ 83,0 83,1 Shapira T, Pereg D, Lishner M (Σεπτέμβριος 2008). «How I treat acute and chronic leukemia in pregnancy». Blood Rev. 22 (5): 247–59. doi:. PMID 18472198.