Ρεμντεσιβίρη
 | |
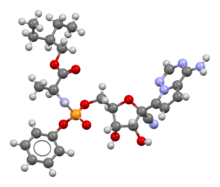 | |
| Ονομασία IUPAC | |
|---|---|
(2S)-2-{(2R,3S,4R,5R)-[5-(4-Aminopyrrolo[2,1-f] [1,2,4]triazin-7-yl)-5-cyano-3,4-dihydroxy-tetrahydro-furan-2-ylmethoxy]phenoxy-(S)-phosphorylamino}propionic acid 2-ethyl-butyl ester | |
| Κλινικά δεδομένα | |
| Εμπορικές ονομασίες | Veklury |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a620033 |
| Δεδομένα άδειας |
|
| Κατηγορία ασφαλείας κύησης | |
| Οδοί χορήγησης | Ενδοφλέβια |
| Κυκλοφορία | |
| Κυκλοφορία |
|
| Κωδικοί | |
| Αριθμός CAS | 1809249-37-3 |
| Κωδικός ATC | None |
| PubChem | CID 121304016 |
| DrugBank | DB14761 |
| ChemSpider | 58827832 |
| UNII | 3QKI37EEHE |
| KEGG | D11472 |
| ChEBI | CHEBI:145994 |
| ChEMBL | CHEMBL4065616 |
| Συνώνυμα | GS-5734 |
| Χημικά στοιχεία | |
| Χημικός τύπος | C27H35N6O8P |
| Μοριακή μάζα | 602,58 g·mol−1 |
CCC(COC(=O)[C@@H](NP(=O)(Oc1ccccc1)OC[C@H]1O[C@@]([C@@H]([C@@H]1O)O)(C#N)c1ccc2n1ncnc2N)C)CC | |
InChI=1S/C27H35N6O8P/c1-4-18(5-2)13-38-26(36)17(3)32-42(37,41-19-9-7-6-8-10-19)39-14-21-23(34)24(35)27(15-28,40-21)22-12-11-20-25(29)30-16-31-33(20)22/h6-12,16-18,21,23-24,34-35H,4-5,13-14H2,1-3H3,(H,32,37)(H2,29,30,31)/t17-,21+,23+,24+,27-,42-/m0/s1 Key:RWWYLEGWBNMMLJ-YSOARWBDSA-N | |
Η ρεμντεσιβίρη που πωλείται με την επωνυμία Veklury,[3] είναι ένα αντιικό φάρμακο ευρέως φάσματος που αναπτύχθηκε από τη βιοφαρμακευτική εταιρεία Gilead Sciences.[7] Χορηγείται με ένεση σε φλέβα.[8][9] Η ρεμντεσιβίρη δοκιμάζεται ως θεραπεία για τον κορωναϊό και έχει εγκριθεί για επείγουσα χρήση στις ΗΠΑ, την Ινδία,[10] Σιγκαπούρη,[11] και έχει εγκριθεί για χρήση στην Ιαπωνία, την Ευρωπαϊκή Ένωση και την Αυστραλία για άτομα με σοβαρά συμπτώματα του.[12][13] Έλαβε επίσης έγκριση στο Ηνωμένο Βασίλειο τον Μάιο του 2020 · ωστόσο με περιορισμένη προσφορά.[14] Μπορεί να μειώσει το χρόνο ανάρρωσης από τη μόλυνση.[15][16]
Η πιο συχνή παρενέργεια σε υγιείς εθελοντές είναι τα αυξημένα επίπεδα ηπατικών ενζύμων στο αίμα (ένα σημάδι ηπατικών προβλημάτων).[3] Οι πιο συχνές ανεπιθύμητες ενέργειες σε άτομα με COVID ‑ 19 είναι ναυτία.[3] Οι ανεπιθύμητες ενέργειες μπορεί να περιλαμβάνουν φλεγμονή του ήπατος και αντίδραση που σχετίζεται με την έγχυση με ναυτία, χαμηλή αρτηριακή πίεση και εφίδρωση.[17] Είναι ένα προφάρμακο που προορίζεται να επιτρέψει την ενδοκυτταρική απελευθέρωση μονοφωσφορικού GS-441524 και επακόλουθη βιομετατροπή σε τριφωσφορικό GS-441524, ένα ανάλογο ριβονουκλεοτιδίου που αναστέλλει την RNA πολυμεράση του ιού.[18]
Παλαιότερες μελέτες διαπίστωσαν αντιιική δράση έναντι αρκετών ιών RNA, συμπεριλαμβανομένου των κοροναϊών του SARS και MERS, αλλά δεν έχει εγκριθεί για κάποια ένδειξη.[7][12] Η ρεμντεσιβίρη αναπτύχθηκε αρχικά για τη θεραπεία της ηπατίτιδας C[19] και στη συνέχεια δοκιμάστηκε κατά της νόσου του ιού Έμπολα και της νόσου του ιού Μάρμπουργκ, αλλά ήταν αναποτελεσματική για όλες αυτές τις ιογενείς λοιμώξεις.[20]
Φαρμακολογία
[Επεξεργασία | επεξεργασία κώδικα]Δραστηριοποίηση
[Επεξεργασία | επεξεργασία κώδικα]
Η ρεμντεσιβίρη είναι ένα προτίδιο (Προφάρμακο ενός νουκλεοΤίδιου). Είναι ικανή να διαχέεται σε κύτταρα όπου μετατρέπεται σε μονοφωσφορικό GS-441524 μέσω της δράσης εστερασών (CES1 και CTSA) και μιας φωσφοαμιδάσης (HINT1). Αυτό με τη σειρά του φωσφορυλιώνεται περαιτέρω στον ενεργό του τριφωσφορικό μεταβολίτη από νουκλεοσιδικές-φωσφορικές κινάσες.[22][23] Αυτή η οδός βιοενεργοποίησης προορίζεται να συμβεί ενδοκυτταρικά, αλλά μια σημαντική ποσότητα ρεμντεσιβίρης υδρολύεται πρόωρα στο πλάσμα, με το GS-441524 να είναι ο κύριος μεταβολίτης στο πλάσμα και ο μόνος μεταβολίτης που απομένει δύο ώρες μετά τη χορήγηση.[18]
Μηχανισμός δράσης
[Επεξεργασία | επεξεργασία κώδικα]Ως ανάλογο νουκλεοτίδιο της τριφωσφορικής αδενοσίνης (GS-443 902),[24] ο ενεργός μεταβολίτης της ρεμντεσιβίρης παρεμβαίνει στη δράση της ιικού RNA-εξαρτώμενη RNA πολυμεράσης και αποφεύγει την μετατροπή από την ιική εξοριβονουκλεάση (εξόνιο), προκαλώντας μια μείωση στην παραγωγή ιικού RNA.[7][25] Σε ορισμένους ιούς, όπως ο αναπνευστικός συγκυτιακός ιός, προκαλεί την παύση των εξαρτώμενων από RNA πολυμεράσης RNA, αλλά το κυρίαρχο αποτέλεσμα του (όπως στον Ebola) είναι να προκαλέσει έναν μη αναστρέψιμο τερματισμό της αλυσίδας. Σε αντίθεση με πολλούς άλλους τερματιστές αλυσίδων, αυτό δεν μεσολαβείται αποτρέποντας την προσθήκη του αμέσως επόμενου νουκλεοτιδίου, αλλά αντ 'αυτού καθυστερεί, συμβαίνει αφού έχουν προστεθεί πέντε επιπλέον βάσεις στην αναπτυσσόμενη αλυσίδα RNA.[26] Για την εξαρτώμενη από RNA πολυμεράση RNA των MERS-CoV, SARS-CoV-1 και SARS-CoV-2 η διακοπή της σύνθεσης RNA συμβαίνει μετά την ενσωμάτωση τριών επιπλέον νουκλεοτιδίων.[27] Ως εκ τούτου, η ρεμντεσιβίρη ταξινομείται ως αντιιικός παράγοντας άμεσης δράσης που λειτουργεί ως καθυστερημένος τερματιστής της αλυσίδας.[21][23]
Φαρμακοκινητική
[Επεξεργασία | επεξεργασία κώδικα]Σε πρωτεύοντα πλην του ανθρώπου, ο χρόνος ημιζωής του προφαρμάκου στο πλάσμα είναι 20 λεπτά, με τον κύριο μεταβολίτη να είναι ο νουκλεοζίτης, GS-441524. Δύο ώρες μετά την ένεση, ο κύριος μεταβολίτης GS-441524 βρίσκεται σε συγκεντρώσεις μικρομορίων, ενώ η άθικτη ρεμντεσιβίρη δεν είναι πλέον ανιχνεύσιμη. Λόγω αυτής της ταχείας εξωκυτταρικής μετατροπής στη νουκλεοσίδη GS-441524, ορισμένοι ερευνητές αμφισβήτησαν εάν το δραστικό τριφωσφορικό νουκλεοτίδιο προέρχεται πραγματικά από την απομάκρυνση του φαρμάκου ρεμντεσιβίρη ή αν συμβαίνει με φωσφορυλίωση του GS-441524 και εάν η άμεση χορήγηση του GS-441524 θα αποτελούν φθηνότερο και ευκολότερο να χορηγηθεί φάρμακο COVID-19 σε σύγκριση με τη ρεμντεσιβίρη.[28][18] Η ενεργοποιημένη μορφή τριφωσφορικού νουκλεοτιδίου διατηρεί τα ενδοκυτταρικά επίπεδά της στα μονοπύρηνα κύτταρα στο περιφερικό αίμα και πιθανώς και σε άλλα κύτταρα.[21]
Αλληλεπιδράσεις
[Επεξεργασία | επεξεργασία κώδικα]Η ρεμντεσιβίρη μεταβολίζεται τουλάχιστον μερικώς από τα ένζυμα CyP2C8, CYP2D6 και CYP3A4 του κυτοχρώματος P450.[29][30] Οι συγκεντρώσεις ρεμντεσιβίρης στο πλάσμα του αίματος αναμένεται να μειωθούν εάν χορηγούνται μαζί με επαγωγείς του κυτοχρώματος P450 όπως ριφαμπικίνη, καρβαμαζεπίνη, φαινοβαρβιτάλη, φαινυτοΐνη, πριμιδόνη και βαλσαμόχορτο.[31]
Στις 15 Ιουνίου 2020, η FDA ενημέρωσε τα ενημερωτικά δελτία για την άδεια χρήσης επείγουσας ανάγκης ρεμντεσιβίρης για να προειδοποιήσει ότι η χρήση χλωροκίνης ή υδροξυχλωροκίνης με ρεμντεσιβίρη ενδέχεται να μειώσει την αντιική δράση της ρεμντεσιβίρης.[32] Δεν συνιστάται συγχορήγηση ρεμντεσιβίρης και φωσφορικής χλωροκίνης ή θειικής υδροξυχλωροκίνης με βάση δεδομένα in vitro που καταδεικνύουν ανταγωνιστική επίδραση της χλωροκίνης στην ενδοκυτταρική μεταβολική ενεργοποίηση και την αντιική δράση της ρεμντεσιβίρης.[30]
Έρευνα
[Επεξεργασία | επεξεργασία κώδικα]Η ρεμντεσιβίρη δημιουργήθηκε αρχικά από την Gilead Sciences το 2009, στο πλαίσιο του εταιρικού προγράμματος έρευνας και ανάπτυξης θεραπειών για την ηπατίτιδα C.[19] Δεν λειτούργησε κατά της ηπατίτιδας C όπως αναμενόταν, αλλά στη συνέχεια επαναχρησιμοποιήθηκε και μελετήθηκε ως πιθανή θεραπεία για τη νόσο του ιού Έμπολα και τις λοιμώξεις από τον ιό Μάρμπουργκ.[20] Σύμφωνα με το τσεχικό πρακτορείο ειδήσεων, αυτή η νέα γραμμή έρευνας πραγματοποιήθηκε υπό την καθοδήγηση του επιστήμονα Τομάς Τσιχλάρ.[33] Μια συνεργασία των ερευνητών από το Κέντρο Ελέγχου και Πρόληψης Νοσημάτων (CDC) και της Gilead Sciences ανακάλυψε ότι η ρεμντεσιβίρη είχε αντι-ιική δράση in vitro έναντι πολλαπλών φιλοϊών, πνευμονοϊοών, παραμυξοϊών και κοροναϊών.[34]
Η προκλινική και κλινική έρευνα και ανάπτυξη πραγματοποιήθηκε σε συνεργασία της Gilead Sciences και διαφόρων κυβερνητικών υπηρεσιών και ακαδημαϊκών ιδρυμάτων των ΗΠΑ.[35][36][37][38]
Στα μέσα της δεκαετίας του 2010, η δικηγορική εταιρεία Mintz Levin διέταξε διάφορες αιτήσεις διπλωμάτων ευρεσιτεχνίας για τη ρεμντεσιβίρη εκ μέρους της Gilead Sciences ενώπιον του Γραφείου Διπλωμάτων Ευρεσιτεχνίας και Εμπορικών Σημάτων των Ηνωμένων Πολιτειών (USPTO). Το USPTO χορήγησε δύο διπλώματα ευρεσιτεχνίας για τη ρεμντεσιβίρη στις Gilead Sciences στις 9 Απριλίου 2019: ένα για τους φιλοϊούς[39] και ένα που κάλυπτε τόσο τους αρεναϊούς όσο και τους κοροναϊούς.[40]
Έμπολα
[Επεξεργασία | επεξεργασία κώδικα]Τον Οκτώβριο του 2015, το Ινστιτούτο Μολυσματικών Νοσημάτων του Ιατρικού Ερευνητικού Στρατού των ΗΠΑ (USAMRIID) ανακοίνωσε προκλινικά αποτελέσματα ότι η ρεμντεσιβίρη είχε εμποδίσει τον ιό Έμπολα σε πιθήκους ρήσους. Ο Τράβις Γουόρεν, ο οποίος είναι κύριος ερευνητής του USAMRIID από το 2007, δήλωσε ότι «το έργο είναι αποτέλεσμα της συνεχιζόμενης συνεργασίας μεταξύ USAMRIID και Gilead Sciences».[41] Η «αρχική εξέταση» της «βιβλιοθήκης σύνθετων επιστημών της Gilead για την εύρεση μορίων με πολλά υποσχόμενη αντιική δράση» πραγματοποιήθηκε από επιστήμονες στο Κέντρο Ελέγχου και Πρόληψης Νοσημάτων (CDC). Ως αποτέλεσμα αυτής της εργασίας, προτείνεται η ρεμντεσιβίρη "να αναπτυχθεί περαιτέρω ως πιθανή θεραπεία."[20]
Η ρεμντεσιβίρη ωθήθηκε γρήγορα σε κλινικές δοκιμές λόγω της επιδημίας του ιού Έμπολα στη Δυτική Αφρική το 2013-2016, που τελικά χρησιμοποιήθηκε σε άτομα με την ασθένεια. Τα προκαταρκτικά αποτελέσματα ήταν πολλά υποσχόμενα. Χρησιμοποιήθηκε σε κατάσταση έκτακτης ανάγκης κατά τη διάρκεια της επιδημίας Έμπολα στο Κίβου που ξεκίνησε το 2018, μαζί με περαιτέρω κλινικές δοκιμές, μέχρι τον Αύγουστο του 2019, όταν αξιωματούχοι υγείας του Κονγκό ανακοίνωσαν ότι ήταν σημαντικά λιγότερο αποτελεσματικό από τις θεραπείες με μονοκλωνικά αντισώματα όπως το mAb114 και το REGN-EB3. Ωστόσο, οι δοκιμές καθιέρωσαν το προφίλ ασφάλειας.[42]
COVID-19
[Επεξεργασία | επεξεργασία κώδικα]Τον Ιανουάριο του 2020, η Gilead Sciences ξεκίνησε εργαστηριακές δοκιμές της ρεμντεσιβίρης έναντι του SARS-CoV-2, δηλώνοντας ότι η ρεμντεσιβίρης είχε αποδειχθεί ότι είναι δραστική κατά του σοβαρού οξέος αναπνευστικού συνδρόμου (SARS) και του αναπνευστικού συνδρόμου της Μέσης Ανατολής (MERS) σε ζωικά μοντέλα.[43][44][45] Στις 21 Ιανουαρίου 2020, το Ινστιτούτο ιολογίας του Γουχάν υπέβαλε αίτηση για κινεζικό «δίπλωμα ευρεσιτεχνίας» για τη θεραπεία του COVID ‑ 19.[46]
Σε μια δοκιμή στην Κίνα τον Φεβρουάριο-Μάρτιο του 2020, η ρεμντεσιβίρη δεν ήταν αποτελεσματική στη μείωση του χρόνου βελτίωσης από το COVID ‑ 19 ή των θανάτων και προκάλεσε διάφορες παρενέργειες, απαιτώντας από τους ερευνητές να τερματίσουν τη δοκιμή.[47]
Στις 18 Μαρτίου 2020, ο Παγκόσμιος Οργανισμός Υγείας (ΠΟΥ) ανακοίνωσε την έναρξη μιας δοκιμής που θα περιλάμβανε μια ομάδα που έλαβε θεραπεία με ρεμντεσιβίρη.[48][49] Άλλες κλινικές δοκιμές βρίσκονται σε εξέλιξη ή προγραμματίζονται.[50][51][52][53][54][55][56][57][58][59][60]
Όσον αφορά τον Απρίλιο του 2020, η ρεμντεσιβίρη θεωρούταν η πιο πολλά υποσχόμενη θεραπεία για τη COVID‑19,[15] και συμπεριλήφθηκε σε τέσσερις αγωγές υπό διευρεύνηση σε διεθνή[48][61] και ευρωπαϊκή μελέτη.[62] Ο FDA δήλωσε την 1η Μαΐου 2020 ότι ήταν λογικά να θεωρείται ότι τα γνωστά και ενδεχόμενα οφέλη της ρεμντεσιβίρης σε κάποιους συγκεκριμένους πληθυσμούς που νοσηλεύονται με σοβαρές επιπτώσεις της νόσου μπορεί να υπερνικούν τα μειονεκτήματα.[12]
Τον Αύγουστο του 2020, το NIAID ξεκίνησε τη δοκιμαστική θεραπεία φάσης 3 για COVID-19 (ACTT 3) για να αξιολογήσει την ασφάλεια και την αποτελεσματικότητα ενός θεραπευτικού σχήματος που αποτελείται από ρεμντεσιβίρη μαζί με ιντερφερόνη βήτα-1α για νοσηλευόμενους ενήλικες που έχουν επιβεβαιωθεί εργαστηριακά λοίμωξη από SARS-CoV- 2 με ενδείξεις εμπλοκής των πνευμόνων, συμπεριλαμβανομένης της ανάγκης για συμπληρωματικό οξυγόνο, παθολογικές ακτινογραφίες θώρακα ή ασθένεια που απαιτεί μηχανικό αερισμό.[63]
Μια μικρή δοκιμή ρεμντεσιβίρης σε πιθήκους μακάκους ρήσους με λοίμωξη COVID‑19 ανέφερε ότι η έγκαιρη θεραπεία με ρεμντεσιβίρη μείωσε τη βλάβη και την πρόοδο της νόσου, αλλά όχι την αποβολή ιών.[64]
Σύμφωνα με διεθνείς εμπειρογνώμονες από το British Medical Journal, «το φάρμακο πιθανότατα δεν έχει σημαντική επίδραση στην ανάγκη μηχανικού αερισμού και μπορεί να έχει μικρή ή καθόλου επίδραση στη διάρκεια της παραμονής στο νοσοκομείο». Λόγω της υψηλής τιμής, οι συγγραφείς επισημαίνουν ότι η ρεμντεσιβίρη μπορεί να εκτρέψει χρηματοδότηση και προσπάθειες από άλλες αποτελεσματικές θεραπείες κατά του COVID-19.[65]
Μια έρευνα που δημοσιεύθηκε το Νοέμβριο του 2020 στο NEJM βρήκε ότι η ρεμντεσιβίρη «ήταν ανώτερη από το εικονικό φάρμακο όσον αφορά τη μείωση του χρόνου ανάρρωσης σε ασθενείς που νοσηλεύονται και υπήρχαν στοιχεία μείωσης των λοιμώξεων κατώτερου αναπνευστικού».[16]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ «Veklury Australian prescription medicine decision summary». Therapeutic Goods Administration (TGA). 13 Ιουλίου 2020. Αρχειοθετήθηκε από το πρωτότυπο στις 13 Αυγούστου 2020. Ανακτήθηκε στις 16 Αυγούστου 2020.
- ↑ «Summary for ARTG Entry:338419 Veklury remdesivir 100 mg powder for injection vial». Therapeutic Goods Administration (TGA). Ανακτήθηκε στις 16 Αυγούστου 2020.[νεκρός σύνδεσμος]
- ↑ 3,0 3,1 3,2 3,3 «Veklury EPAR». European Medicines Agency (EMA). 23 Ιουνίου 2020. Ανακτήθηκε στις 6 Ιουλίου 2020. Text was copied from this source which is © European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- ↑ «Veklury 100 mg concentrate for solution for infusion - Summary of Product Characteristics (SmPC)». (emc). 6 Ιουλίου 2020. Αρχειοθετήθηκε από το πρωτότυπο στις 24 Νοεμβρίου 2020. Ανακτήθηκε στις 4 Οκτωβρίου 2020.
- ↑ «Veklury 100 mg powder for concentrate for solution for infusion - Summary of Product Characteristics (SmPC)». (emc). Ανακτήθηκε στις 4 Οκτωβρίου 2020.
- ↑ «Remdesivir injection Remdesivir injection, powder, lyophilized, for solution». DailyMed. 1 Σεπτεμβρίου 2020. Ανακτήθηκε στις 25 Σεπτεμβρίου 2020.
- ↑ 7,0 7,1 7,2 «Current pharmacological treatments for COVID-19: What's next?». British Journal of Pharmacology. April 2020. doi:. PMID 32329520.
- ↑ «Remdesivir». Drugs.com. 20 Απριλίου 2020. Ανακτήθηκε στις 30 Απριλίου 2020.
- ↑ «Pharmacotherapy in COVID-19; A narrative review for emergency providers». The American Journal of Emergency Medicine 38 (7): 1488–1493. July 2020. doi:. PMID 32336586.
- ↑ «India approves emergency use of remdesivir to treat Covid-19 patients». The Times of India. Reuters (Gurgaon, Haryana, India: Times Internet). 2 June 2020. https://timesofindia.indiatimes.com/india/india-approves-emergency-use-of-remdesivir-to-treat-covid-19-patients/articleshow/76152949.cms. Ανακτήθηκε στις 2 June 2020.
- ↑ «Singapore approves remdesivir drug for emergency COVID-19 treatment». Reuters. 10 Ιουνίου 2020. Ανακτήθηκε στις 10 Ιουνίου 2020.
- ↑ 12,0 12,1 12,2 «Remdesivir EUA Letter of Authorization» (PDF). U.S. Food and Drug Administration (FDA). 1 Μαΐου 2020. Ανακτήθηκε στις 1 Μαΐου 2020.
 Αυτό το λήμμα περιλαμβάνει κείμενο από αυτή την πηγή, που είναι κοινό κτήμα.
Αυτό το λήμμα περιλαμβάνει κείμενο από αυτή την πηγή, που είναι κοινό κτήμα.
- ↑ «Japan approves remdesivir for COVID-19 despite uncertainties». The Asahi Shimbun. 8 Μαΐου 2020. Αρχειοθετήθηκε από το πρωτότυπο στις 25 Μαΐου 2020. Ανακτήθηκε στις 9 Μαΐου 2020.
- ↑ Roberts, Michelle (26 May 2020). «Anti-viral drug that speeds recovery offered by NHS». BBC News Online. https://www.bbc.com/news/health-52805828. Ανακτήθηκε στις 26 May 2020.
- ↑ 15,0 15,1 «Coronavirus COVID-19 (SARS-CoV-2)». Johns Hopkins ABX Guide. Ανακτήθηκε στις 12 Απριλίου 2020.
Remdesivir: Likely the most promising drug.
- ↑ 16,0 16,1 Beigel, John H.; Tomashek, Kay M.; Dodd, Lori E.; Mehta, Aneesh K.; Zingman, Barry S.; Kalil, Andre C.; Hohmann, Elizabeth; Chu, Helen Y. και άλλοι. (2020-05-22). «Remdesivir for the Treatment of Covid-19 — Final Report» (στα αγγλικά). New England Journal of Medicine. doi:. PMID 32445440. PMC PMC7262788. https://www.nejm.org/doi/10.1056/NEJMoa2007764.
- ↑ «Fact Sheet for Patients And Parent/Caregivers Emergency Use Authorization (EUA) Of Remdesivir For Coronavirus Disease 2019 (COVID-19)» (PDF). U.S. Food and Drug Administration (FDA). Ανακτήθηκε στις 8 Μαΐου 2020.
- ↑ 18,0 18,1 18,2 Yan, Victoria C.· Muller, Florian L. (14 Μαΐου 2020). «Gilead should ditch remdesivir and focus on its simpler and safer ancestor». Stat. Boston Globe Media Partners.
- ↑ 19,0 19,1 Stephens, Bret (18 April 2020). «The Story of Remdesivir». The New York Times: σελ. A23. https://www.nytimes.com/2020/04/17/opinion/remdesivir-coronavirus.html. Ανακτήθηκε στις 11 May 2020.
- ↑ 20,0 20,1 20,2 «Therapeutic efficacy of the small molecule GS-5734 against Ebola virus in rhesus monkeys». Nature 531 (7594): 381–5. March 2016. doi:. PMID 26934220. Bibcode: 2016Natur.531..381W.
- ↑ 21,0 21,1 21,2 «Remdesivir: A Review of Its Discovery and Development Leading to Emergency Use Authorization for Treatment of COVID-19». ACS Central Science 6 (5): 672–683. May 2020. doi:. PMID 32483554.
- ↑ «Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses». Science Translational Medicine 9 (396): eaal3653. June 2017. doi:. PMID 28659436.
- ↑ 23,0 23,1 «Remdesivir is a direct-acting antiviral that inhibits RNA-dependent RNA polymerase from severe acute respiratory syndrome coronavirus 2 with high potency». The Journal of Biological Chemistry 295 (20): 6785–6797. May 2020. doi:. PMID 32284326.
- ↑ «Synthesis and antiviral activity of a series of 1'-substituted 4-aza-7,9-dideazaadenosine C-nucleosides». Bioorganic & Medicinal Chemistry Letters 22 (8): 2705–7. April 2012. doi:. PMID 22446091.
- ↑ «Remdesivir in covid-19». BMJ 369: m1610. April 2020. doi:. PMID 32321732. https://www.bmj.com/content/369/bmj.m1610.long.
- ↑ «Mechanism of Inhibition of Ebola Virus RNA-Dependent RNA Polymerase by Remdesivir». Viruses 11 (4): 326. April 2019. doi:. PMID 30987343.
- ↑ «The antiviral compound remdesivir potently inhibits RNA-dependent RNA polymerase from Middle East respiratory syndrome coronavirus». The Journal of Biological Chemistry 295 (15): 4773–4779. April 2020. doi:. PMID 32094225.
- ↑ Yan, Victoria C.; Muller, Florian L. (July 2020). «Advantages of the parent nucleoside GS-441524 over remdesivir for Covid-19 treatment». ACS Medicinal Chemistry Letters 11 (7): 1361–1366. doi:. PMID 32665809.
- ↑ «Summary on Compassionate Use: Remdesivir Gilead» (PDF). European Medicines Agency (EMA). 3 Απριλίου 2020. Ανακτήθηκε στις 1 Μαΐου 2020.
- ↑ 30,0 30,1 «Fact Sheet For Health Care Providers Emergency Use Authorization (EUA) Of Remdesivir (GS-5734TM)» (PDF). U.S. Food and Drug Administration (FDA). 15 Ιουνίου 2020. Ανακτήθηκε στις 15 Ιουνίου 2020.
 Αυτό το λήμμα περιλαμβάνει κείμενο από αυτή την πηγή, που είναι κοινό κτήμα.
Αυτό το λήμμα περιλαμβάνει κείμενο από αυτή την πηγή, που είναι κοινό κτήμα.
- ↑ «COVID-19 interactions». University of Liverpool. Ανακτήθηκε στις 28 Απριλίου 2020.
- ↑ (15 June 2020). Coronavirus (COVID-19) Update: FDA Warns of Newly Discovered Potential Drug Interaction That May Reduce Effectiveness of a COVID-19 Treatment Authorized for Emergency Use. Δελτίο τύπου.
 Αυτό το λήμμα περιλαμβάνει κείμενο από αυτή την πηγή, που είναι κοινό κτήμα.
Αυτό το λήμμα περιλαμβάνει κείμενο από αυτή την πηγή, που είναι κοινό κτήμα.
- ↑ Czech News Agency, "Did Czech scientists create the cure for coronavirus?", Aktuálně.cz, 5 February 2020.
- ↑ «GS-5734 and its parent nucleoside analog inhibit Filo-, Pneumo-, and Paramyxoviruses». Scientific Reports 7: 43395. March 2017. doi:. PMID 28262699. Bibcode: 2017NatSR...743395L.
- ↑ «Remdesivir: A Review of Its Discovery and Development Leading to Emergency Use Authorization for Treatment of COVID-19». ACS Central Science 6 (5): 672–683. May 2020. doi:. PMID 32483554.
- ↑ Silverman, Ed (8 Μαΐου 2020). «U.S. government contributed research to a Gilead remdesivir patent – but didn't get credit». Stat. Ανακτήθηκε στις 28 Μαΐου 2020.
- ↑ Ardizzone, Kathryn (20 March 2020). «Role of the Federal Government in the Development of Remdesivir». Knowledge Ecology International. https://www.keionline.org/wp-content/uploads/KEI-Briefing-Note-2020_1GS-5734-Remdesivir.pdf. Ανακτήθηκε στις 28 May 2020.
- ↑ «Investigational compound remdesivir, developed by UAB and NIH researchers, being used for treatment of novel coronavirus». UAB News. Ανακτήθηκε στις 28 Μαΐου 2020.
- ↑ [1], "Methods for treating Filoviridae virus infections"
- ↑ [2], "Methods for treating arenaviridae and coronaviridae virus infections"
- ↑ Antiviral Compound Provides Full Protection from Ebola Virus in Nonhuman Primates (Report). 9 October 2015.
- ↑ «Remdesivir for severe acute respiratory syndrome coronavirus 2 causing COVID-19: An evaluation of the evidence». Travel Medicine and Infectious Disease 35: 101647. April 2020. doi:. PMID 32247927.
- ↑ «Prophylactic and therapeutic remdesivir (GS-5734) treatment in the rhesus macaque model of MERS-CoV infection». Proceedings of the National Academy of Sciences of the United States of America 117 (12): 6771–6776. March 2020. doi:. PMID 32054787.
- ↑ «Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses». Science Translational Medicine 9 (396): eaal3653. June 2017. doi:. PMID 28659436.
- ↑ Joseph, Saumya Sibi; Samuel, Maju (31 January 2020). «Gilead working with China to test Ebola drug as new coronavirus treatment». Reuters. Αρχειοθετήθηκε από το πρωτότυπο στις 31 January 2020. https://web.archive.org/web/20200131201118/https://www.reuters.com/article/us-health-china-gilead-sciences/gilead-working-with-china-to-test-ebola-drug-as-new-coronavirus-treatment-idUSKBN1ZU2RX. Ανακτήθηκε στις 31 January 2020.
- ↑ Barmann, Jay (6 February 2020). «Bay Area-Based Gilead Sees Potential Legal Conflict With China Over Its Coronavirus Drug». SFist. Impress Media. Αρχειοθετήθηκε από το πρωτότυπο στις 26 March 2020. https://web.archive.org/web/20200326060714/https://sfist.com/2020/02/06/bay-area-based-gilead-donates-experimental-anti-viral-drug-to-china/. Ανακτήθηκε στις 22 March 2020.
- ↑ «Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial». Lancet 395 (10236): 1569–1578. May 2020. doi:. PMID 32423584.
- ↑ 48,0 48,1 «"Solidarity" clinical trial for COVID-19 treatments». World Health Organization (WHO). 3 Μαρτίου 2020. Ανακτήθηκε στις 19 Απριλίου 2020.
- ↑ «UN health chief announces global 'solidarity trial' to jumpstart search for COVID-19 treatment». UN News. 18 Μαρτίου 2020.
- ↑ «Remdesivir Clinical Trials». Gilead Sciences. Ανακτήθηκε στις 20 Απριλίου 2020.
- ↑ «7 Studies found for: Remdesivir & Recruiting, Not yet recruiting, Active, not recruiting, Completed, Enrolling by invitation Studies & COVID-19». ClinicalTrials.gov. U.S. National Library of Medicine. Ανακτήθηκε στις 16 Απριλίου 2020.
- ↑ «A Trial of Remdesivir in Adults With Severe COVID-19». ClinicalTrials.gov. 6 Φεβρουαρίου 2020. Ανακτήθηκε στις 19 Απριλίου 2020.
- ↑ «A Trial of Remdesivir in Adults With Mild and Moderate COVID-19». ClinicalTrials.gov. 5 Φεβρουαρίου 2020. Ανακτήθηκε στις 19 Απριλίου 2020.
- ↑ «Study to Evaluate the Safety and Antiviral Activity of Remdesivir (GS-5734) in Participants With Moderate Coronavirus Disease (COVID-19) Compared to Standard of Care Treatment». ClinicalTrials.gov. 3 Μαρτίου 2020. Ανακτήθηκε στις 19 Απριλίου 2020.
- ↑ «Study to Evaluate the Safety and Antiviral Activity of Remdesivir (GS-5734) in Participants With Severe Coronavirus Disease (COVID-19)». ClinicalTrials.gov. 3 Μαρτίου 2020. Ανακτήθηκε στις 19 Απριλίου 2020.
- ↑ «Trial of Treatments for COVID-19 in Hospitalized Adults (DisCoVeRy)». ClinicalTrials.gov. 20 Μαρτίου 2020. Ανακτήθηκε στις 19 Απριλίου 2020.
- ↑ «Expanded Access Remdesivir (RDV; GS-5734)». ClinicalTrials.gov. 10 Μαρτίου 2020. Ανακτήθηκε στις 19 Απριλίου 2020.
- ↑ «Expanded Access Treatment Protocol: Remdesivir (RDV; GS-5734) for the Treatment of SARS-CoV2 (CoV) Infection (COVID-19)». ClinicalTrials.gov. 27 Μαρτίου 2020. Ανακτήθηκε στις 19 Απριλίου 2020.
- ↑ «Multi-centre, adaptive, randomized trial of the safety and efficacy of treatments of COVID-19 in hospitalized adults (DisCoVeRy)». European Union Clinical Trials Register. Ανακτήθηκε στις 19 Απριλίου 2020.
- ↑ «Adaptive COVID-19 Treatment Trial (ACTT)». ClinicalTrials.gov. 21 Φεβρουαρίου 2020. Ανακτήθηκε στις 11 Μαΐου 2020.
- ↑ Kupferschmidt, Kai; Cohen, Jon (22 March 2020). «WHO launches global megatrial of the four most promising coronavirus treatments». Science. doi:.
- ↑ «Launch of a European clinical trial against COVID-19». INSERM. 22 Μαρτίου 2020. Ανακτήθηκε στις 1 Μαΐου 2020.
- ↑ «Adaptive COVID-19 Treatment Trial 3 (ACTT-3)». ClinicalTrials.gov. 30 Ιουλίου 2020. Ανακτήθηκε στις 5 Αυγούστου 2020.
- ↑ «Clinical benefit of remdesivir in rhesus macaques infected with SARS-CoV-2». Nature 585 (7824): 273–276. June 2020. doi:. PMID 32516797.
- ↑ Wilson J. (July 30, 2020). "Remdesivir Gets Lukewarm Endorsement From Experts in Covid Fight". Bloomberg. Retrieved 31 July 2020.