Φινερενόνη
 | |
| Ονομασία IUPAC | |
|---|---|
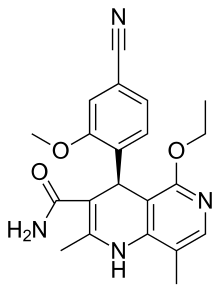
(4S)-4-(4-Cyano-2-methoxyphenyl)-5-ethoxy-2,8-dimethyl-1,4-dihydro-1,6-naphthyridine-3-carboxamide | |
| Κλινικά δεδομένα | |
| Εμπορικές ονομασίες | Kerendia |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a621038 |
| Δεδομένα άδειας |
|
| Κατηγορία ασφαλείας κύησης | |
| Οδοί χορήγησης | Από το στόμα |
| Κυκλοφορία | |
| Κυκλοφορία | |
| Φαρμακοκινητική | |
| Μεταβολισμός | κυρίως CYP3A4 |
| Βιολογικός χρόνος ημιζωής | 2-3 ώρες[8] |
| Απέκκριση | 80% ούρα, 20% κόπρανα[8] |
| Κωδικοί | |
| Αριθμός CAS | 1050477-31-0 |
| Κωδικός ATC | C03DA05 |
| PubChem | CID 60150535 |
| DrugBank | DB16165 |
| ChemSpider | 28669387 |
| UNII | DE2O63YV8R |
| KEGG | D10633 |
| ChEMBL | CHEMBL2181927 |
| Συνώνυμα | BAY 94-8862 |
| Χημικά στοιχεία | |
| Χημικός τύπος | C21H22N4O3 |
| Μοριακή μάζα | 378,43 g·mol−1 |
NC(=O)C1=C(C)Nc2c(C)cnc(OCC)c2[C@@H]1c3ccc(C#N)cc3OC | |
InChI=1S/C21H22N4O3/c1-5-28-21-18-17(14-7-6-13(9-22)8-15(14)27-4)16(20(23)26)12(3)25-19(18)11(2)10-24-21/h6-8,10,17,25H,5H2,1-4H3,(H2,23,26)/t17-/m1/s1 Key:BTBHLEZXCOBLCY-QGZVFWFLSA-N | |
Η φινερενόνη, που διατίθεται στην αγορά με την εμπορική ονομασία Kerendia μεταξύ άλλων, είναι φάρμακο που χρησιμοποιείται για τη μείωση του κινδύνου έκπτωσης της νεφρικής λειτουργίας, νεφρικής ανεπάρκειας, καρδιαγγειακού θανάτου, μη θανατηφόρων εμφραγμάτων και νοσηλείας για καρδιακή ανεπάρκεια σε ενήλικες με χρόνια νεφρική ανεπάρκεια που σχετίζεται με σακχαρώδη διαβήτη τύπου 2.[9] Η φινερενόνη είναι ένας μη στεροειδής ανταγωνιστής των υποδοχέων των μεταλλοκορτικοειδών (MRA).[8] Λαμβάνεται από το στόμα.
Συχνές ανεπιθύμητες ενέργειες περιλαμβάνουν υπερκαλιαιμία (υψηλά επίπεδα καλίου στο αίμα), υπόταση (χαμηλή αρτηριακή πίεση) και υπονατριαιμία (χαμηλά επίπεδα νατρίου).[9]
Η φινερενόνη εγκρίθηκε για ιατρική χρήση στις Ηνωμένες Πολιτείες τον Ιούλιο του 2021,[9] και στην Ευρωπαϊκή Ένωση τον Φεβρουάριο του 2022. Ο Οργανισμός Τροφίμων και Φαρμάκων των ΗΠΑ θεωρεί ότι είναι φάρμακο πρώτο στην κατηγορία του.[10]
Ιατρικές χρήσεις
[Επεξεργασία | επεξεργασία κώδικα]Στις Ηνωμένες Πολιτείες, η φινερενόνη ενδείκνυται για τη μείωση του κινδύνου μείωσης της νεφρικής λειτουργίας, νεφρικής ανεπάρκειας, καρδιαγγειακού θανάτου, μη θανατηφόρων καρδιακών προσβολών και νοσηλείας για καρδιακή ανεπάρκεια σε ενήλικες με χρόνια νεφρική νόσο που σχετίζεται με τον τύπο 2 διαβήτης.[9] Στην Ευρωπαϊκή Ένωση, η φινερενόνη ενδείκνυται για τη θεραπεία της χρόνιας νεφρικής νόσου (στάδιο 3 και 4 με λευκωματουρία) που σχετίζεται με σακχαρώδη διαβήτη τύπου 2 σε ενήλικες.[7]
Η αποτελεσματικότητα της φινερενόνης στη βελτίωση της έκβασης των νεφρών και της καρδιάς αξιολογήθηκε σε μια τυχαιοποιημένη, πολυκεντρική, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο μελέτη σε ενήλικες με χρόνια νεφρική νόσο που σχετίζεται με τον τύπο 2 διαβήτης.[9] Σε αυτή τη μελέτη, 5.674 συμμετέχοντες ανατέθηκαν τυχαία για να λάβουν είτε φινερενόνη είτε εικονικό φάρμακο.[9]
Η μελέτη συνέκρινε τις δύο ομάδες για τον αριθμό των συμμετεχόντων των οποίων η νόσος εξελίχθηκε σε σύνθετο (ή συνδυασμένο) τελικό σημείο που περιελάμβανε τουλάχιστον 40% μείωση της νεφρικής λειτουργίας, εξέλιξη σε νεφρική ανεπάρκεια ή νεφρικό θάνατο.[9] Τα αποτελέσματα έδειξαν ότι 504 από τους 2.833 συμμετέχοντες που έλαβαν φινερενόνη είχαν τουλάχιστον ένα από τα συμβάντα στο σύνθετο τελικό σημείο σε σύγκριση με 600 από τους 2.841 συμμετέχοντες που έλαβαν εικονικό φάρμακο.[9]
Μια μετα-ανάλυση δεδομένων από επτά τυχαιοποιημένες ελεγχόμενες δοκιμές (13.783 συμμετέχοντες) βρήκε όφελος από τη χρήση της φινερενόνης σε άτομα με διαβητική νεφρική νόσο και εξεσημασμένη πρωτεϊνουρία.[11]
Παρενέργειες
[Επεξεργασία | επεξεργασία κώδικα]Η φινερενόνη μπορεί να προκαλέσει ηλεκτρολυτικές ανισορροπίες.[12] Τα συμπτώματα που σχετίζονται με υψηλότερα επίπεδα καλίου περιλαμβάνουν ναυτία, αδυναμία, πόνο στο στήθος και απώλεια κίνησης.[12] Τα άτομα με χαμηλότερα επίπεδα νατρίου μπορεί να εμφανίσουν πονοκεφάλους, σύγχυση, αδυναμία και αίσθημα ισορροπίας.[12] Καθώς η φινερενόνη μεταβολίζεται από το κυτόχρωμα CYP3A4, αναστολείς του, όπως ο χυμός γκρέιπφρουτ μπορεί να αυξήσουν τις συγκεντρώσεις της στο αίμα και έτσι να επιδεινώσουν τις παρενέργειες.[8]
Φαρμακολογία
[Επεξεργασία | επεξεργασία κώδικα]Η φινερενόνη απορροφάται εξ ολοκλήρου όταν λαμβάνεται από το στόμα, όπως επειδή μεταβολίζεται μόνο το 44% καταλήγει να είναι βιοδιαθέσιμη. Η μέγιστη συγκέντρωση στο αίμα παρατηρείται μισή με μία ώρα και ένα τέταρτο μετά τη λήψη. Σταθερή συγκέντρωση στο αίμα επιτυγχάνεται μετά από δύο ημέρες λήψης.[8] Η φινερενόνη μεταβολίζεται κυρίως από το κυτόχρωμα CYP3A4 και σε μικρότερο βαθμό από το CYP2C8 σε ανενεργούς μεταβολίτες. Αποβάλλεται κυρίως από τα ούρα (80%) και η υπόλοιπη από τα κόπρανα.[8]
Η φινερενόνη είναι ένας μη στεροειδικός ανταγωνιστής των υποδοχέων των αλατικορτικοειδών (MRA), όπως η αλδοστερόνη. Εμποδίζει την επαναρρόφηση νατρίου στους νεφρούς από τους μεταφορείς αλατικοκορτικοειδών και εμποδίζει την υπερενεργοποίησή τους στην καρδιά και στα αγγεία η οποία θεωρείται οδηγεί σε φλεγμονή και ίνωση.[8] Η φινερενόνη έχει μικρότερη σχετική συγγένεια με άλλους υποδοχείς στεροειδών ορμονών από τους ανταγωνιστές της αλδοστερόνης που είναι διαθέσιμοι επί του παρόντος, όπως η επλερενόνη και η σπιρονολακτόνη, κάτι που θα πρέπει να έχει ως αποτέλεσμα λιγότερες ανεπιθύμητες ενέργειες όπως γυναικομαστία, στυτική δυσλειτουργία και χαμηλή λίμπιντο.[13][14]
Η φινερενόνη δρα ως ανταγωνιστής σε υποδοχείς αλατικορτικοειδών με τη μετάλλαξη S810L, σε αντίθεση με άλλους παραδοσιακούς αναστολείς όπως η σπιρονολακτόνη και η επλερενόνη που παρεμπιπτόντως δρουν ως αγωνιστές.[15]
Ιστορία
[Επεξεργασία | επεξεργασία κώδικα]Τον Δεκέμβριο του 2021, η Επιτροπή Φαρμάκων για Ανθρώπινη Χρήση του Ευρωπαϊκού Οργανισμού Φαρμάκων εξέδωσε θετική γνώμη, προτείνοντας τη χορήγηση άδειας κυκλοφορίας για το φαρμακευτικό προϊόν Kerendia, που προορίζεται για τη θεραπεία χρόνιας νεφρικής νόσου που σχετίζεται με τον τύπο 2 Διαβήτης σε ενήλικες.[16] Ο αιτών για αυτό το φαρμακευτικό προϊόν είναι η Bayer AG. [16] Η φινερενόνη εγκρίθηκε για ιατρική χρήση στην Ευρωπαϊκή Ένωση τον Φεβρουάριο του 2022. [17]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ «Updates to the Prescribing Medicines in Pregnancy database». Therapeutic Goods Administration (TGA). 12 Μαΐου 2022. Ανακτήθηκε στις 13 Μαΐου 2022.
- ↑ 2,0 2,1 «Kerendia APMDS». Therapeutic Goods Administration (TGA). 9 Δεκεμβρίου 2021. Ανακτήθηκε στις 12 Ιουνίου 2022.
- ↑ «AusPAR: Finerenone». Therapeutic Goods Administration (TGA). 31 Μαΐου 2022. Ανακτήθηκε στις 12 Ιουνίου 2022.[νεκρός σύνδεσμος]
- ↑ «Kerendia Product information». Health Canada. 25 Απριλίου 2012. Ανακτήθηκε στις 2 Ιανουαρίου 2023.
- ↑ «Kerendia Summary Basis of Decision». Health Canada. 23 Οκτωβρίου 2014. Ανακτήθηκε στις 10 Μαρτίου 2023.[νεκρός σύνδεσμος]
- ↑ «Details for: Kerendia». Health Canada. 22 Νοεμβρίου 2022. Ανακτήθηκε στις 3 Μαρτίου 2024.
- ↑ 7,0 7,1 «Kerendia EPAR». European Medicines Agency (EMA). 14 Δεκεμβρίου 2021. Ανακτήθηκε στις 11 Μαρτίου 2022. Text was copied from this source which is copyright European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- ↑ 8,0 8,1 8,2 8,3 8,4 8,5 8,6 8,7 «Kerendia- finerenone tablet, film coated». DailyMed. Ανακτήθηκε στις 20 Αυγούστου 2021.
- ↑ 9,0 9,1 9,2 9,3 9,4 9,5 9,6 9,7 9,8 «FDA Approves Drug for Chronic Kidney Disease». U.S. Food and Drug Administration (FDA). 9 Ιουλίου 2021. Ανακτήθηκε στις 9 Ιουλίου 2021.
- ↑ (PDF) Advancing Health Through Innovation: New Drug Therapy Approvals 2021 (Report). 13 May 2022. https://www.fda.gov/media/155227/download. Ανακτήθηκε στις 22 January 2023.
 Αυτό το λήμμα περιλαμβάνει κείμενο από αυτή την πηγή, που είναι κοινό κτήμα.
Αυτό το λήμμα περιλαμβάνει κείμενο από αυτή την πηγή, που είναι κοινό κτήμα.
- ↑ «Efficacy and Safety of Novel Non-steroidal Mineralocorticoid Receptor Antagonist Finerenone in the Management of Diabetic Kidney Disease: A Meta-analysis.». Indian J Endocrinol Metab 26 (3): 198–205. May–Jun 2022. doi:. PMID 36248038.
- ↑ 12,0 12,1 12,2 «Finerenone Uses, Side Effects & Warnings». Drugs.com. Ανακτήθηκε στις 11 Ιουνίου 2022.
- ↑ «Renin-angiotensin system blockade: Finerenone». Nephrologie & Therapeutique 13 (Suppl 1): S47–S53. April 2017. doi:. PMID 28577743.
- ↑ «Rationale and design of MinerAlocorticoid Receptor antagonist Tolerability Study-Heart Failure (ARTS-HF): a randomized study of finerenone vs. eplerenone in patients who have worsening chronic heart failure with diabetes and/or chronic kidney disease». European Journal of Heart Failure 17 (2): 224–32. February 2015. doi:. PMID 25678098. https://deepblue.lib.umich.edu/bitstream/2027.42/110733/1/ejhf218.pdf.
- ↑ «Finerenone Impedes Aldosterone-dependent Nuclear Import of the Mineralocorticoid Receptor and Prevents Genomic Recruitment of Steroid Receptor Coactivator-1». The Journal of Biological Chemistry 290 (36): 21876–89. September 2015. doi:. PMID 26203193.
- ↑ 16,0 16,1 «Kerendia: Pending EC decision». European Medicines Agency (EMA). 16 Δεκεμβρίου 2021. Αρχειοθετήθηκε από το πρωτότυπο στις 28 Οκτωβρίου 2022. Ανακτήθηκε στις 18 Δεκεμβρίου 2021.
- ↑ «Kerendia Product information». Union Register of medicinal products. Ανακτήθηκε στις 3 Μαρτίου 2023.