Natria poloniido
| Natria poloniido | |||

| |||
| Kemia strukturo de la Natria poloniido | |||

| |||
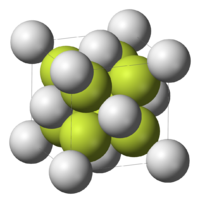
| 3D Kemia strukturo de la Natria poloniido | |||
| |||
| Kristala strukturo de natria poloniido | |||
| Alternativa(j) nomo(j) | |||
| Natria salo de poloniida acido | |||
| Kemia formulo | |||
| Fizikaj proprecoj | |||
| Aspekto | Grizkolora solido | ||
| Molmaso | 254.96 g mol−1 | ||
| Denseco | 4,08 g/cm3 | ||
| Sekurecaj Indikoj | |||
| Risko | R34 R50 | ||
| Sekureco | (S1/2) S26 S37 S45 S61 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H311, H315, H331 | ||
| GHS Deklaroj pri antaŭgardoj | P101, P102, P103, P262, P353, P302+352, P306+360 | ||
(25 °C kaj 100 kPa) | |||
Natria poloniido, poloniido de natrio aŭ Na2Po estas neorganika kombinaĵo de natrio kaj polonio, grizkolora kaj tre stabila el la poloniaj kombinaĵoj. Pro la alta elektronegativeco inter la atomoj de natrio kaj polonio, laŭ la sistemo de Linus Pauling, kaj la milda nemetala karaktero de polonio, ĝia strukturo kuŝas inter intermetalaj fazoj kaj jonaj komponaĵoj.
Sintezo
[redakti | redakti fonton]- Natria poloniido prepareblas per traktado de elementa natrio kaj polonia hidrido kun liberigo de hidrogeno. Ĉi-metodo estas iom malfacila pro la kemia malstabileco de la polona hidrido:
- Aŭ rekte ekde la fandado de polonia metalo kaj natrio:
- aŭ per traktado de la polonio kaj kaŭstika sodo:
Proprecoj
[redakti | redakti fonton]Poloniidoj estas toksaj komponaĵoj[1] kaj ĝenerale produktiĝas ekde senpera reakcio inter la elementoj sub temperaturoj inter 300 °C kaj 400 °C. Ili estas la plej kemie stabilaj kombinaĵoj de polonio kaj povas dividiĝi inter du grandaj grupoj:
- la jonaj poloniidoj, kiuj laŭŝajne enhavas la anjonon Po2+
- la intermetalaj poloniidoj, kiu prezentas pli kompleksajn ligilojn
Kelkaj poloniidoj estas peraĵoj inter ĉi-du kazoj kaj aliaj estas nestekiometriaj kombinaĵoj. Alojoj enhavantaj polonion ankaŭ nomatas poloniidoj. Ĉar polonio kuŝas rekte malsupra ol teluro en la perioda tabelo, poloniidoj kaj teluridoj prezentas plurajn kemiajn kaj strukturajn similaĵojn.[2]
Literaturo
[redakti | redakti fonton]- IOPScience
- Snipview[rompita ligilo]
- Inorganic Hydrides: The Commonwealth and International Library: Chemistry ..., B. L. Shaw
- Inorganic Chemistry, Mark Weller, Tina Overton, Jonathan Rourke, Fraser Armstrong
- The Radiochemistry of Polonium, Edição 3037, P. E. Figgins
- Advances in Inorganic Chemistry and Radiochemistry, Volume 4
| ||||||







