Budesónida
| Budesónida | ||
|---|---|---|
 | ||
 | ||
| Nombre (IUPAC) sistemático | ||
| 16,17-(butilidenebis(oxi))-11,21-dihidroxi-, (11-β,16-α)-pregna-1,4-dieno-3,20-diona | ||
| Identificadores | ||
| Número CAS | 51333-22-3 | |
| Código ATC | A07EA06 | |
| PubChem | 40000 | |
| DrugBank | DB01222 | |
| Datos químicos | ||
| Fórmula | C25H34O6 | |
| Peso mol. | 430,534 g/mol | |
|
O=C(CO)[C@]25O[C@@H](O[C@@H]5C[C@H]1[C@H]4[C@H]([C@@H](O)C[C@@]12C)[C@]/3(/C=C\C(=O)\C=C\3CC4)C)CCC
| ||
| Farmacocinética | ||
| Biodisponibilidad | 100% | |
| Unión proteica | 85-90% | |
| Metabolismo | Hígado. | |
| Vida media | 2.0-3.6 | |
| Excreción | Heces (%) y orina | |
| Datos clínicos | ||
| Estado legal | POM (UK) ? (EUA) | |
| Vías de adm. | Oral, nasal, traqueal o rectal | |
La budesónida es un medicamento glucocorticoide, de la familia de los corticosteroides,[1] disponible como inhalador, píldora, aerosol nasal, solución para nebulizar y formas rectales.[1][2] En su forma inhalada, se utiliza para el tratamiento a largo plazo del asma y de la enfermedad pulmonar obstructiva crónica,[1][3][4] mientras que como aerosol nasal está indicada para la rinitis alérgica y la poliposis nasal.[2][5] Las demás formas de administración de la budesónida antes citadas pueden utilizarse para el tratamiento de la enfermedad inflamatoria intestinal, la enfermedad de Crohn, la colitis ulcerosa y la colitis microscópica.[6][7]
Los efectos secundarios más comunes en su forma inhalada incluyen infecciones respiratorias, tos y dolores de cabeza, mientras que la budesónida en píldoras puede provocar cansancio, vómitos y dolores en las articulaciones. Los efectos adversos más graves pueden incluir mayor exposición a infecciones, perforación nasal y graves dificultades para respirar.[8] El uso a largo plazo de las píldoras de budesónida puede causar insuficiencia adrenal y detener su consumo de forma repentina puede ser peligroso. Por su parte, inhalada no entraña riesgos (generalmente) durante el embarazo.
La budesónida se patentó en 1973[9] y su comercialización comenzó en 1981 como medicamento para el asma.[9] Está en la lista de medicamentos esenciales de la Organización Mundial de la Salud, donde se recogen los medicamentos que todo sistema de salud básico debería tener.[10] También está disponible como medicamento genérico.[11] En los países en vías de desarrollo, el precio al por mayor de un inhalador de 200 dosis era de entre 5 y 7 dólares estadounidenses (USD) en 2014[12] y es un medicamento sufragado por los sistemas públicos de salud europeos; sin embargo, en Estados Unidos su precio es mucho mayor y el precio de un mes de tratamiento oscilaba entre los 100 y 200 USD en 2015.[11]
Estereoquímica
[editar]| Budesónida (2 estereoisómeros) | |
|---|---|
 (22R)-configuración |
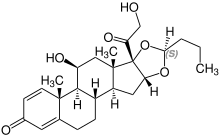 (22S)-configuración |
Farmacodinámica
[editar]Budesonida es ampliamente metabolizada al primer paso. Tiene eficacia en el íleon terminal y el colon ascendente. La budesonida comparativamente a prednisolona tendría menor perdida de densidad ósea y a diferencia de otros corticosteroides ejerce poca influencia en el eje hipotalámico-hipofisario-adrenal. En general, tiene poca incidencia en las manifestaciones sistémicas comparado con otros medicamentos afines.
Inhalación oral de budesónida
[editar]La budesónida se utiliza para evitar la dificultad para respirar, opresión en el pecho, sibilancia y tos ocasionada por asma. El polvo de budesónida para inhalación oral se usa en adultos y niños mayores de 6 años. La suspensión de budesónida (líquido) para inhalación oral se usa en niños de 12 meses a 8 años de edad. La budesónida disminuye la hinchazón e irritación en las vías respiratorias y así permite una respiración más fácil.
Reacciones adversas
[editar]
Budesónida puede provocar:[13]
- Irritación o ardor nasal.
- Hemorragia o escoriaciones de fosas nasales (uso vía nasal).
- Dolor estomacal.
- Tos.
- Carraspera (a modo de laringitis).
- Sequedad de boca.
- Rash.
- Picazón de garganta.
- Mal gusto.
- Cambios en la coloración del mucus.
Además la siguiente sintomatología debiera informarse inmediatamente:
- Dificultad para respirar o hinchamiento de la cara.
- Perforación del tabique nasal con uso vía nasal, aunque es extremadamente raro.[8]
- Manchas blancas en la garganta, boca o nariz.
- Trastornos menstruales.
- Acné grave.
- A veces, cambios de conducta —cuando aparecen, afectan principalmente a los niños.
Notas
[editar]- ↑ a b c «Budesonide». Drugs.com (en inglés). The American Society of Health-System Pharmacists. Consultado el 3 de diciembre de 2016.
- ↑ a b «Budesonide eent». Drugs.com (en inglés). The American Society of Health-System Pharmacists. 2016. Consultado el 3 de diciembre de 2015.
- ↑ Coster, Daan A. De; Jones, Melvyn (6 de julio de 2014). «Tailoring of corticosteroids in COPD management». Current Respiratory Care Reports (en inglés) 3 (3): 121-132. ISSN 2161-332X. PMC 4113685. PMID 25089228. doi:10.1007/s13665-014-0084-2. Consultado el 3 de diciembre de 2016.
- ↑ Christophi, George P.; Rengarajan, Arvind; Ciorba, Matthew A. (1 de enero de 2016). «Rectal budesonide and mesalamine formulations in active ulcerative proctosigmoiditis: efficacy, tolerance, and treatment approach». Clinical and Experimental Gastroenterology 9: 125-130. PMC 4876845. PMID 27274301. doi:10.2147/CEG.S80237. Consultado el 3 de diciembre de 2016.
- ↑ Rudmik, Luke; Schlosser, Rodney J.; Smith, Timothy L.; Soler, Zachary M. (1 de julio de 2012). «Impact of topical nasal steroid therapy on symptoms of nasal polyposis». The Laryngoscope (en inglés) 122 (7): 1431-1437. ISSN 1531-4995. doi:10.1002/lary.23259. Consultado el 3 de diciembre de 2016.
- ↑ Silverman, Jason; Otley, Anthony (1 de julio de 2011). «Budesonide in the treatment of inflammatory bowel disease». Expert Review of Clinical Immunology 7 (4): 419-428. ISSN 1744-666X. PMID 21790284. doi:10.1586/eci.11.34. Consultado el 3 de diciembre de 2016.
- ↑ Pardi, Darrell S.; Tremaine, William J.; Carrasco-Labra, Alonso (1 de enero de 2016). «American Gastroenterological Association Institute Technical Review on the Medical Management of Microscopic Colitis». Gastroenterology 150 (1): 247-274.e11. ISSN 1528-0012. PMID 26584602. doi:10.1053/j.gastro.2015.11.006. Consultado el 3 de diciembre de 2016.
- ↑ a b «Prospecto: información para el paciente. Budesonida nasal Aldo-Unión 100 microgramos/dosis». www.aemps.gob.es. Agencia Española del Medicamento y Productos Sanitarios. abril de 2013. Consultado el 14 de noviembre de 2016.
- ↑ a b Domeij, Bengt (15 de marzo de 2000). Pharmaceutical Patents in Europe (en inglés). Martinus Nijhoff Publishers. ISBN 9041113487. Consultado el 3 de diciembre de 2016.
- ↑ «WHO Model List of Essential Medicines». Organización Mundial de la Salud (OMS). abril de 2013. Consultado el 3 de diciembre de 2016.
- ↑ a b Hamilton, Richart (2015). Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. Jones & Bartlett Learning. p. 451. ISBN 9781284057560.
- ↑ «Budesonide». www.erc.msh.org (en inglés). Guía Internacional de Indicadores de Precios de Medicamentos. 2014. Consultado el 3 de diciembre de 2016. (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- ↑ BUDESONIDE - NASAL AEROSOL INHALER (Rhinocort) side effects, medical uses, and drug interactions
Enlaces externos
[editar] Wikimedia Commons alberga una categoría multimedia sobre Budesónida.
Wikimedia Commons alberga una categoría multimedia sobre Budesónida.