Tetrodotoxina
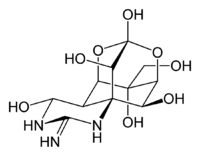
| tetrodotoxina | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| (4R,4aR,5R,6S,7S,8S,8aR,10S,12S)-2-azaniomilideno-4,6,8,12-tetrahidroxi-6-(hidroximetil)-2,3,4,4a,5,6,7,8-octahidro-1H-8a,10-metano-5,7-(epoximetanooxi)quinazolin-10-olato | ||
| General | ||
| Otros nombres | anhidrotetrodotoxina, 4-epitetrodotoxina, ácido tetrodónico, TTX | |
| Fórmula estructural |
 | |
| Fórmula molecular | C11H17N3O8 | |
| Identificadores | ||
| Número CAS | 4368-28-9[1] | |
| Número RTECS | IO1450000 | |
| ChEBI | 9506 | |
| ChemSpider | 9349691 | |
| KEGG | C11692 | |
|
O1[C@@H]4[C@@](O)([C@@H]3O[C@@]1(O)[C@@H](O)[C@]2(N\C(=N/[C@H](O)[C@H]23)N)[C@@H]4O)CO
| ||
| Propiedades físicas | ||
| Masa molar | 319,268 g/mol | |
| Riesgos | ||
| LD50 | 5-8 µg/kg | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La tetrodotoxina, generalmente abreviada como TTX, es una neurotoxina mortal de actuación potente y rápida,[2] derivada de las quinazolinas, de origen principalmente marino. A pesar de producir anualmente miles de intoxicaciones y varias muertes[3], ha mostrado eficacia en varios ensayos clínicos fase II y III para el tratamiento del dolor asociado a cáncer.
Características
[editar]Se trata de un compuesto amino (una perhidroquinazolina) con un peso molecular de 319 Da.[4] Es una base monoacídica con un pKa de 8,5 en solución acuosa. Es soluble en agua, pero se descompone fácilmente en condiciones fuertemente ácidas o alcalinas siendo estable en un amplio rango de pH(3-8,5).
La toxicidad puede ser anulada por la acción de hidróxido de sodio al 2% durante 90 minutos. Debido a que la toxina no es proteica, es relativamente estable al frío y al calor. La molécula tiene una estructura tricíclica y contiene un grupo guanidino cargado positivamente.
Fuentes en la naturaleza
[editar]Previamente se pensaba que el envenenamiento por tetrodotoxina se producía casi exclusivamente a partir de la intoxicación por peces globo,[4] sin embargo la evidencia más reciente ha demostrado que la toxina también se puede encontrar en una amplia variedad de organismos acuáticos, anfibios y otros, incluido géneros de bacterias. No obstante el origen de la tetrodotoxina en estas especies se desconoce.
La distribución irregular de la tetrodotoxina en especies tan diferentes sugiere que la toxina se adquiere a través de la cadena alimentaria como consecuencia de algas marinas tóxicas. Dicha hipótesis se basa en el descubrimiento de tetrodotoxina producida por bacterias del género Pseudomonas aislada del alga roja Jania y a la diferencia observada en cuanto a toxicidad entre peces globo de la misma especie dependiendo de la región en la que habiten. Sin embargo, algunos investigadores opinan que la capacidad de sintetizar tetrodotoxina por parte de diversos organismos marinos y anfibios puede ser simplemente una coincidencia en el desarrollo genético debido a su alto valor de cara a la supervivencia de la especie que la produce.
El hallazgo de glándulas exocrinas únicas para la secreción de tetrodotoxina en el pez globo, así como su almacenamiento en las glándulas postsalivares del pulpo de anillos azules admite la posibilidad de que algunas especies sean capaces de producir la toxina.
Mecanismo de acción
[editar]Esta toxina suprime la propagación de los potenciales de acción a través de un bloqueo neuronal selectivo de los canales de sodio dependientes de voltaje, concretamente los canales de sodio 1.6, cuya función es conducir el potencial de acción.[4] En algunos experimentos se ha demostrado que, a altas concentraciones, reduce la producción de acetilcolina y disminuye la actividad de la citocromo oxidasa y de la acetilcolinesterasa.
La tetrodotoxina es aproximadamente 160.000 veces más potente que la cocaína en el bloqueo de la conducción axonal de las neuronas sensoriales. El sitio de unión a TTX es muy estrecho. Se encuentra en la cara extracelular del canal de sodio[5] y está presente en todas la isoformas conocidas del canal; por lo tanto, la afinidad a la toxina es independiente de la isoforma. Tras la unión de la TTX a un residuo de glutamato del canal de sodio, tiene lugar un cambio conformacional en la estructura del canal responsable de la inhibición de entrada de sodio a través del mismo.
Intoxicación
[editar]La más conocida y común es por ingesta de carne de peces globo.[6] Estos animales producen una toxina en sus gónadas, la tetradotoxina o fugutoxina, que se acumula posteriormente en su piel y en su hígado sin que a ellos mismos les afecte.
La intoxicación se produce por la ingestión de estos tejidos sin afectar a la parte muscular del animal. Su carne es comestible porque habitualmente sus músculos están libres de tetrodotoxina. Con ellos se prepara el famoso “Fugu”.
Toxicidad
[editar]La TTX es extremadamente tóxica. Puede acceder al cuerpo por ingestión, inyección, inhalación y a través de la piel dañada.[2]
La DL50 es 8 µg/kg por vía intravenosa, alrededor de 2 µg/kg si se inhala y de 30 µg/kg por vía oral. Ingerida requiere dosis mayores porque el ácido estomacal destruye esta toxina.
Tetrodotoxismo
[editar]Es un cuadro de intoxicación de pescado, el pez globo, una exquisitez culinaria[6] muy típica, pero no exclusiva de Japón.[4]
La molécula implicada en este envenenamiento es la tetrodotoxina, neurotoxina considerada uno de los venenos más potentes del reino marino.
Fisiopatología
[editar]La depresión respiratoria es el signo clínico más destacado del efecto tóxico que produce la tetrodotoxina.[2] Esta depresión se produce por parálisis directa de los músculos diafragmáticos, los cuales son muy sensibles a la acción de la tetrodotoxina, sobre todo el diafragma (se considera que con un 4% de la DL50 ya hay efectos sobre la respiración), debido a la mayor irrigación sanguínea, lo que conlleva a una llegada más rápida y a una mayor proporción de toxina en estos músculos. Además, la tetrodotoxina es capaz de producir depresión del reflejo de la tos y relaja la musculatura lisa bronquial.
Otro síntoma importante es la severa hipotensión asociada o no a bradicardia. La hipotensión se atribuye más a una vasodilatación periférica que a una depresión de la actividad cardíaca. Parece deberse a una combinación del efecto relajante directo sobre el músculo liso de las paredes vasculares y al bloqueo de la conducción nerviosa vasomotora.
La primera acción sistémica de la tetrodotoxina es el bloqueo de la conducción nerviosa, empieza sobre nervios periféricos, y después alcanza el Sistema Nervioso Central, concretamente los centros respiratorios y vasomotor. Esta toxina bloquea las respuestas del Sistema Nervioso Autónomo y como consecuencia puede producir una disminución de la secreción gástrica, midriasis, hipersalivación e hiperglucemia.
Sintomatología
[editar]El comienzo de los síntomas ocurre en cuestión de minutos cuando la toxina es inyectada o inhalada pero si es ingerida el desarrollo es más lento (10 a 40 minutos).[2]
El primer síntoma de intoxicación es insensibilidad ligera de los labios y la lengua, apareciendo entre 20 minutos y tres horas después de tomar el alimento con la toxina. El siguiente síntoma es parestesia en la cara y extremidades, que puede ir seguida de sensación de ligereza. Puede darse dolor de cabeza, dolor epigástrico, náuseas, diarrea y/o vómitos. Ocasionalmente también puede presentarse dificultad al caminar.
La segunda etapa de la intoxicación es un aumento de la parálisis: muchas víctimas son incapaces de moverse, incluso sentarse puede resultar difícil. La víctima sufre debilidad, dilatación de las pupilas, tics, temblores y pérdida de la coordinación muscular y de la voz. Hay aumento de la insuficiencia respiratoria. Se incrementa la parálisis y las convulsiones, discapacidad mental y pueden darse arritmias cardíacas. La víctima aunque esté completamente paralizada puede estar consciente y en algunos casos completamente lúcida antes de la muerte.
La muerte normalmente ocurre en cuatro o seis horas, con un margen de 20 minutos a ocho horas.
Tratamiento
[editar]El tratamiento del tetradotoxismo consiste en limitar al máximo la absorción de la toxina y aliviar la sintomatología, puesto que hoy en día no existe antídoto.[6]
Es recomendable realizar un lavado gástrico, mientras que el tratamiento específico lo determinará el médico basándose en el estado general del paciente, en la tolerancia a determinados medicamentos, así como en la fase en la que se encuentre la intoxicación.
Información útil
[editar]- Los peces globo son inmunes a la toxina, debido a que la proteína que conforma los canales celulares de sodio es diferente al resto de especies, lo que impide su unión.[4]
- El contenido tóxico de un pez globo podría ocasionar la muerte de unas 30 personas adultas.
- En Japón, y últimamente en países como los Estados Unidos, el pez globo es considerado una exquisitez y varias decenas de personas mueren cada año como consecuencia de su consumo. Debido a la elevada mortalidad que se produjo en Japón en 1958 (alrededor de 180 muertes), se reglamentó por ley la preparación de este alimento. Desde entonces sólo la pueden llevar a cabo cocineros que han realizado un curso de adiestramiento y manipulación oficial que dura 3-5 años, con un examen final muy riguroso.
- Debido a que en la actualidad la mortalidad por esta intoxicación alimentaria resulta ser superior al 50%, es considerada la intoxicación más grave producida por peces.[6]
Referencias
[editar]- ↑ Número CAS
- ↑ a b c d Patocka J; Stredav L (23 de abril de 2002). «BRIEF REVIEW OF NATURAL NONPROTEIN NEUROTOXINS». Consultado el 19 de noviembre de 2014.
- ↑ Guardone, Lisa; Maneschi, Andrea; Meucci, Valentina; Gasperetti, Laura; Nucera, Daniele; Armani, Andrea (2 de octubre de 2020). «A Global Retrospective Study on Human Cases of Tetrodotoxin (TTX) Poisoning after Seafood Consumption». Food Reviews International (en inglés) 36 (7): 645-667. ISSN 8755-9129. doi:10.1080/87559129.2019.1669162. Consultado el 23 de mayo de 2023.
- ↑ a b c d e Bergillos Gasion, Dr. Fernando. Toxicología clínica. Lesiones por picaduras y mordeduras de animales, Volumen 2. ISBN 978-84-686-3690-0.
- ↑ Emilio Salceda y Aída Ortega. «Neurotoxinas: significado biológico y mecanismos de acción». Archivado desde el original el 17 de diciembre de 2014. Consultado el 19 de noviembre de 2014.
- ↑ a b c d Buceo XXI. «Envenenadas delicatessen». Consultado el 19 de noviembre de 2014.
Enlaces externos
[editar] Wikimedia Commons alberga una categoría multimedia sobre Tetrodotoxina.
Wikimedia Commons alberga una categoría multimedia sobre Tetrodotoxina.