Vaccinia virus
| Vaccinia virus | ||
|---|---|---|
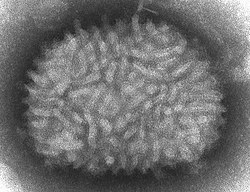 | ||
| Taxonomía | ||
| Dominio: | Varidnaviria | |
| Reino: | Bamfordvirae | |
| Filo: | Nucleocytoviricota | |
| Clase: | Pokkesviricetes | |
| Familia: | Poxviridae | |
| Género: | Orthopoxvirus | |
| Especie: | Vaccinia virus | |
| Clasificación de Baltimore | ||
| Grupo: | I (Virus ADN bicatenario) | |
Vaccinia virus, VACV, VV o virus vacuna es un virus bien conocido por su papel como vacuna en la erradicación de la enfermedad de la viruela, la primera enfermedad erradicada con éxito de la humanidad. Esta tarea fue llevada a cabo por la Organización Mundial de la Salud en el marco del Programa de Erradicación de la Viruela.
Aunque es un virus artificial se desconoce exactamente su origen, debido a la falta de registros de los primeros cultivos. Actualmente los investigadores consideran que no procede del virus que propiamente produce la «viruela bovina» (Cowpox virus), sino que sería una especie relacionada que fue aislada originariamente de los caballos.
Origen
[editar]El virus vacuna (Vaccinia virus) está estrechamente relacionado con el virus de la viruela bovina (Cowpox virus); históricamente a menudo se los ha considerado como el mismo virus.[1] El origen exacto del Vaccinia virus es desconocido debido a la falta de mantenimiento de los registros de virus cultivados en los laboratorios de investigación durante muchos decenios;[2] se especula que fuera originalmente aislado de los caballos.[1]
Sin embargo, la vacuna original contra la viruela y el origen de la idea de la vacunación es el Cowpox virus, utilizado por Edward Jenner en 1796.[2] El término latino empleado en esa época para referirse al «cowpox» era variolae vaccinae, traducción directa de "viruela bovina". Ese término ha prestado su nombre a la idea de la vacunación. Años después, cuando se notó que el virus que se estaba utilizado en la vacuna antivariólica había dejado de ser «cowpox», el nombre vaccinia se transfirió al nuevo virus. Se considera que Vaccinia virus, Cowpox virus y Variola virus (virus de la viruela) derivan de un virus ancestral común.
Biología
[editar]Es un virus grande, complejo, con envoltura, perteneciente a la familia Poxviridae.[3] Tiene una genoma ADN bicatenario lineal, de aproximadamente 190 Kbp de longitud, y que codifica para aproximadamente 250 genes. Las dimensiones del virion son de alrededor de 360 × 270 × 250 nm.
Poxviridae son únicos entre los virus ADN por reproducirse únicamente en el citoplasma de la célula huésped, fuera del núcleo.[4] Por lo tanto, precisan de un gran genoma para la codificación de diversas enzimas y proteínas implicadas en la replicación del ADN viral y en la transcripción.
Durante su ciclo de replicación, el virus vacuna produce cuatro formas infecciosas que difieren en su membrana exterior: virión maduro intracelular (IMV), virión intracelular con envoltura (IEV), virión con envoltura asociado a la célula (CEV) y virión extracelular con envoltura (VEM).[5] Aunque la cuestión es controvertida, la opinión predominante es que IMV consta de una única membrana de lipoproteína, mientras que CEV y VEM están rodeadas por dos capas de membrana e IEV presenta tres capas.
IMV es la forma infecciosa más abundante y se piensa que es la responsable de la propagación entre huéspedes. Por otra parte, CEV se cree que desempeña un papel en la diseminación célula a célula y VEM en la difusión a distancias más largas dentro del organismo hospedador.
El virus contiene en su genoma varias proteínas que le dan resistencia contra los interferones. K3L es una proteína con homología a las proteínas eucarióticas de inicio factor 2 (FEI-2alpha). La proteína K3L inhibe la acción de PKR, un activador de los interferones. E3L es otra proteína codificada por el virus. E3L también inhibe la activación de PKR y es capaz de unirse al ARN bicateniario.[6]
Actualmente, los científicos estudian el virus vacuna para su uso como una herramienta para la introducción de genes en los tejidos biológicos (terapia génica e ingeniería genética). Por otra parte, debido a la preocupación reciente de que la viruela pueda ser usada como agente de bioterrorismo, los científicos han renovado su interés en el estudio del virus vacuna.
Uso como vacuna
[editar]
Una infección por el virus vacuna es muy leve y normalmente asintomática en individuos sanos, pero puede causar una leve erupción y fiebre. La respuesta inmune generada a partir de la infección de este virus protege a la persona contra la viruela, por este motivo se utiliza como vacuna contra la viruela. A diferencia de las vacunas que utilizan formas debilitadas de los virus, esta vacuna no puede causar una infección de viruela, ya que no contiene el virus de la viruela. Sin embargo, se producen a veces algunas complicaciones y efectos secundarios. La probabilidad de que esto ocurra es significativamente mayor en las personas inmunocomprometidas. Aproximadamente una de cada millón de personas desarrollará una respuesta fatal a la vacunación.
Actualmente, la vacuna sólo se administra a los trabajadores de la salud o de investigación que tienen un alto riesgo de contraer la viruela y al personal militar de los Estados Unidos de América. Debido a la actual amenaza de la viruela relacionada con el bioterrorismo, existe la posibilidad de que la vacuna puede tener que ser administrada ampliamente a la población. Por lo tanto, los científicos están desarrollando actualmente nuevas estrategias de vacunas contra la viruela que son más seguras y mucho más rápidas de administrar en caso de bioterrorismo. En septiembre de 2007 la Food and Drug Administration (FDA) de EE. UU. licenció una nueva vacuna (ACAM2000) contra la viruela que puede producirse rápidamente en caso de necesidad. Actualmente los centros para el Control y Prevención de Enfermedades de EE. UU. almacenan 192,5 millones de dosis de la nueva vacuna (derivada de la antigua Dryvax y fabricada utilizando un virus vacuna).[7]
En marzo de 2007, un niño de dos años de edad contrajo la infección por el virus vacuna debido a un eczema, que es un conocido factor de riesgo para la infección.[8] El niño fue contagiado por su padre que al pertenecer al ejército de EE. UU. había sido vacunado con el virus. El niño desarrolló erupción en más del 80 por ciento de su cuerpo y fue tratado con inmunoglobulina intravenosa, cidofovir y un fármaco experimental que se está desarrollando en SIGA Technologies.[9] El niño se curó sin secuelas a excepción de las posibles cicatrices en la piel.
JX-594 - virus oncolítico - modificación genética
[editar]JX-594 es un virus oncolítico desarrollado por la empresa privada estadounidense Jennerex[10] diseñado para localizar, atacar y destruir las células del cáncer.[11][12] JX-594 es una modificación, mediante ingeniería genética, del poxviridae Vaccinia virus (virus utilizado como vacuna para la erradicación de la viruela) diseñado para reproducirse de forma selectiva en células tumorales que tienen activividad vía EGFR/Ras, pero no así en el tejido normal. El vaccinia virus modificado facilita la transferencia del gen (transgen) a las células de cáncer que las mata por lisis.[13][14] JX-594 está en fases muy avanzadas de ensayos clínicos para el cáncer de hígado.[13][15][16]
Referencias
[editar]- ↑ a b Huygelen C (1996). «Jenner's cowpox vaccine in light of current vaccinology». Verh. K. Acad. Geneeskd. Belg. (en neerlandés) 58 (5): 479-536; discussion 537-8. PMID 9027132.
- ↑ a b Henderson DA, Moss B (1999) [1988]. «Smallpox and Vaccinia». En Plotkin SA, Orenstein WA, ed. Vaccines (3rd ed edición). Philadelphia, Pennsylvania: WB Saunders. ISBN 0-7216-7443-7. Consultado el 25 de julio de 2007.
- ↑ Ryan KJ, Ray CG (editors) (2004). Sherris Medical Microbiology (4th ed. edición). McGraw Hill. ISBN 0-8385-8529-9.
- ↑ Tolonen N, Doglio L, Schleich S, Krijnse Locker J (2001). «Vaccinia virus DNA replication occurs in endoplasmic reticulum-enclosed cytoplasmic mini-nuclei». Mol. Biol. Cell 12 (7): 2031-46. PMID 11452001.
- ↑ Smith GL, Vanderplasschen A, Law M (2002). «The formation and function of extracellular enveloped Vaccinia virus». J. Gen. Virol. 83 (Pt 12): 2915-31. PMID 12466468. Archivado desde el original el 23 de abril de 2010. Consultado el 27 de julio de 2008.
- ↑ Davies MV, Chang HW, Jacobs BL, Kaufman RJ (1993). «The E3L and K3L vaccinia virus gene products stimulate translation through inhibition of the double-stranded RNA-dependent protein kinase by different mechanisms». J. Virol. 67 (3): 1688-92. PMID 8094759.
- ↑ Canadian Press, FDA licenses new vaccine against smallpox; can be produced quickly if needed
- ↑ Centers for Disease Control and Prevention (CDC) (2007). «Household transmission of vaccinia virus from contact with a military smallpox vaccinee--Illinois and Indiana, 2007». Morbidity and Mortality Weekly Report 56 (19): 478-81. PMID 17510612.
- ↑ «SIGA’s Smallpox Drug Candidate Administered to Critically Ill Human Patient». SIGA Technologies. 17 de marzo de 2007. Archivado desde el original el 22 de junio de 2007. Consultado el 5 de junio de 2007.
- ↑ Jennerex – About
- ↑ Jennerex Biotherapeutics, Inc [1] Press Release (2010)
- ↑ PR Newswire [2] Press Release (2011).
- ↑ a b «Novel Cancer-Targeting Virus Therapy Shows Efficacy in Early-Stage Trial». 31 de agosto de 2011.
- ↑ Breitbach at al. (2011). Intravenous delivery of a multi-mechanistic cancer-targeted oncolytic poxvirus in humans. doi:10.1038/nature10358. Archivado desde el original el 24 de septiembre de 2011.
- ↑ September 01, 2011 - Voice of America
- ↑ «Cancer-fighting virus shown to target tumors alone». Aug 31, 2011. Archivado desde el original el 5 de noviembre de 2011. Consultado el 17 de septiembre de 2011.
Véase también
[editar]- Variola virus (virus de la viruela)
- Cowpox virus (virus de la viruela bovina)
- Edward Jenner