سطح انرژی پتانسیل
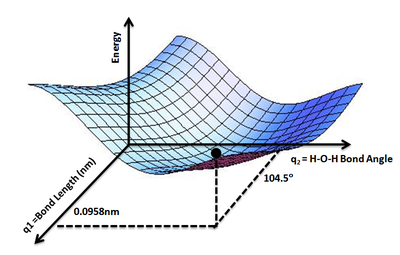
سطح انرژی پتانسیل (به انگلیسی: Potential energy surface) یا چشمانداز انرژی، انرژی یک سیستم (مانند مجموعهای از اتمها) را بر اساس پارامترهایی مانند موقعیت اتمها، نشان میدهد. این سطح میتواند انرژی را بهصورت تابعی از یک یا چند مختصات تعریف کند. اگر تنها یک مختصات در نظر گرفته شود، به این سطح "منحنی انرژی پتانسیل" یا "پروفایل انرژی" گفته میشود. یک نمونه از این مفهوم، پتانسیل مورس/بلندبرد (Morse/Long-range potential) است.استفاده از یک قیاس مانند چشمانداز برای درک بهتر مفید است: در سیستمی با دو درجه آزادی (مثلاً دو طول پیوند)، انرژی سیستم (مشابه ارتفاع زمین) بهصورت تابعی از دو طول پیوند تعریف میشود (مشابه مختصات موقعیت روی زمین).[۱]

مفهوم منحنی انرژی پتانسیل (PES) در حوزههایی مانند فیزیک، شیمی و بیوشیمی، بهویژه در شاخههای نظری این علوم، کاربرد دارد. این مفهوم برای بررسی نظری خواص ساختارهای اتمی مفید است؛ مثلاً برای تعیین شکل با حداقل انرژی یک مولکول یا محاسبه نرخ واکنشهای شیمیایی. همچنین میتوان از آن برای توصیف تمام حالتهای ممکن یک مولکول، موقعیتهای فضایی مولکولهای در تعامل، یا پارامترها و سطوح انرژی مرتبط (مانند انرژی آزاد گیبس) استفاده کرد.
از نظر هندسی، چشمانداز انرژی نمایشی از تابع انرژی در فضای پیکربندی سیستم است. این مفهوم بهطور گستردهتر در هندسه مرتبط با بهینهسازی ریاضی نیز به کار میرود، زمانی که دامنه تابع زیان، فضای پارامترهای یک سیستم باشد.
تعریف ریاضی و محاسبه
[ویرایش]هندسه یک مجموعه از اتمها را میتوان با یک بردار r توصیف کرد، که عناصر آن نشاندهنده موقعیت اتمها هستند. بردار r میتواند شامل مجموعهای از دستگاه مختصات دکارتی اتمها باشد، یا میتواند مجموعهای از فواصل بیناتمی و زوایا را در بر گیرد.
با داشتن r، انرژی بهعنوان تابعی از موقعیتها، (r)E مقدار، E(r) را برای تمامی E(r) های مورد نظر ارائه میدهد. با استفاده از قیاس "چشمانداز انرژی" که در مقدمه مطرح شد، E ارتفاع را روی "چشمانداز انرژی" نشان میدهد و از این طریق مفهوم سطح انرژی پتانسیل شکل میگیرد.
برای مطالعه یک واکنش شیمیایی با استفاده از سطح انرژی پتانسیل (PES) بهعنوان تابعی از موقعیت اتم ها، لازم است انرژی را برای هر آرایش اتمی مورد نظر، محاسبه کرد. روشهای محاسبه انرژی یک آرایش خاص از اتمها بهخوبی در مقاله شیمی محاسباتی توضیح داده شدهاند، و تأکید اینجا بر یافتن تقریبهایی برای E(r) بهمنظور ارائه اطلاعات دقیق و جزئی از رابطه انرژی-موقعیت خواهد بود.
برای سیستمهای شیمیایی بسیار ساده یا در شرایطی که تقریبهایی در برهمکنشهای بیناتمی اعمال میشود، گاهی میتوان از یک رابطه تحلیلی مشتقشده برای انرژی بهعنوان تابعی از موقعیت اتمها استفاده کرد.
برای سیستمهای پیچیدهتر، محاسبه انرژی یک آرایش خاص از اتمها، اغلب از نظر محاسباتی بسیار پرهزینه است، بهطوری که ایجاد نمایشهای گسترده از سطح انرژی پتانسیل (PES) امکانپذیر نیست. برای این سیستمها، یک رویکرد ممکن این است که تنها یک مجموعه محدود از نقاط روی PES محاسبه شود و سپس از یک روش میانیابی کمهزینهتر از نظر محاسباتی، مانند میانیابی شپرد (Shepard interpolation)، برای پر کردن فواصل بین نقاط استفاده شود.[۲]
کاربرد
[ویرایش]سطح انرژی پتانسیل (PES) ابزاری مفهومی است که برای بررسی شکل مولکولی و دینامیک واکنشهای شیمیایی استفاده میشود. پس از بررسی نقاط کلیدی روی PES، این نقاط بر اساس مشتقات مرتبه اول و دوم انرژی نسبت به موقعیت طبقهبندی میشوند که به ترتیب نشاندهنده گرادیان و انحنای سطح هستند. نقاط سکون (نقاط با گرادیان صفر) معنای فیزیکی خاصی دارند: کمینههای انرژی نشاندهنده گونههای شیمیایی پایدار هستند و نقاط زینی حالتهای گذار را نشان میدهند، که بالاترین نقطه انرژی در مسیر واکنش محسوب میشوند. مسیر واکنش نیز کمانرژیترین راه اتصالدهنده واکنشدهندهها به محصولات است.
این موضوع در بررسی فرآیند تاشدگی پروتئین بسیار مفید است؛ در حالی که یک پروتئین از نظر تئوری میتواند تعداد تقریباً بینهایتی از حالتهای ساختاری را در تمام حالات انرژی خود اختیار کند، در واقعیت، پروتئینها به سمت ساختارهای دوم و سومی که دارای کمترین انرژی آزاد ممکن هستند، تا میشوند.
در کاتالیز، هنگام طراحی یا بهبود کاتالیزرها، به وضعیتهای انرژی توجه میشود تا از واسطههایی با انرژی خیلی پایین (که ممکن است واکنش را متوقف کنند) یا واسطههایی با انرژی خیلی بالا (که انرژی زیادی برای رسیدن به محصول نهایی نیاز دارند) جلوگیری شود.[۳]
در یادگیری ماشین (machine learning)، شبکههای عصبی مصنوعی ممکن است با استفاده از روشهای مشابه تحلیل شوند.[۴] برای مثال، یک شبکه عصبی ممکن است بتواند دادههای مجموعه آموزش را کاملاً تطبیق دهد، که معادل رسیدن به کمینه جهانی با مقدار ضرر صفر است.
سطوح جاذبه و دافعه
[ویرایش]سطوح انرژی پتانسیل برای واکنشهای شیمیایی میتوانند بر اساس مقایسه تغییرات طول پیوندها در کمپلکس فعال نسبت به واکنشدهندهها و محصولات به عنوان جاذبهای یا دافعهای طبقهبندی شوند.[۵][۶] در واکنشی از نوع A + B—C → A—B + C، افزایش طول پیوند برای پیوند تازه تشکیلشده A—B به این صورت تعریف میشود: R*AB = RAB − R0AB که در آن RAB طول پیوند A—B در حالت گذار و R0AB طول پیوند A—B در مولکول محصول است. به همین ترتیب، برای پیوندی که در واکنش شکسته میشود: R*BC = RBC − R0BC که R0BC به طول پیوند B—C در مولکول واکنشدهنده اشاره دارد.
تاریخچه
[ویرایش]مفهوم سطح انرژی پتانسیل در واکنشهای شیمیایی اولین بار در سال ۱۹۱۳ توسط فیزیکدان فرانسوی رنه مارسِلَن(René Marcelin) معرفی شد. سپس در سال ۱۹۳۱، هنری آیرینگ و مایکل پولانی اولین محاسبه نیمهتجربی این سطح انرژی را برای واکنش H + H2 ارائه دادند. آیرینگ در سال ۱۹۳۵ از این سطوح انرژی برای محاسبه سرعت واکنشها با استفاده از نظریه حالت گذار بهره گرفت.
سطح انرژی پتانسیل دو بعدی برای H + H2
سطوح انرژی پتانسیل (PES) معمولاً بهصورت نمودارهای سهبعدی نشان داده میشوند، اما میتوان آنها را در قالب نمودارهای دوبعدی نیز ترسیم کرد. در این نمودارها، پیشرفت واکنش از طریق خطوط همانرژی که بهطور مشخص نشاندهنده انرژی ثابت در نقاط مختلف سیستم هستند، نشان داده میشود.
یکی از واکنشهای سادهای که میتوان آن را بهصورت دوبعدی نمایش داد، واکنش همراسته H + H₂ است. در این واکنش، یک اتم هیدروژن (H) با یک مولکول دیهیدروژن (H₂) واکنش میدهد و با یکی از اتمهای مولکول پیوند جدیدی میسازد، در حالی که پیوند قبلی مولکول شکسته میشود. این واکنش بهصورت Ha + Hb–Hc → Ha–Hb + Hc نمادگذاری میشود.
در این واکنش، پیشرفت از مرحله واکنشدهندهها (H + H₂) به محصولات (H–H–H) و انرژی گونههای مختلف که در واکنش دخیل هستند، در سطح انرژی پتانسیل بهوضوح مشخص است. این سطح انرژی به ما کمک میکند تا مسیرهای مختلف واکنش و انرژی مربوط به هر مرحله از واکنش را مشاهده کنیم.
در نهایت، پروفایلهای انرژی، انرژی پتانسیل را بهعنوان تابعی از متغیرهای هندسی مانند فاصلهها و زوایا بین اتمها توصیف میکنند. این سطوح انرژی پتانسیل برای هر واکنشدهندهای در هر ابعادی که باشند، مستقل از زمان و دما هستند.
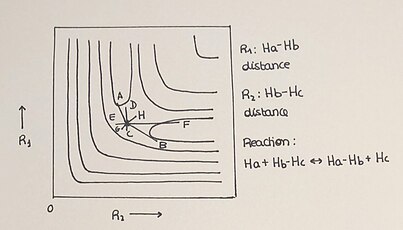
ما در سطح انرژی پتانسیل دوبعدی (2-D PES) عناصر مختلف و مرتبطی داریم:
- نمودار دوبعدی نقاط مینیمای مربوط به واکنشدهندهها، محصولات و نقطه زین یا حالت گذار را نشان میدهد.
- حالت گذار نقطهای است که در طول مختصات واکنش بهعنوان یک ماکسیمم و در مختصات عمود بر مسیر واکنش بهعنوان یک مینیمم عمل میکند.
- با گذر زمان، هر واکنش یک مسیر یا trajectory را توصیف میکند. بسته به شرایط واکنش، این فرآیند روشهای مختلفی را برای رسیدن به تشکیل محصول نشان میدهد که بین دو محور ترسیم میشود.
جستارهای وابسته
[ویرایش]منابع
[ویرایش]- ↑ McNaught and A. Wilkinson. Blackwell Scientific (۱۹۹۷). Potential-energy (reaction) surface in Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Publications, Oxford.
- ↑ Moving least-squares enhanced Shepard interpolation for the fast marching and string methods, Burger SK1, Liu Y, Sarkar U, Ayers PW, J Chem Phys. 2009 130(2) 024103. doi: 10.1063/1.2996579.
- ↑ Chen, Shentan; Ho, Ming-Hsun; Bullock, R. Morris; DuBois, Daniel L.; Dupuis, Michel; Rousseau, Roger; Raugei, Simone (2014-01-03). "Computing Free Energy Landscapes: Application to Ni-based Electrocatalysts with Pendant Amines for H 2 Production and Oxidation". ACS Catalysis (به انگلیسی). 4 (1): 229–242. doi:10.1021/cs401104w. ISSN 2155-5435.
- ↑ Ballard, Andrew J.; Das, Ritankar; Martiniani, Stefano; Mehta, Dhagash; Sagun, Levent; Stevenson, Jacob D.; Wales, David J. (2017). "Energy landscapes for machine learning". Physical Chemistry Chemical Physics (به انگلیسی). 19 (20): 12585–12603. doi:10.1039/C7CP01108C. ISSN 1463-9076.
- ↑ Repulsive potential-energy surface in Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Compiled by A. D. McNaught and A. Wilkinson. Blackwell Scientific Publications, Oxford (1997)
- ↑ Attractive potential-energy surface in Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Compiled by A. D. McNaught and A. Wilkinson. Blackwell Scientific Publications, Oxford (1997)