Timanttirakenne

Timanttirakenne on kiderakenne, jossa jokaisen atomin lähimpinä naapureina on neljä atomia sijoittuneina tätä ympäröivän säännöllisen tetraedrin kärkiin. Rakenteen nimi johtuu siitä, että timantissa hiiliatomit ovat sijoittuneet toisiinsa nähden tällä tavalla. Samalla tavalla kiteytyvät eräät muutkin jaksollisen järjestelmän 14. ryhmän eli hiiliryhmän alkuaineet: puolijohteina tunnetut pii ja germanium sekä niiden seokset, sekä myös tina esiintyessään harmaana eli α-tinana. Sitä vastoin samaan ryhmään kuuluvalla lyijyllä ei tällaista kiderakennetta esiinny.[1]
Kiteen rakenne
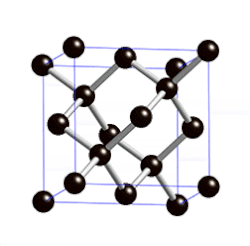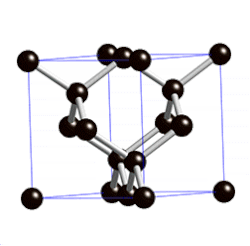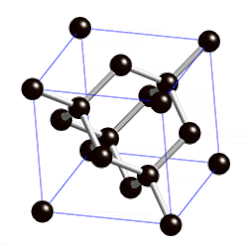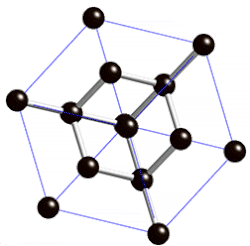
[muokkaa | muokkaa wikitekstiä]Timanttirakenne voidaan käsittää pintakeskisen kuutiollisen (fcc)-rakenteen muunnokseksi. Se muodostuu kuutiomaisista yksikkökopeista siten, että atomien ytimet sijaitsevat kuution kärkipisteissä, kuution jokaisen sivutahkon keskipisteissä sekä neljä atomia kuution sisällä sen avaruuslävistäjien varrella, tämän lävistäjän pituuden neljäsosan etäisyydellä kuution kärjistä. Täten jokaisella atomilla on neljä lähintä naapuriatomia, joihin se on sitoutunut kovalenttisesti.[2]
Timanttirakenteinen kide kokonaisuudessaan ei muodosta Bravais'n hilaa, sillä vaikka kaikki atomit ovatkin samalla tavalla neljän muun atomin ympäröimiä, nämä eivät kaikilla atomeilla ole samoin päin orientoituneina. Atomit voidaan kuitenkin ajatella jaetuksi kahteen ryhmään, joista toisen muodostavat kuution kärjissä ja sivutahkojen keskipisteissä olevat, toisen taas kuution sisällä olevat atomit. Nämä kummatkin erikseen muodostavat täysin pintakeskisen kuutiollisen kiteen kaltaisen Bravais'n hilan.[2]
Timanttirakenteessa atomit eivät muodosta tiiveintä pakkausta. Mikäli ajatellaan atomit palloiksi, joiden säde on puolet kahden lähimpänä toisiaan sijaitsevan atomin ytimien etäisyyksistä niin, että ne eivät osittainkaan ole päällekkäin, niiden osuus kiteen viemästä tilasta on ,[3]. Tämä on selvästi pienempi kuin pintakeskisessä kuutiollisessa hilassa, jossa vastaava suhde on .
Jos yksikkökopin yhden kärkipisteen ajatellaan sijaitsevan origossa ja pituusyksikkönä käytetään yksikkökopin muodostavan kuution särmää eli kiteen hilavakiota, niin yksikkökopissa olevien atomien ytimet sijaitsevat pisteissä (0, 0, 0), (1/2, 1/2, 0), (0, 1/2, 1/2), (1/2, 0, 1/2), (1/4, 1/4, 1/4), (1/4, 3/4, 3/4), (3/4, 1/4, 3/4) ja (3/4, 3/4, 1/4). Muissa yksikkökopeissa atomien ytimet ovat niissä pisteissä, joiden koordinaatit saadaan lisäämällä edellä mainittujen pisteiden koordinaatteihin mielivaltaisia kokonaislukuja.
Timanttirakenteessa kahden lähimpänä toisiaan sijaitsevan atomin etäisyyden eli sidospituuden suhde kuution sivun pituuteen eli hilavakioon on . Niinpä esimerkiksi timantin hilavakio on 356,7 pikometriä[4] ja sidospituus 0,43 · 356,7 = 154 pm.[1]. Vastaavasti piin ja germaniumin hilavakiot ovat 543,0 pm ja 565,8 pm[4] ja sidospituudet näin ollen 235 pm ja 245 pm.
Sinkkivälkkeen rakenne
[muokkaa | muokkaa wikitekstiä]Timanttirakennetta muistuttaa myös eräiden yhdisteiden kuten sinkkivälkkeen (ZnS) kiderakenne. Siinä on kuitenkin kahdenlaisia atomeja siten, että riippuen siitä, mikä kohta kiteessä valitaan lähtökohdaksi, joko sinkkiatomit ovat kuution kärkipisteissä ja sivutahkojen keskipisteissä, rikkiatomit taas kuutioiden sisällä, tai päinvastoin. Vastaavanlainen kiderakenne on myös useilla sellaisilla yhdisteillä, jonka muodostavat jaksollisen järjestelmän 13. ryhmän eli booriryhmän ja 15. ryhmän eli typpiryhmän alkuaineet, esimerkiksi puolijohteena tunnetulla galliumarsenidilla (GaAs).[2]
Lähteet
[muokkaa | muokkaa wikitekstiä]- ↑ a b Antti Kivinen, Osmo Mäkitie: Kemia, 5. painos, s. 324–325. Otava, 1988. ISBN 951-1-10136-6
- ↑ a b c J. E. Hall: Solid State Physics, s. 38–40. John Wiley & Sons Ltd, 1979. ISBN 0-471-34281-5
- ↑ The Science and Engineering of Materials, s. 82. Cengage Learning, 2006. ISBN 978-0534553968
- ↑ a b Esko Valtanen: Fysiikan taulukkokirja. Genesis-kirjat, 2007. ISBN 978-952-9867-26-4


