Ertugliflozine
| Ertugliflozine | |
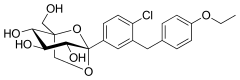
| |
| Identification | |
|---|---|
| Nom systématique | (1S,2S,3S,4R,5S)-5-[4-chloro-3-(4-éthoxybenzyl)phényl]-1-(hydroxyméthyl)-6,8-dioxabicyclo[3.2.1]octane-2,3,4-triol |
| Synonymes |
Steglatro |
| No CAS | |
| No ECHA | 100.237.989 |
| Code ATC | |
| DrugBank | DB11827 |
| PubChem | 44814423 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C22H25ClO7 |
| Masse molaire[1] | 436,883 ± 0,023 g/mol C 60,48 %, H 5,77 %, Cl 8,11 %, O 25,64 %, |
| Précautions | |
| SGH | |
| H314, H318, P260, P264, P280, P310, P321, P363, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P405 et P501 |
|
| Données pharmacocinétiques | |
| Biodisponibilité | 70-90% |
| Liaison protéique | 94-96% |
| Métabolisme | hépatique |
| Demi-vie d’élim. | 11-17 heures |
| Excrétion |
41% faeces, 50% urine |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'ertugliflozine (nom commercial Steglatro) est un médicament destiné au traitement du diabète de type 2. Aux États-Unis, il a été approuvé par la Food and Drug Administration pour une utilisation en monothérapie et en association à dose fixe avec la sitagliptine ou la metformine[2]. L'agence européenne des médicaments lui a accordé en mars 2018 une AMM au bénéfice du laboratoire Merck Sharp & Dohme, sous forme de comprimés pelliculés dosés à 5 et 15 mg[3]. À partir d'une cohorte de patients atteints d'athérosclérose et de diabète type II, l'ertugliflozine ne provoque pas plus d'effets indésirables graves qu'un placebo[4].
Les effets secondaires les plus courants sont des infections fongiques du vagin et d'autres infections du système reproducteur féminin[5].
L'ertugliflozine est un inhibiteur du cotransporteur sodium/glucose 2 (SGLT2)[6],[5]. Elle appartient à la classe des gliflozines.
Quatre associations fixes de ertugliflozine et de metformine sont disponibles en Europe sous le nom de spécialité Segluromet, commercialisée par Merck Sharp & Dohme (EMEA/H/C/004314). Deux associations fixes ertugliflozine/sitagliptine sont également commercialisés en Europe, toujours par Merck Sharp & Dohme, sous le nom de spécialité de Steglujan (EMEA/H/C/004313 - IG/1157)[7],[8],[9],[10].
Pharmacologie
[modifier | modifier le code]Métabolisme
[modifier | modifier le code]Après administration orale, l'ertugliflozine est presque complètement absorbée par l'intestin et ne subit aucun effet de premier passage significatif . La concentrations maximale plasmatiques est atteinte après une heure. Dans le sang circulant 93,6% du médicament est lié aux protéines plasmatiques . L'ertugliflocine est principalement métabolisée en glucuronides par les enzymes UGT1A9 et UGT2B7 . Les enzymes du cytochrome P450 ne jouent qu'un rôle mineur dans son métabolisme[3],[6].
La demi-vie d'élimination est estimée à 17 heures. 40,9% sont éliminés par les fèces (33,8% sous forme inchangée et 7,1% sous forme de métabolites) et 50,2% par voie urinaire (1,5% inchangé et 48,7% sous forme de métabolites). La proportion de substance inchangée dans les fécès est due probablement à un retour des métabolites vers la substance d'origine (réaction d'hydrolyse)[3],[6].
Références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « FDA Approves SGLT2 Inhibitor Ertugliflozin for Type 2 Diabetes », MedScape
- « Steglatro: EPAR – Product Information », European Medicines Agency,
- Cannon, Pratley, Dagogo-Jack et Mancuso, « Cardiovascular Outcomes with Ertugliflozin in Type 2 Diabetes », New England Journal of Medicine, (PMID 32966714, DOI 10.1056/NEJMoa2004967)
- « Steglatro EPAR », European Medicines Agency (EMA) (consulté le )
- « Steglatro- ertugliflozin tablet, film coated », DailyMed, (consulté le )
- « Segluromet- ertugliflozin and metformin hydrochloride tablet, film coated », DailyMed, (consulté le )
- « Segluromet EPAR », European Medicines Agency (EMA) (consulté le )
- « Steglujan- ertugliflozin and sitagliptin tablet, film coated », DailyMed, (consulté le )
- « Steglujan EPAR », European Medicines Agency (EMA) (consulté le )
