Imidure de lithium
| Imidure de lithium | |
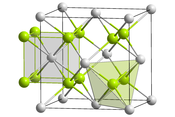 __ Li+ __ NH2− Structure cristalline de l'imidure de lithium  |
|
| Molécule d'imidure de lithium | |
| Identification | |
|---|---|
| No CAS | |
| Propriétés chimiques | |
| Formule | HLi2N |
| Masse molaire[1] | 28,897 ± 0,004 g/mol H 3,49 %, Li 48,04 %, N 48,47 %, |
| Propriétés physiques | |
| Masse volumique | 1,48 g·cm-3[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'imidure de lithium est un composé chimique de formule Li2NH. Il se présente comme un solide blanc qui peut être obtenu en faisant réagir de l'amidure de lithium LiNH2 avec de l'hydrure de lithium LiH[3] sous atmosphère d'argon :
L'imidure de lithium est photosensible et peut connaître une dismutation pour donner du nitrure de lithium Li3N, d'une couleur rouge caractéristique :
On pense que l'imidure de lithium cristallise avec une structure cubique à faces centrées dans le groupe d'espace Fm3m (no 225) avec une liaison N–H de l'ordre de 82 pm et un angle H–N–H de 109,5°, ce qui lui confère une structure semblable à celle de l'amidure de lithium[4],[5].
L'imidure de lithium est une substance très basique qui peut déprotoner des acides extrêmement faibles comme le méthane CH4 et l'ammoniac NH3. Ceci provient de la charge électrique négative localisée sur l'atome d'azote, porteur de deux charges formelles. Il peut être utilisé en chimie organométallique et fait l'objet de recherches comme matériau pour stockage de l'hydrogène[3].
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (de) Georg Brauer, en collaboration avec Marianne Baudler, Handbuch der Präparativen Anorganischen Chemie, 3e éd. révisée, vol. I, 1975, p. 451. (ISBN 3-432-02328-6)
- (en) Takayuki Ichikawa, Nobuko Hanada, Shigehito Isobe, Haiyan Leng et Hironobu Fujii, « Mechanism of Novel Reaction from LiNH2 and LiH to Li2NH and H2 as a Promising Hydrogen Storage System », The Journal of Physical Chemistry B, vol. 108, no 23, , p. 7887-7892 (DOI 10.1021/jp049968y, lire en ligne)
- (en) Kenji Ohoyama, Yuko Nakamori, Shin-ichi Orimo et Kazuyoshi Yamada, « Revised Crystal Structure Model of Li2NH by Neutron Powder Diffraction », Journal of the Physical Society of Japan, vol. 74, no 1, , p. 483-487 (DOI 10.1143/JPSJ.74.483, Bibcode 2005JPSJ...74..483O, arXiv 0406025, lire en ligne)
- (en) T. Noritake, H. Nozaki, M. Aoki, S. Towata, G. Kitahara, Y. Nakamori et S. Orimo, « Crystal structure and charge density analysis of Li2NH by synchrotron X-ray diffraction », Journal of Alloys and Compounds, vol. 393, nos 1-2, , p. 264-268 (DOI 10.1016/j.jallcom.2004.09.063, lire en ligne)