Rétrosynthèse
La rétrosynthèse ou analyse rétrosynthétique est une technique de résolution de problèmes dans la planification de synthèses organiques. La rétrosynthèse consiste à décomposer une molécule d'intérêt, souvent complexe, en un ensemble de précurseurs plus simples, sans hypothèse a priori sur les composés de départ qui seront utilisés.
Ce processus est itéré sur les précurseurs eux-mêmes, qui sont à leur tour décomposés, jusqu'à ce qu'on aboutisse à des molécules disponibles commercialement.
Ce concept a été formalisé par E. J. Corey dans son ouvrage The Logic of Chemical Synthesis[1],[2],[3].
L'analyse rétrosynthétique est particulièrement utile pour le design de synthèses totales, en permettant une décomposition rationnelle de la structure chimique à atteindre, que l'on réduit à des éléments plus simples. Dans la plupart des cas, il existe plusieurs voies de synthèse possibles. La rétrosynthèse permet d'identifier ces différentes voies et de les comparer entre elles en termes de faisabilité et de complexité[4]. Il existe des outils chémoinformatiques d'aide à la rétrosynthèse[5], ils s'appuient en général sur des bases de données de produits disponibles commercialement pour assister le processus.
Exemple
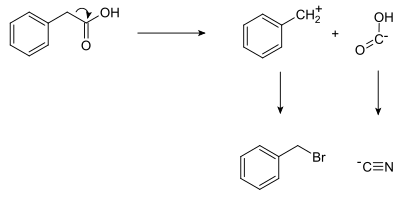
[modifier | modifier le code]Voici un exemple simple illustrant le concept de rétrosynthèse de l'acide phénylacétique.
La molécule cible est décomposée en deux blocs ou synthons : un groupe nucléophile -COOH et un groupe électrophile PhCH2+ (les deux synthons n'existent pas en réalité). On fait réagir des équivalents synthétiques correspondant aux synthons pour produire le produit désiré. Dans ce cas, l'anion cyanure est l'équivalent synthétique du synthon -COOH, tandis que le bromure de benzyle est l'équivalent synthétique du synthon benzyle.
Liste de logiciels de rétrosynthèse
[modifier | modifier le code]Il existe une liste assez importante de différents logiciels de synthèse organique assistée par ordinateur (computer-assisted organic synthesis, CAOS) :
- Spaya[6], reposant sur sa technologie d’intelligence artificielle spécifique dédiée à la rétrosynthèse[7], propriétaire et accessible gratuitement en ligne, développé par l'entreprise française Iktos ;
- Organic Synthesis Exploration Tool (OSET), logiciel open source, développement à l'arrêt[8] ;
- Synthia[9], logiciel propriétaire développé par l'entreprise allemande Merck.
Références
[modifier | modifier le code]- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Retrosynthetic analysis » (voir la liste des auteurs).
- E.J. Corey et X-M. Cheng, The Logic of Chemical Synthesis, New York, Wiley, (ISBN 0-471-11594-0)
- E.J. Corey, « Retrosynthetic Thinking - Essentials and Examples », Chem. Soc. Rev., vol. 17, , p. 111–133 (DOI 10.1039/CS9881700111).
- E.J. Corey, « The Logic of Chemical Synthesis: Multistep Synthesis of Complex Carbogenic Molecules (Nobel Lecture) », Angewandte Chemie International Edition in English, vol. 30, no 5, , p. 455–465 (DOI 10.1002/anie.199104553, lire en ligne [Reprint]).
- James Law, Zsolt Zsoldos, Aniko Simon et Darryl Reid, « Route Designer: A Retrosynthetic Analysis Tool Utilizing Automated Retrosynthetic Rule Generation », Journal of Chemical Information and Modeling, vol. 49, no 3, , p. 593–602 (ISSN 1549-9596, DOI 10.1021/ci800228y, lire en ligne, consulté le ).
- Anders Bøgevig, Hans-Jürgen Federsel, Fernando Huerta et Michael G. Hutchings, « Route Design in the 21st Century: The ICSYNTH Software Tool as an Idea Generator for Synthesis Prediction », Organic Process Research & Development, vol. 19, no 2, , p. 357–368 (ISSN 1083-6160, DOI 10.1021/op500373e, lire en ligne, consulté le ).
- Spaya.
- « SRI International », sur Medicen, (consulté le ).
- « SAL- Other Scientific Fields - Chemistry, Biology & Related - OSET », sur sai.msu.su (consulté le )
- Synthia.
Voir aussi
[modifier | modifier le code]Articles connexes
[modifier | modifier le code]Bibliographie
[modifier | modifier le code]- Daniel Sparfel, Chimie organique : Synthèse organique - La rétrosynthèse, les déconnexions, méthodologie - Cours et exercices corrigés, 2015, édition Ellipses (ISBN 9782340-009158).