Yersiniabactine
| Yersiniabactine | |
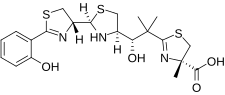 Structure de la yersiniabactine |
|
| Identification | |
|---|---|
| Nom UICPA | acide (4S)-2-[(1S)-1-hydroxy-2-méthyl-1-[(4R)-2-[(2E,4R)-2-(6-oxocyclohexa-2,4-dién-1-ylidène)-1,3-thiazolidin-4-yl]-1,3-thiazolidin-4-yl]propan-2-yl]-4-méthyl-5H-1,3-thiazole-4-carboxylique |
| PubChem | 5462519 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C21H27N3O4S3 |
| Masse molaire[1] | 481,652 ± 0,035 g/mol C 52,37 %, H 5,65 %, N 8,72 %, O 13,29 %, S 19,97 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La yersiniabactine est un sidérophore produit par des bactéries pathogènes telles que Yersinia pestis, Yersinia pseudotuberculosis, Yersinia enterocolitica ainsi que chez certaines souches d’Escherichia coli. Les sidérophores sont des composés de faible masse moléculaire ayant une affinité très élevée pour le fer(III) et sont des facteurs de virulence importants des bactéries pathogènes.
Le fer est un élément essentiel à certains processus biochimiques critiques tels que la respiration cellulaire et la réplication de l'ADN. Il est présent chez les cellules hôtes sous forme chélatée par des protéines telles que la ferritine et la lactoferrine. Les agents infectieux utilisent alors des molécules ayant une affinité encore plus élevée pour le fer ferrique afin de s'approprier le fer de leur hôte[2].
Les atomes de fer(III) se lient chacun à une molécule de yersiniabactine en formant un complexe coordonné à trois doublets d'azote et trois atomes d'oxygène chargés négativement selon une géométrie octaédrique déformée[3]. La constante de dissociation de ce complexe vaut K = 4 × 1036[2]. C'est cette affinité élevée pour le fer qui permet à ces bactéries de se multiplier chez leur hôte pour y causer des infections systémiques. Le complexe yersiniabactine-Fe3+ reconnaît le récepteur membranaire TonB de la membrane externe de la bactérie et est transféré dans le cytosol à l'aide de protéines membranaires[4].
Lorsqu'elles sont dépourvues de yersiniabactine, ces bactéries du genre Yersinia, responsables notamment de la peste bubonique, ne provoquent que des infections localisées de faible intensité.
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Robert D. Perry, Paul B. Balbo, Heather A. Jones, Jacqueline D. Fetherston et Edward DeMoll, « Yersiniabactin from Yersinia pestis: biochemical characterization of the siderophore and its role in iron transport and regulation », Microbiology, vol. 145, no 5, , p. 1181-1190 (lire en ligne) DOI 10.1099/13500872-145-5-1181
- (en) M. Clarke Miller, Sean Parkin, Jacqueline D. Fetherston, Robert D. Perry et Edward DeMoll, « Crystal structure of ferric-yersiniabactin, a virulence factor of Yersinia pestis », Journal of Inorganic Biochemistry, vol. 100, no 9, , p. 1495-1500 (lire en ligne) DOI 10.1016/j.jinorgbio.2006.04.007
- (en) Robert D. Perry, Jessica Shah, Scott W. Bearden, Jan M. Thompson et Jacqueline D. Fetherston, « Yersinia pestis TonB: Role in Iron, Heme, and Hemoprotein Utilization », Infection and Immunity, vol. 71, no 7, , p. 4159-4162 (lire en ligne) DOI 10.1128/IAI.71.7.4159-4162.2003