Proteína de replicación A
| Proteína de replicación A | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| (heterotrímero) | |||||||||||||
 | |||||||||||||
| Función | unión ao ADN danado, unión a ADN monocatenario | ||||||||||||
| |||||||||||||
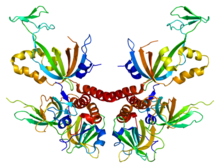
A proteína de replicación A (RPA) é a principal proteína que se une ao ADN monocatenario (ssDNA) nas células eucariotas.[1][2] In vitro, a RPA mostra unha moita maior afinidade polo ADN monocatenario que polo ARN ou polo ADN bicatenario.[3] A RPA é necesaria para a replicación do ADN, a recombinación xenética e os procesos de reparación como a reparación por escisión de nucleótidos e a recombinación homóloga.[2][4] Tamén exerce unha función na resposta aos danos no ADN.[4]
Estrutura
[editar | editar a fonte]A RPA é un heterotrímero composto polas subunidades RPA1 (RPA70, subunidade de 70kDa), RPA2 (RPA32, subunidade de 32kDa) e RPA3 (RPA14, subunidade de 14kDa). As tres subunidades da RPA conteñen seis pregamentos OB (de unión a oligonucleótidos/oligosacáridos), con dominios de unión ao ADN (DBD) designados como DBDs A-F, que unen a RPA ao ADN monocatenario.[2][3]
Os DBDs A, B, C e F están localizados na RPA1, o DBD D está situado na RPA2 e o DBD E na RPA3.[4] Os DBDs C, D e E constitúen o núcleo de trimerización da proteína con rexións enlazadoras flexibles que os conectan.[4] Debido a estas rexións enlazadoras flexibles, a RPA considérase moi flexible e isto favorece a unión dinámica que a RPA pode conseguir. Debido a esta dinámica de unión, a RPA tamén pode adoptar diferentes conformacións e pode abranguer un variado número de nucleótidos.[4]
Os DBDs A, B, C e D son os sitios que están implicados na unión ao ADN monocatenario.[5] As interaccións proteína-proteína entre a RPA e outras proteínas ocorren no N-terminal da RPA1, especificamente no DBD F, xunto co C-terminal da RPA2.[5] A fosforilación da RPA ten lugar no N-terminal da RPA2.[5]
A RPA comparte moitas características co heterotrímero complexo CST, aínda que a RPA ten unha estequiometría máis uniforme 1:1:1.[6]
Funcións
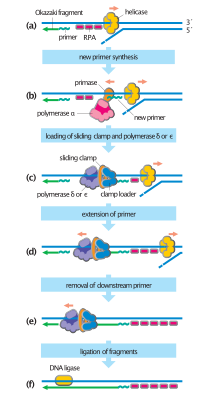
[editar | editar a fonte]Durante a replicación do ADN, a RPA impide que o ADN bicatenario se enrole de novo sobre si mesmo ou forme estruturas secundarias. Tamén axuda a protexer o ADN monocatenario do ataque das endonucleases.[2] Isto mantén o ADN desenrolado para que a polimerase o replique. A RPA tamén se une ao ADN monocatenario durante a fase inicial da recombinación homóloga, un importante proceso na reparación do ADN e na profase I da meiose.
A hipersensibilidade a axentes que danan o ADN pode ser causada por mutacións no xene RPA.[7] Igual que o seu papel na replicación do ADN, isto evita que o ADN monocatenario se una consigo mesmo (en zonas autocomplementarias) para que o filamento de nucleoproteína resultante poida unirse a Rad51 e aos seus cofactores.[7]
A RPA tamén se une ao ADN durante o proceso de reparación por escisión de nucleótidos. Esta unión estabiliza o complexo de reparación durante o proceso de reparación. Un homólogo bacteriano denomínase proteína SSB, que exerce a mesma función pero non ten homoloxía de secuencias.
Notas
[editar | editar a fonte]- ↑ Wold MS (1997). "Replication protein A: a heterotrimeric, single-stranded DNA-binding protein required for eukaryotic DNA metabolism". Annual Review of Biochemistry 66 (1): 61–92. PMID 9242902. doi:10.1146/annurev.biochem.66.1.61.
- ↑ 2,0 2,1 2,2 2,3 Chen R, Wold MS (decembro de 2014). "Replication protein A: single-stranded DNA's first responder: dynamic DNA-interactions allow replication protein A to direct single-strand DNA intermediates into different pathways for synthesis or repair". BioEssays 36 (12): 1156–1161. PMC 4629251. PMID 25171654. doi:10.1002/bies.201400107.
- ↑ 3,0 3,1 Flynn RL, Zou L (agosto de 2010). "Oligonucleotide/oligosaccharide-binding fold proteins: a growing family of genome guardians". Critical Reviews in Biochemistry and Molecular Biology 45 (4): 266–275. PMC 2906097. PMID 20515430. doi:10.3109/10409238.2010.488216.
- ↑ 4,0 4,1 4,2 4,3 4,4 Caldwell CC, Spies M (outubro de 2020). "Dynamic elements of replication protein A at the crossroads of DNA replication, recombination, and repair". Critical Reviews in Biochemistry and Molecular Biology 55 (5): 482–507. PMC 7821911. PMID 32856505. doi:10.1080/10409238.2020.1813070.
- ↑ 5,0 5,1 5,2 Dueva R, Iliakis G (setembro de 2020). "Replication protein A: a multifunctional protein with roles in DNA replication, repair and beyond". NAR Cancer 2 (3): zcaa022. PMC 8210275. PMID 34316690. doi:10.1093/narcan/zcaa022.
- ↑ Lue NF, Zhou R, Chico L, Mao N, Steinberg-Neifach O, Ha T (2013). "The telomere capping complex CST has an unusual stoichiometry, makes multipartite interaction with G-Tails, and unfolds higher-order G-tail structures". PLOS Genetics 9 (1): e1003145. PMC 3536697. PMID 23300477. doi:10.1371/journal.pgen.1003145.
- ↑ 7,0 7,1 Li X, Heyer WD (xaneiro de 2008). "Homologous recombination in DNA repair and DNA damage tolerance". Cell Research 18 (1): 99–113. PMC 3087377. PMID 18166982. doi:10.1038/cr.2008.1.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]