Selección clonal
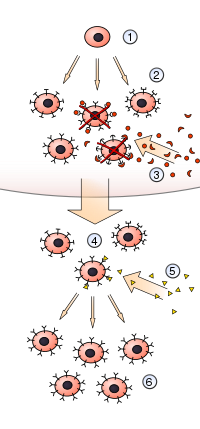
A teoría da selección clonal (ou, inicialmente, hipótese da selección clonal) converteuse no modelo máis amplamente aceptado para explicar como o sistema inmunitario responde ás infeccións e como certos tipos de linfocitos B e T son seleccionados para que destrúan antíxenos estraños específicos que invaden o corpo.[1]
Os catro principios da teoría da selección clonal
[editar | editar a fonte]- Cada linfocito leva un só tipo de receptor para antíxenos na súa membrana cunha especificidade única (creada pola recombinación V(D)J).
- Para que se active a célula requírese que o receptor se una ao antíxeno.
- As células efectoras diferenciadas derivadas dun linfocito activado levarán receptores de especificidade idéntica á da célula parental.
- Os linfocitos que leven receptores para moléculas propias serán eliminados nas fases iniciais.
Resposta monoclonal e policlonal
[editar | editar a fonte]A teoría pode servir de base para explicar as respostas monoclonais e policlonais. O sistema inmunitario orixina millóns de linfocitos cada un cun receptor diferente, que será específico para un antíxeno. Cando un antíxeno estraño entra no corpo activará só o clon de linfocitos que teña o receptor específico para el (resposta monoclonal), o cal proliferará, orixinando moitas células iguais, que realizarán a resposta. Porén, normalmente, dos millóns de linfocitos que hai no corpo, hai varios que teñen receptores que poden unirse a un determinante antixénico do antíxeno; estes receptores non son exactamente iguais, pero si moi parecidos e cada un se unirá ao antíxeno cunha afinidade un pouco distinta, polo que se activarán varios clons (resposta policlonal a un determinante)[2], que proliferarán e darán lugar a unha resposta, na que producirán anticorpos parecidos (ver tamén maduración da afinidade); de todos modos, só son unha diminuta fracción dos millóns de clons de linfocitos que hai, a inmensa maioría non reactivos para ese antíxeno. Ademais desta acción sobre un só determinante, un antíxeno adoita a ser unha molécula grande, que ten varios determinantes antixénicos ou epitopos distintos, polo que para cada determinante se activarán distintos clons de linfocitos e se producirán anticorpos diferentes para cada determinante (resposta policlonal a varios determinantes dun antíxeno).
Memoria inmunolóxica
[editar | editar a fonte]Tamén se pode explicar a memoria inmunolóxica por medio da selección de clons linfocitarios. Cando se activa un linfocito por un antíxeno prodúcense dous clons de linfocitos, un de vida curta, que actúa inmediatamente contra a infección, e outro de vida longa, que non actúa pero que pode vivir moito tempo no corpo, gardando unha memoria inmunolóxica dese antíxeno. Estes últimos chámanse linfocitos con memoria e garanten a inmunidade contra posteriores infeccións por ese mesmo antíxeno, xa que producirán unha resposta rápida e efectiva se o antíxeno infecta outra vez.
Tolerancia inmunolóxica
[editar | editar a fonte]A tolerancia inmunolóxica foi explicada utilizando os principios da teoría da selección clonal. Os linfocitos que teñen a capacidade de reaccionar con antíxenos propios son eliminados durante as fases iniciais do desenvolvemento e só sobreviven os clons que son tolerantes a antíxenos propios.
Historia
[editar | editar a fonte]Traballos iniciais
[editar | editar a fonte]En 1954, o inmunólogo danés Niels Jerne presentou a hipótese de que existía no corpo un enorme conxunto de linfocitos distintos antes de calquera infección. A entrada do antíxeno no corpo selecciona só un tipo de linfocitos, que será o que teña un receptor que sexa específico para ese antíxeno, e producirá un anticorpo (no caso das células B) específico para o antíxeno, que o acabará por destruír.[3]
Esta selección do linfocito fará que se reproduza orixinando un clon numeroso de linfocitos iguais, que asegure que vai haber suficiente produción dese anticorpo para neutralizar a infección.
Traballos posteriores
[editar | editar a fonte]O inmunólogo australiano Frank Macfarlane Burnet coas achegas de David W. Talmage traballou neste modelo, e foi o primeiro en chamarlle "teoría da selección clonal". Burnet explicou a memoria inmunolóxica como a clonación de dous tipos de linfocitos. Un clon actúa inmediatamente combatendo a infección mentres que o outro non actúa inicialmente pero ten maior duración, polo que permanece no sistema inmunitario durante moito tempo, o que ten como resultado unha inmunidade duradeira contra ese antíxeno. En 1958, Gustav Nossal e Joshua Lederberg demostraron que unha célula B sempre produce un só tipo de anticorpo, o cal era a primeira evidencia da teoría da selección clonal.[4]
O premio Nobel xaponés Susumu Tonegawa explicou como os linfocitos podían orixinar a enorme diversidade de anticorpos e receptores necesaria cunha cantidade limitada de ADN, grazas ao seus traballos da década de 1970 sobre a recombinación somática nos xenes das inmunoglobulinas. Durante o desenvolvemento do linfocito prodúcense rearranxos xenéticos que poden orixinar esa gran diversidade a partir dun conxunto relativamente pequeno de xenes e segmentos xénicos.
Teorías apoiadas pola selección clonal
[editar | editar a fonte]Burnet e Peter Medawar traballaron xuntos na comprensión da tolerancia inmunolóxica, un fenómeno tamén explicado pola selección clonal. Esta consiste na capacidade do organismo de tolerar certos antíxenos (xeralmente os antíxenos propios). Observouse que a introdución de células ao comezo do desenvolvemento do organismo (embrión) non producía unha resposta inmune. Do enorme número de linfocitos que inicialmente hai no organismo, algúns son reactivos contra antíxenos propios e outros non (tolerantes). Porén, só as células que son tolerantes aos antíxenos propios sobrevivirán ás fases embrionarias. Se nas fases embrionarias introducimos un tecido non propio, o organismo considerará ese tecido como propio e eliminará os linfocitos reactivos contra el.
En 1959 Burnet propuxo que en certas circunstancias, podía transplantarse con éxito tecidos en receptores alleos. Este traballo levou a unha maior comprensión do sistema inmunitario e tamén a grandes avances no transplante de tecidos. Burnet e Medawar compartiron o premio Nobel de medicina en 1960.
En 1974 Niels Kai Jerne propuxo que o sistema inmunitario funciona como unha rede, e está regulado por medio de interaccións entre os receptores dos linfocitos e as moléculas que segregan. A teoría da rede inmune está baseada firmemente no concepto da selección clonal. Jerne gañou o premio Nobel de medicina en 1984 principalmente pola súa contribución a esta teoría.
Notas
[editar | editar a fonte]- ↑ Rajewsky, Klaus (1996). "Clonal selection and learning in the antibody system". Nature 381 (6585): 751–758. ISSN 0028-0836. doi:10.1038/381751a0.
- ↑ Bruce Alberts et al. Biología Molecular de la Célula. Omega. 1986. Páxina 1027. ISBN 84-282-0752-6.
- ↑ Burnet, F. M. (1976). "A Modification of Jerne's Theory of Antibody Production using the Concept of Clonal Selection". CA: A Cancer Journal for Clinicians 26 (2): 119–121. ISSN 0007-9235. doi:10.3322/canjclin.26.2.119.
- ↑ Nossal, G. J. V. & Lederberg, J. 1958. Antibody production by single cells. Nature 181:1419-1420
- "Biology in Context - The Spectrum of Life" Authors, Peter Aubusson, Eileen Kennedy.
- Forsdyke, D.R. 1995. The Origins of the Clonal Selection Theory of Immunity FASEB. Journal 9:164-66
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- Animación sobre a selección clonal Arquivado 06 de xullo de 2011 en Wayback Machine. do instituto Walter & Elisa Hall.