Vilosidade coriónica

As vilosidades coriónicas ou villi coriónicos (en singular villus) son prolongacións que saen do tecido do corion embrionario e se estenden pola parede uterina proporcionando unha área de contacto aumentada co sangue materno.
Son elementos esenciais no embarazo desde un punto de vista histomorfolóxico e funcional e son, por definición, un produto da concepción. Ramas das arterias umbilicais levan o sangue embrionario ás vilosidades. Despois de circular polos capilares das vilosidades, o sangue volve ao embrión a través da vea umbilical. Así, as vilosidades son parte do límite entre o sangue materno e fetal durante o embarazo e permiten o intercambio de substancias entre os dous sangues.
Estrutura
[editar | editar a fonte]

As vilosidades tamén se poden clasificar atendendo ás súas relacións con outras estruturas:
- Vilosidades flotantes, que flotan libremente no espazo interviloso. Mostran un epitelio de dúas capas que consta de citotrofoblastos cun sincitio por riba (sincitiotrofoblasto).
- Vilosidades de ancoraxe (con talo) que estabilizan a integridade mecánica da interface placentaria-maternal.
Desenvolvemento
[editar | editar a fonte]O corion experimenta unha rápida proliferación e forma numerosos procesos, as vilosidades coriónicas, que invaden e destrúen a decidua uterina e ao mesmo tempo absorben dela materiais nutritivos para o crecemento do embrión. Pasan por varios estadios, dependenedo da súa composición.
| Estadio | Descrición | Período de xestación | Contidos |
| Primarias | As vilosidades coriónicas son ao principio pequenas e non vasculares. | 13–15 días | soamente trofoblasto[1] |
| Secondarias | As vilosidades incrementan o seu tamaño e ramifícanse, mentres que o mesoderma crece dentro delas. | 16–21 días | trofoblasto e mesoderma[1] |
| Terciarias | Crecen ramas da arteria e vea umbilicais no mesoderma e dese xeito as vilosidades coriónicas quedan vascularizadas. | 17–22 días | trofoblasto, mesoderma e vasos sanguíneos[1] |
Ata aproximadamente o final do segundo mes de embarazo, as vilosidades cobren todo o corion e son case dun tamaño uniforme, mais despois desenvolvense de maneira desigual.
Microanatomía
[editar | editar a fonte]
A maior parte da masa das vilosidades consiste en tecido conectivo que contén vasos sanguíneos. A maioría das células do tecido nectivo das vilosidades son fibroblastos. Tamén están presentes macrófagos denominados células de Hofbauer.
Importancia clínica
[editar | editar a fonte]Uso para a diagnose prenatal
[editar | editar a fonte]En 1983 o biólogo italinao Giuseppe Simoni descubriu un novo método de diagnose prenatal no que se utilizaban as vilosidades coriónicas (ver biopsia de vilosidades coriónicas ou coriocentese, vilocentese).
Células nais
[editar | editar a fonte]As vilosidades coriónicas son unha rica fonte de células nais. O Biocell Center, unha empresa biotecnolóxica dirixida por Giuseppe Simoni, está estudando e probando estes tipos de células nais. As células nais coriónicas, igual que as células nais amnióticas, son células nais multipotentes de uso non polémico (non se dana o embrión).[2][3][4]
Infeccións
[editar | editar a fonte]Estudos recentes indican que as vilosidades coriónicas poden ser susceptibles ás infeccións bacterianas[5] e virais. Recentes descubrimentos indican que a bacteria Ureaplasma parvum (un micoplasma) pode infectar os tecidos das vilosidades coriónicas de mulleres preñadas, prexudicando ao resultado do embarazo.[6] Detectouse ADN do poliomavirus JC e o poliomavirus de células de Merkel nas vilosidades coriónicas de mulleres que sufriron abortos naturais.[7][8] Tamén se detectou ADN de poliomavirus BK nos mesmos tecidos pero en menor medida.[7]
Abortos naturais temperáns
[editar | editar a fonte]
Nos abortos naturais temperáns a presenza de vilosidades coriónicas nas expulsións vaxinais adoita ser a única confirmación definitiva de que houbo un embarazo intrauterino en vez dun embarazo ectópico.
Galería
[editar | editar a fonte]-
Micrografía que mostra vilosidades coriónicas a aumento medio. Tinguidura de hematoxilina-eosina.
-
Micrografía que mostra vilosidades coriónicas a moitos aumentos. Tinguidura de hematoxilina-eosina.
-
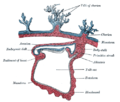
Corte a través do embrión.
-
Corte transversal dunha vilosidade corionica.
-
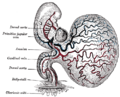
Embrión humano duns 28 días, con saco vitelino.
Notas
[editar | editar a fonte]- ↑ 1,0 1,1 1,2 Larsen, William J. : Human embryology. Sherman, Lawrence S.; Potter, S. Steven; Scott, William J. 3. ed.
- ↑ "European Biotech Company Biocell Center Opens First U.S. Facility for Preservation of Amniotic Stem Cells in Medford, Massachusetts | Reuters". 2009-10-22. Consultado o 2010-01-11.[Ligazón morta]
- ↑ "Europe's Biocell Center opens Medford office – Daily Business Update – The Boston Globe". 2009-10-22. Consultado o 2010-01-11.
- ↑ "The Ticker - BostonHerald.com". Arquivado dende o orixinal o 2012-09-21. Consultado o 2010-01-11.
- ↑ Contini C, Rotondo JC, Magagnoli F, Maritati M, Seraceni S, Graziano A (2019). "Investigation on silent bacterial infections in specimens from pregnant women affected by spontaneous miscarriage.". J Cell Physiol 34 (3): 433–440. PMID 30078192. doi:10.1002/jcp.26952.
- ↑ Contini C, Rotondo JC, Magagnoli F, Maritati M, Seraceni S, Graziano A, Poggi A, Capucci R, Vesce F, Tognon M, Martini F (2018). "Investigation on silent bacterial infections in specimens from pregnant women affected by spontaneous miscarriage.". J Cell Physiol 234 (1): 100–9107. PMID 30078192. doi:10.1002/jcp.26952.
- ↑ 7,0 7,1 Tagliapietra A, Rotondo JC, Bononi I, Mazzoni E, Magagnoli F, Maritati M (2019). "Footprints of BK and JC polyomaviruses in specimens from females affected by spontaneous abortion.". Hum Reprod 34 (3): 433–440. PMID 30590693. doi:10.1002/jcp.27490.
- ↑ Tagliapietra A, Rotondo JC, Bononi I, Mazzoni E, Magagnoli F, Maritati M (2020). "Droplet-digital PCR assay to detect Merkel cell polyomavirus sequences in chorionic villi from spontaneous abortion affected females". J Cell Physiol 235 (3): 1888–1894. PMID 31549405. doi:10.1002/jcp.29213.