FGF9
| FGF9 | |
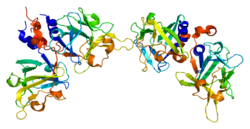 | |
| Azonosítók | |
| Jel | FGF9 |
| Entrez | 2254 |
| OMIM | 600921 |
| RefSeq | NM_002010 |
| UniProt | P31371 |
| PDB | 1G82 |
| Egyéb adatok | |
| Lokusz | 13. krom. q12.11 |
A gliaaktiváló faktor az FGF9 gén által kódolt fehérje.[1][2]
Funkció
[szerkesztés]A gén által kódolt fehérje a fibroblasztnövekedési faktor (FGF) családba tartozik. E család széles körben rendelkezik mitogén és sejttúlélési funkciókkal, és számos biológiai folyamatban, például az embrionális fejlődésben, a sejtnövekedésben, a morfogenezisben, a szövetregenerációban és a tumornövekedésben és -invázióban részt vesz. E fehérjét tenyésztett gliasejtek növekedését stimuláló szekrétumként izolálták. Az idegrendszerben e fehérjét főképp neuronok termelik, és fontos lehet a gliasejtek fejlődésében. A gén egérhomológjának expressziója függ a Sonic hedgehog (Shh)-jelzéstől. E homológgal nem rendelkező egérben hím–nőstény ivarfordulás történik, így feltehetően a herék embriogenezisében is fontos.[2] E gén fontos a nemi meghatározásban, a tüdő- és vázfejlődésben.
Nemi meghatározás
[szerkesztés]Az FGF9 fontos a hím nemi fejlődésben. Az FGF9 szerepe a nemi meghatározásban a bipotens gonádokban történő expresszióval kezdődik.[3] A SOX9 által aktiválva azzal előrecsatolási ciklust hoz létre, mindkét fehérje szintjét növelve. Pozitív visszacsatolási ciklust hoz létre, és inaktiválja a női Wnt4-jelzőutat.[3][4]
Tüdőfejlődés
[szerkesztés]A tüdőfejlődésben az FGF9-et a mezotélium és tüdőepitélium expresszálja, itt a mezenchimális proliferációt tartja fenn. Inaktivációja csökkenti az epitél elágazást.[5] A gestatio végére az így kifejlett tüdő nem tudja fenntartani az életet, prenatalis halált okozva.[5]
Vázfejlődés
[szerkesztés]E gén további biológiai szerepe a vázfejlődésben és -javításban van. Az FGF9 és FGF18 stimulálják a chondrocita-proliferációt.[6] FGF9-heterozigóta mutáns egerek csontjavulása sérülés után rosszabb volt, kisebb VEGF- és VEGFR2-expresszióval és oszteoklasztaktivitással.[6] E génnel kapcsolatos egyik betegség a több szinosztózisos szindróma (SYNS), egy ujjak és lábujjak fúziójával összefüggő betegség.[7] Az FGF9 gén 2. exonjának S99N misszenz mutációja a SYNS harmadik oka.[8] A noggin (NOG) és a növekedési differenciációs faktor 5 (GDF5) mutációi a SYNS másik két oka.[8] Az S99N mutáció sejtkommunikációs hibákat okoz, melyek a chondrogenezissel és az oszteogenezissel ütköznek, a fejlődés során ízületek egyesülését okozva.[8]
Túlexpressziója
[szerkesztés]Az FGF9 a fibroblaszt-növekedési faktorok (FGF) családjába, egy sejtkommunikációs fehérjecsaládba tartozik. E gén jelzi az embrionális őssejtek fejlődését és a nemi meghatározást. Az FGF9-expresszió fontos az epitél és stromalis sejtekből álló prosztata fejlődéséhez és szövetei homeosztázisának fenntartásához. Az FGF9 túlexpressziója a prosztata epitél sejtjeiben magas fokú prosztata-intraepitél neopláziát okoz, mely a prosztatarák prekurzora. Ezenkívül a túlexpresszió megzavarja a szöveti homeosztázist, és nagy metasztázis-valószínűséget okoz. A prosztata stromalis sejtjeiben lévő túlexpresszió a ráksejtekkel való kommunikációt segíti.[9]
A nem megfelelő FGF9-expresszió számos humán rákban onkogén, például petefészek-,[10] agy-, tüdő- és vastagbéltumorban.[11] A magas FGF9-expresszió a prosztata és a seminalis vezikulumok fúzióját, péniszprotrúziót és az epitél és stromalis részek hiperpláziáját okozza.[12] A hiperplázia a sejtek reprodukciójának növekedése miatti szövetnagyobbodás miatt gyakran a rák első szakasza.
Bár több tanulmány is igazolta az FGF9 túlexpressziója és a prosztatarák korrelációját, hogy ok-okozati kapcsolat van-e köztük, még nem ismert.[12]
Kölcsönhatások
[szerkesztés]Az FGF9 kölcsönhatásba lép a fibroblasztnövekedésifaktor-receptor 3-mal.[13][14]
Jegyzetek
[szerkesztés]- ↑ Miyamoto M, Naruo K, Seko C, Matsumoto S, Kondo T, Kurokawa T (1993. július 1.). „Molecular cloning of a novel cytokine cDNA encoding the ninth member of the fibroblast growth factor family, which has a unique secretion property”. Molecular and Cellular Biology 13 (7), 4251–9. o. DOI:10.1128/mcb.13.7.4251. PMID 8321227. PMC 359975.
- ↑ a b Entrez Gene: FGF9 fibroblast growth factor 9 (glia-activating factor)
- ↑ a b Sánchez L, Chaouiya C (2016. május 1.). „Primary sex determination of placental mammals: a modelling study uncovers dynamical developmental constraints in the formation of Sertoli and granulosa cells”. BMC Systems Biology 10 (1), 37. o. DOI:10.1186/s12918-016-0282-3. PMID 27229461. PMC 4880855.
- ↑ Kim Y, Kobayashi A, Sekido R, DiNapoli L, Brennan J, Chaboissier MC, Poulat F, Behringer RR, Lovell-Badge R, Capel B (2006. június 1.). „Fgf9 and Wnt4 act as antagonistic signals to regulate mammalian sex determination”. PLOS Biology 4 (6), e187. o. DOI:10.1371/journal.pbio.0040187. PMID 16700629. PMC 1463023.
- ↑ a b Yin Y, Wang F, Ornitz DM (2011. augusztus 1.). „Mesothelial- and epithelial-derived FGF9 have distinct functions in the regulation of lung development”. Development 138 (15), 3169–77. o. DOI:10.1242/dev.065110. PMID 21750028. PMC 3188607.
- ↑ a b Sivaraj KK, Adams RH (2016. augusztus 1.). „Blood vessel formation and function in bone”. Development 143 (15), 2706–15. o. DOI:10.1242/dev.136861. PMID 27486231.
- ↑ Multiple Synostoses Syndrome. Orphanet . (Hozzáférés: 2017. április 16.)
- ↑ a b c Wu XL, Gu MM, Huang L, Liu XS, Zhang HX, Ding XY, Xu JQ, Cui B, Wang L, Lu SY, Chen XY, Zhang HG, Huang W, Yuan WT, Yang JM, Gu Q, Fei J, Chen Z, Yuan ZM, Wang ZG (2009. július 1.). „Multiple synostoses syndrome is due to a missense mutation in exon 2 of FGF9 gene”. American Journal of Human Genetics 85 (1), 53–63. o. DOI:10.1016/j.ajhg.2009.06.007. PMID 19589401. PMC 2706969.
- ↑ Li ZG, Mathew P, Yang J, Starbuck MW, Zurita AJ, Liu J, Sikes C, Multani AS, Efstathiou E, Lopez A, Wang J, Fanning TV, Prieto VG, Kundra V, Vazquez ES, Troncoso P, Raymond AK, Logothetis CJ, Lin S-H, Maity S, Navone NM (2008. augusztus 1.). „Androgen receptor–negative human prostate cancer cells induce osteogenesis in mice through FGF9-mediated mechanisms”. J Clin Invest 118 (8), 2697–2710. o. DOI:10.1172/JCI33093. PMID 18618013. PMC 2447924. (Hozzáférés: 2023. december 27.)
- ↑ Bhattacharya R, Chaudhuri SR, Roy SS (2018. június 15.). „FGF9-induced ovarian cancer cell invasion involves VEGF-A/VEGFR2 augmentation by virtue of ETS1 upregulation and metabolic reprogramming”. J Cell Biochem. DOI:10.1002/jcb.26820. PMID 29904943. (Hozzáférés: 2023. december 27.)
- ↑ Li L, Zhang C, Li Y, Zhang Y, Lei Y (2020. május 15.). „DJ-1 promotes epithelial-to-mesenchymal transition via enhancing FGF9 expression in colorectal cancer”. Biol Open 9 (5), bio051680. o. DOI:10.1242/bio.051680. PMID 32366371. PMC 7325429. (Hozzáférés: 2023. december 27.)
- ↑ a b Huang Y, Jin C, Hamana T, Liu J, Wang C, An L, McKeehan WL, Wang F (2015. június 11.). „Overexpression of FGF9 in Prostate Epithelial Cells Augments Reactive Stroma Formation and Promotes Prostate Cancer Progression”. Int J Biol Sci, 948–960. o. DOI:10.7150/ijbs.12468. PMID 26157349. PMC 4495412. (Hozzáférés: 2023. december 27.)
- ↑ Santos-Ocampo S, Colvin JS, Chellaiah A, Ornitz DM (1996. január 1.). „Expression and biological activity of mouse fibroblast growth factor-9”. The Journal of Biological Chemistry 271 (3), 1726–31. o. DOI:10.1074/jbc.271.3.1726. PMID 8576175.
- ↑ Chellaiah A, Yuan W, Chellaiah M, Ornitz DM (1999. december 1.). „Mapping ligand binding domains in chimeric fibroblast growth factor receptor molecules. Multiple regions determine ligand binding specificity”. The Journal of Biological Chemistry 274 (49), 34785–94. o. DOI:10.1074/jbc.274.49.34785. PMID 10574949.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a FGF9 című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.