Noskapin
| |
|---|---|

| |
| Nama sistematis (IUPAC) | |
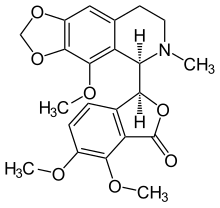
| (3S)-6,7-Dimetoksi-3-[(5R)-5,6,7,8-tetrahidro-4-metoksi-6-metil-1,3-dioksolo(4,5-g)isokuinolin-5-il]-1(3H)-isobenzofuranona | |
| Data klinis | |
| AHFS/Drugs.com | International Drug Names |
| Kat. kehamilan | Dikontraindikasikan |
| Status hukum | Apotek saja (S2) (AU) ℞ Preskripsi saja |
| Data farmakokinetik | |
| Bioavailabilitas | ~30% |
| Waktu paruh | 1,5 – 4 jam (Rata-rata 2,5) |
| Pengenal | |
| Nomor CAS | 128-62-1 |
| Kode ATC | R05DA07 |
| PubChem | CID 275196 |
| ChemSpider | 242139 |
| UNII | 8V32U4AOQU |
| KEGG | D01036 |
| ChEBI | CHEBI:73237 |
| ChEMBL | CHEMBL364713 |
| Sinonim | Narkotin |
| Data kimia | |
| Rumus | C22H23NO7 |
| SMILES | eMolecules & PubChem |
| |
Noskapin (juga dikenal sebagai Narkotin, Nektodon, Nospen, Anarkotin dan (arkaat) Opiana) adalah alkaloid benzilisokuinolin, dari subkelompok struktural ftalideisokuinolin, yang telah diasingkan dari banyak spesies tumbuhan keluarga Papaveraceae (keluarga popi). Obat ini tidak memiliki efek hipnotis, euforia, atau analgesik yang signifikan sehingga menghasilkan potensi kecanduan yang sangat rendah. [1] Obat ini terutama digunakan karena efek antitusifnya (menekan batuk).
Sejarah
[sunting | sunting sumber]Noskapin pertama kali diisolasi dan dikarakterisasi berdasarkan kerusakan dan sifat kimianya pada tahun 1803 dengan nama "Narkotin"[2][3] oleh Jean-Francois Derosne, seorang ahli kimia asal Prancis di Paris. Kemudian Pierre-Jean Robiquet, ahli kimia Prancis lainnya, membuktikan narkotin dan morfin sebagai alkaloid yang berbeda pada tahun 1831.[4] Terakhir, Pierre-Jean Robiquet melakukan selama 20 tahun (antara tahun 1815 dan 1835) serangkaian penelitian dalam peningkatan metode isolasi morfin, dan juga mengisolasi komponen lain yang sangat penting dari opium mentah (pada tahun 1832), yang dia sebut kodein, yang saat ini merupakan senyawa turunan opium yang banyak digunakan.
Kegunaan dalam Medis
[sunting | sunting sumber]Noskapin sering digunakan sebagai obat antitusif.[5] Namun, pedoman Belanda tahun 2012 tidak merekomendasikan penggunaannya untuk batuk akut.[6]
Efek Samping
[sunting | sunting sumber]- Mual
- Muntah
- Ataksia
- Halusinasi (pendengaran dan visual)
- Disfungsi seksual
- Hiperplasia prostat jinak
- Anoreksia
- Midriasis
- Takikardia
- Tremor dan spasmofili otot
- Sakit dada
- Peningkatan kewaspadaan
- Hilangnya rasa kantuk
- Hilangnya penglihatan stereoskopis
Interaksi
[sunting | sunting sumber]Noskapin dapat meningkatkan efek obat penenang terpusat seperti alkohol dan hipnotik.[7]
Obat ini tidak boleh dikonsumsi dengan MAOI (penghambat oksidase monoamina) apa pun, karena efek yang tidak diketahui dan berpotensi fatal dapat terjadi.[butuh rujukan]
Noskapin tidak boleh dikonsumsi bersamaan dengan warfarin karena efek antikoagulan warfarin dapat meningkat.[8]
Biosintesis
[sunting | sunting sumber]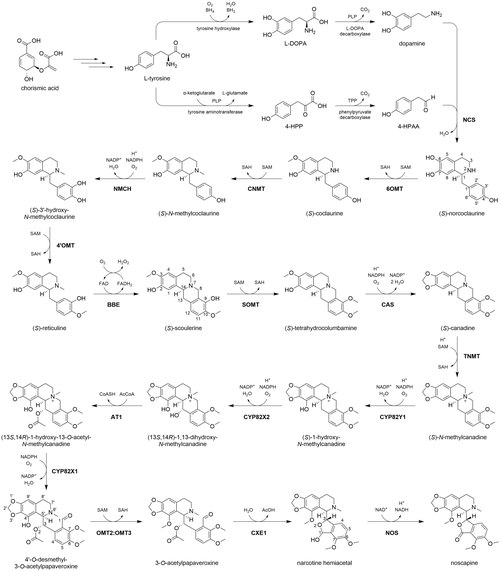
Biosintesis noskapin di Papaver somniferum dimulai dengan asam korismat, yang disintesis melalui jalur sikimat dari eritrosa 4-fosfat dan fosfoenolpiruvat. Asam korismat adalah prekursor asam amino tirosina, sumber nitrogen dalam alkaloid benzilisokuinolin. Tirosina dapat mengalami transaminasi yang dimediasi PLP untuk membentuk asam 4-hidroksifenilpiruvat (4-HPP), diikuti oleh dekarboksilasi yang dimediasi TPP untuk membentuk 4-hidroksifenilasetaldehid (4-HPAA). Tirosina juga dapat dihidroksilasi menjadi 3,4-dihidroksifenilalanin (levodopa), diikuti oleh dekarboksilasi yang dimediasi PLP untuk membentuk dopamin. Norkoklaurin sintase (NCS) mengkatalisis reaksi Pictet-Spengler antara 4-HPAA dan dopamin untuk mensintesis (S)-norkoklaurin, memberikan perancah benzilisokuinolin yang khas. (S) -Norkoklaurin secara berurutan 6-O-metilasi (6OMT), N-metilasi (CNMT), 3-hidroksilasi (NMCH), dan 4′-O-metilasi (4′OMT), dengan menggunakan kofaktor S- adenosil-metionin (SAM) dan NADP+ masing-masing untuk metilasi dan hidroksilasi. Reaksi ini menghasilkan (S)-retikulin, titik cabang utama dalam biosintesis alkaloid benzilisokuinolin.[9]
Sisa dari jalur biosintetik noskapin sebagian besar diatur oleh satu kluster 10 gen biosintetik.[10] Gen yang terdiri dari kluster mengkode enzim yang bertanggung jawab atas sembilan dari sebelas transformasi kimia yang tersisa. Pertama, enzim jembatan berberin (BBE), suatu enzim yang tidak dikodekan oleh kluster, membentuk struktur empat cincin yang menyatu dalam (S)-skoulerin. BBE menggunakan O2 sebagai oksidan dan dibantu oleh kofaktor flavin adenina dinukleotida (FAD). Selanjutnya, O-metiltransferase (SOMT) memetilasi gugus 9-hidroksil. Kanadin sintase (CAS) mengkatalisis pembentukan jembatan metilenadioksi C2-C3 yang unik di (S)-kanadin.[11] Metilasi N (TNMT) dan dua hidroksilasi (CYP82Y1, CYP82X2) menyusul, masing-masing dibantu oleh SAM dan O2/NADPH. Alkohol C13 kemudian diasetilasi oleh asetiltransferase (AT1) menggunakan asetil-KoA. Enzim sitokrom P450 lainnya (CYP82X1) mengkatalisis hidroksilasi C8, dan hemiaminal yang baru terbentuk secara spontan membelah, menghasilkan amina tersier dan aldehid. Heterodimer metiltransferase (OMT2:OMT3) mengkatalisis metilasi O yang dimediasi SAM pada C4′.[12] Gugus O-asetil kemudian dibelah oleh karboksilesterase (CXE1), menghasilkan alkohol yang segera bereaksi dengan aldehid C1 di dekatnya untuk membentuk hemiasetal dalam cincin baru beranggota lima. Kontraaktivitas yang nyata antara AT1 dan CXE1 menunjukkan bahwa asetilasi dalam konteks ini digunakan sebagai gugus pelindung, mencegah pembentukan hemiasetal sampai ester dibelah secara enzimatis.[13] Akhirnya, dehidrogenase rantai pendek (NOS) yang bergantung pada NAD+ mengoksidasi hemiasetal menjadi lakton, menyelesaikan biosintesis noskapin.[9]
Mekanisme Kerja
[sunting | sunting sumber]Efek antitusif noskapin tampaknya terutama dimediasi oleh aktivitas agonis reseptor σ. Bukti mekanisme ini ditunjukkan oleh bukti eksperimental pada tikus besar. Perawatan awal dengan rimkazol, antagonis reseptor spesifik σ, menyebabkan penurunan aktivitas antitusif noskapin yang bergantung pada dosis.[14] Noskapin dan turunan sintetiknya yang disebut noskapinoid, diketahui berinteraksi dengan mikrotubulus dan menghambat proliferasi sel kanker.[15]
Analisis Struktur
[sunting | sunting sumber]Cincin lakton tidak stabil dan terbuka pada media dasar. Reaksi sebaliknya disajikan dalam media asam. Ikatan (C1−C3′) yang menghubungkan dua atom karbon yang aktif secara optik juga tidak stabil. Dalam larutan asam sulfat encer dan pemanasan, ia terdisosiasi menjadi kotarnin (4-metoksi-6-metil-5,6,7,8-tetrahidro-[1,3]dioksolo[4,5-g]isokuinolin) dan asam opat (asam 6-formil-2,3-dimetoksibenzoat). Ketika noskapin direduksi dengan seng/HCl, ikatan C1−C3′ menjadi jenuh dan molekul terdisosiasi menjadi hidrokotarin (2-hidroksikotarnin) dan mekonin (6,7-dimetoksiisobenzofuran-1(3H)-ona).
Dalam Budaya Masyarakat
[sunting | sunting sumber]Penggunaan rekreasi
[sunting | sunting sumber]Ada laporan anekdot mengenai penggunaan obat-obatan bebas yang dijual bebas di beberapa negara,[16] yang tersedia di apotek lokal tanpa resep dokter. Efeknya, dimulai sekitar 45 hingga 120 menit setelah dikonsumsi, mirip dengan keracunan dekstrometorfan dan mabuk. Tidak seperti dekstrometorfan, noskapin bukanlah antagonis reseptor NMDA.[17]
Noskapin dalam Heroin
[sunting | sunting sumber]Noskapin dapat bertahan dalam proses pembuatan heroin dan dapat ditemukan di heroin jalanan. Hal ini berguna bagi lembaga penegak hukum, karena jumlah kontaminan dapat mengidentifikasi sumber obat yang disita. Pada tahun 2005 di Liège, Belgia, konsentrasi noskapin rata-rata adalah sekitar 8%.[18]
Noskapin juga telah digunakan untuk mengidentifikasi pengguna narkoba yang menggunakan heroin jalanan bersamaan dengan diamorfin yang diresepkan.[19] Karena diamorfin dalam heroin jalanan sama dengan diamorfin farmasetikal, pemeriksaan kontaminan adalah satu-satunya cara untuk menguji apakah heroin jalanan telah digunakan. Kontaminan lain yang digunakan dalam sampel urin bersama noskapin termasuk papaverin dan asetilkodein. Noskapin dimetabolisme oleh tubuh, dan jarang ditemukan dalam urin, melainkan hadir sebagai metabolit utama, yakni kotarnin dan mekonin. Deteksi dilakukan dengan kromatografi gas–spektrometri massa atau kromatografi cair–spektrometri massa (LCMS), tetapi juga dapat menggunakan berbagai teknik analisis lainnya.
Penelitian
[sunting | sunting sumber]Uji Coba Klinis
[sunting | sunting sumber]Kemanjuran noskapin dalam pengobatan keganasan hematologi tertentu telah dieksplorasi di klinik.[20][21] Induksi poliploidi oleh noskapin telah diamati secara in vitro pada limfosit manusia pada tingkat dosis tinggi (>30 μM); namun, misalnya paparan sistemik tingkat rendah dengan obat batuk, tampaknya tidak menimbulkan bahaya genotoksik. Mekanisme induksi poliploidi oleh noscapine diduga melibatkan kerusakan pemintal kromosom atau fusi sel.[22][23]
Rekonstitusi Biosintesis Noskapin
[sunting | sunting sumber]Banyak enzim dalam jalur biosintetik noskapin dijelaskan dengan penemuan 10 gen "gugus mirip operon" bernama HN1.[10] Pada tahun 2016, jalur biosintetik noskapin dibentuk kembali dalam sel ragi,[24] memungkinkan obat ini disintesis tanpa memerlukan pemanenan dan pemurnian dari bahan tanaman. Pada tahun 2018, seluruh jalur noskapin dibentuk kembali dan diproduksi dalam ragi dari molekul sederhana. Selain itu, ekspresi protein dioptimalkan dalam ragi, memungkinkan produksi noskapin ditingkatkan 18.000 kali lipat.[25] Diharapkan bahwa teknologi ini dapat digunakan untuk memproduksi alkaloid farmasetikal seperti noskapin yang saat ini dihasilkan dengan hasil yang terlalu rendah dari tumbuhan untuk diproduksi secara massal, sehingga memungkinkannya menjadi obat terapeutik yang dapat dipasarkan.[26]
Turunan Antikanker
[sunting | sunting sumber]Noskapin sendiri merupakan agen antimitotik, oleh karena itu analognya memiliki potensi besar sebagai obat antikanker baru.[27] Analog yang memiliki efek sitotoksik signifikan melalui modifikasi bagian 1,3-benzodioksol telah dikembangkan.[28] Demikian pula, turunan N-alkil amina, 1,3-diinil, 9-vinil-fenil dan 9-arilimino dari noskapin juga telah dikembangkan.[29][30][31][32] Mekanisme kerjanya adalah melalui penghambatan tubulin.[33]
Efek Antiinflamasi
[sunting | sunting sumber]Menariknya, berbagai penelitian menunjukkan bahwa noskapin memiliki efek antiinflamasi dan secara signifikan mengurangi kadar faktor proinflamasi seperti interleukin 1β (IL-1β), IFN-c, dan IL-6. Dalam hal ini, dalam penelitian lain, Khakpour dkk meneliti efek noskapin terhadap peradangan yang diinduksi karagenan pada tikus besar. Mereka menemukan bahwa noskapin dengan dosis 5 mg/kg berat badan dalam tiga jam setelah injeksi memiliki efek antiinflamasi paling besar. Selain itu, mereka menunjukkan bahwa jumlah pengurangan peradangan pada dosis noskapin ini kira-kira sama dengan indometasin sebagai obat antiinflamasi standar yang dikenal. Lebih lanjut, Shiri dkk menyimpulkan bahwa noskapin mencegah perkembangan peradangan yang disebabkan oleh bradikinin pada kaki tikus besar dengan mengantagonis reseptor bradikinin. Selain itu, Zughaier dkk mengevaluasi efek antiinflamasi dari noskapin brominasi. Bentuk noskapin brominasi telah terbukti menghambat sekresi sitokin TNF-α dan kemokin IP-10/CXCL10 dari makrofag, sehingga mengurangi peradangan tanpa mempengaruhi kelangsungan hidup makrofag. Selain itu, turunan bromat dari noskapin memiliki efek sekitar 5 hingga 40 kali lebih kuat dibandingkan noskapin. Sekali lagi, turunan brominasi ini juga menghambat reseptor seperti tol (TLR), faktor nekrosis tumor α (TNF-α), dan NO pada makrofag manusia dan tikus tanpa menyebabkan toksisitas. Selain itu, noskapin brominasi memiliki aktivitas antiinflamasi yang kuat pada model peradangan septik, menghambat faktor inflamasi dengan cara yang bergantung pada dosis, dan mencegah pelepasan TNF-α dan NO pada makrofag manusia dan tikus. Studi lain tentang penyakit radang usus (kolitis ulserativa) dan kanker usus besar menemukan bahwa noskapin memiliki efek antiinflamasi yang sangat baik yang secara signifikan dapat menurunkan kadar faktor proinflamasi seperti IL-1β, IFN-c, dan IL-6 dibandingkan dengan kelompok kontrol. Selain itu, telah ditemukan bahwa nanopartikel kitosan yang mengandung turunan noskapin brominasi dapat mengurangi sitokin proinflamasi seperti IL-1β, IFN-c, dan IL-6 serta peradangan pada jaringan mukosa usus besar.[34]
Referensi
[sunting | sunting sumber]- ^ Altinoz MA, Topcu G, Hacimuftuoglu A, Ozpinar A, Ozpinar A, Hacker E, Elmaci İ (August 2019). "Noscapine, a Non-addictive Opioid and Microtubule-Inhibitor in Potential Treatment of Glioblastoma". Neurochemical Research. 44 (8): 1796–1806. doi:10.1007/s11064-019-02837-x. PMID 31292803.
- ^ Derosne JF (1803). "Mémoire sur l'opium". Annales de chimie. 11: 257–285.
- ^ Drobnik J, Drobnik E (December 2016). "Timeline and bibliography of early isolations of plant metabolites (1770-1820) and their impact to pharmacy: A critical study". Fitoterapia. 115: 155–164. doi:10.1016/j.fitote.2016.10.009. PMID 27984164.
- ^ Wisniak J (March 2013). "Pierre-Jean Robiquet". Educación Química. 24 (Supplement 1): 139–149. doi:10.1016/S0187-893X(13)72507-2
 .
.
- ^ Singh H, Singh P, Kumari K, Chandra A, Dass SK, Chandra R (March 2013). "A review on noscapine, and its impact on heme metabolism". Current Drug Metabolism. 14 (3): 351–360. doi:10.2174/1389200211314030010. PMID 22935070.
- ^ Verlee L, Verheij TJ, Hopstaken RM, Prins JM, Salomé PL, Bindels PJ (2012). "[Summary of NHG practice guideline 'Acute cough']". Nederlands Tijdschrift voor Geneeskunde. 156: A4188. PMID 22917039.
- ^ Jasek, W, ed. (2007). Austria-Codex (dalam bahasa Jerman) (edisi ke-2007/2008). Vienna: Österreichischer Apothekerverlag. ISBN 978-3-85200-181-4.
- ^ Ohlsson S, Holm L, Myrberg O, Sundström A, Yue QY (February 2008). "Noscapine may increase the effect of warfarin". British Journal of Clinical Pharmacology. 65 (2): 277–278. doi:10.1111/j.1365-2125.2007.03018.x. PMC 2291222
 . PMID 17875192.
. PMID 17875192.
- ^ a b Singh A, Menéndez-Perdomo IM, Facchini PJ (2019). "Benzylisoquinoline alkaloid biosynthesis in opium poppy: an update". Phytochemistry Reviews. 18 (6): 1457–1482. Bibcode:2019PChRv..18.1457S. doi:10.1007/s11101-019-09644-w.
- ^ a b Winzer T, Gazda V, He Z, Kaminski F, Kern M, Larson TR, et al. (June 2012). "A Papaver somniferum 10-gene cluster for synthesis of the anticancer alkaloid noscapine". Science. 336 (6089): 1704–1708. Bibcode:2012Sci...336.1704W. doi:10.1126/science.1220757
 . PMID 22653730.
. PMID 22653730.
- ^ Dang TT, Facchini PJ (January 2014). "Cloning and characterization of canadine synthase involved in noscapine biosynthesis in opium poppy". FEBS Letters. 588 (1): 198–204. doi:10.1016/j.febslet.2013.11.037. PMID 24316226.
- ^ Park MR, Chen X, Lang DE, Ng KK, Facchini PJ (July 2018). "Heterodimeric O-methyltransferases involved in the biosynthesis of noscapine in opium poppy". The Plant Journal. 95 (2): 252–267. doi:10.1111/tpj.13947
 . PMID 29723437.
. PMID 29723437.
- ^ Dang TT, Chen X, Facchini PJ (February 2015). "Acetylation serves as a protective group in noscapine biosynthesis in opium poppy". Nature Chemical Biology. 11 (2): 104–106. doi:10.1038/nchembio.1717. PMID 25485687.
- ^ Kamei J (1996). "Role of opioidergic and serotonergic mechanisms in cough and antitussives". Pulmonary Pharmacology. 9 (5–6): 349–356. doi:10.1006/pulp.1996.0046. PMID 9232674.
- ^ Lopus M, Naik PK (February 2015). "Taking aim at a dynamic target: Noscapinoids as microtubule-targeted cancer therapeutics". Pharmacological Reports. 67 (1): 56–62. doi:10.1016/j.pharep.2014.09.003. PMID 25560576.
- ^ Bhatia M, Vaid L (August 2004). "Type of drug abuse in patients with psychogenic cough". The Journal of Laryngology and Otology. 118 (8): 659–660. doi:10.1258/0022215041917844
 . PMID 15453951.
. PMID 15453951.
- ^ Church J, Jones MG, Davies SN, Lodge D (June 1989). "Antitussive agents as N-methylaspartate antagonists: further studies". Canadian Journal of Physiology and Pharmacology. 67 (6): 561–567. doi:10.1139/y89-090. PMID 2673498.
- ^ Denooz R, Dubois N, Charlier C (September 2005). "[Analysis of two year heroin seizures in the Liege area]". Revue Médicale de Liège (dalam bahasa Prancis). 60 (9): 724–728. PMID 16265967.
- ^ Paterson S, Lintzeris N, Mitchell TB, Cordero R, Nestor L, Strang J (December 2005). "Validation of techniques to detect illicit heroin use in patients prescribed pharmaceutical heroin for the management of opioid dependence". Addiction. 100 (12): 1832–1839. doi:10.1111/j.1360-0443.2005.01225.x
 . PMID 16367984.
. PMID 16367984.
- ^ "Study of Noscapine for Patients With Low Grade Non-Hodgkin's Lymphoma or Chronic Lymphocytic Leukemia Refractory to Chemotherapy". ClinicalTrials.gov. May 22, 2014.
- ^ "A Study of Noscapine HCl (CB3304) in Patients with Relapsed or Refractory Multiple Myeloma". ClinicalTrials.gov. October 7, 2016.
- ^ Mitchell ID, Carlton JB, Chan MY, Robinson A, Sunderland J (November 1991). "Noscapine-induced polyploidy in vitro". Mutagenesis. 6 (6): 479–486. doi:10.1093/mutage/6.6.479. PMID 1800895.
- ^ Schuler M, Muehlbauer P, Guzzie P, Eastmond DA (January 1999). "Noscapine hydrochloride disrupts the mitotic spindle in mammalian cells and induces aneuploidy as well as polyploidy in cultured human lymphocytes". Mutagenesis. 14 (1): 51–56. doi:10.1093/mutage/14.1.51
 . PMID 10474821.
. PMID 10474821.
- ^ Li Y, Smolke CD (July 2016). "Engineering biosynthesis of the anticancer alkaloid noscapine in yeast". Nature Communications. 7: 12137. Bibcode:2016NatCo...712137L. doi:10.1038/ncomms12137. PMC 4935968
 . PMID 27378283.
. PMID 27378283.
- ^ Li Y, Li S, Thodey K, Trenchard I, Cravens A, Smolke CD (April 2018). "Complete biosynthesis of noscapine and halogenated alkaloids in yeast". Proceedings of the National Academy of Sciences of the United States of America. 115 (17): E3922–E3931. Bibcode:2018PNAS..115E3922L. doi:10.1073/pnas.1721469115
 . PMC 5924921
. PMC 5924921  . PMID 29610307.
. PMID 29610307.
- ^ Kries H, O'Connor SE (April 2016). "Biocatalysts from alkaloid producing plants". Current Opinion in Chemical Biology. 31: 22–30. doi:10.1016/j.cbpa.2015.12.006
 . hdl:21.11116/0000-0002-B92F-A
. hdl:21.11116/0000-0002-B92F-A  . PMID 26773811.
. PMID 26773811.
- ^ Mahmoudian M, Rahimi-Moghaddam P (January 2009). "The anti-cancer activity of noscapine: a review". Recent Patents on Anti-Cancer Drug Discovery. 4 (1): 92–97. doi:10.2174/157489209787002524. PMID 19149691.
- ^ Yong C, Devine SM, Abel AC, Tomlins SD, Muthiah D, Gao X, et al. (September 2021). "1,3-Benzodioxole-Modified Noscapine Analogues: Synthesis, Antiproliferative Activity, and Tubulin-Bound Structure". ChemMedChem. 16 (18): 2882–2894. doi:10.1002/cmdc.202100363. PMID 34159741 Periksa nilai
|pmid=(bantuan). - ^ Dash SG, Suri C, Nagireddy PK, Kantevari S, Naik PK (September 2021). "Rational design of 9-vinyl-phenyl noscapine as potent tubulin binding anticancer agent and evaluation of the effects of its combination on Docetaxel". Journal of Biomolecular Structure & Dynamics. 39 (14): 5276–5289. doi:10.1080/07391102.2020.1785945. PMID 32608323.
- ^ Meher RK, Pragyandipta P, Pedapati RK, Nagireddy PK, Kantevari S, Nayek AK, Naik PK (September 2021). "Rational design of novel N-alkyl amine analogues of noscapine, their chemical synthesis and cellular activity as potent anticancer agents". Chemical Biology & Drug Design. 98 (3): 445–465. doi:10.1111/cbdd.13901. PMID 34051055 Periksa nilai
|pmid=(bantuan). - ^ Patel AK, Meher RK, Reddy PK, Pedapati RK, Pragyandipta P, Kantevari S, et al. (July 2021). "Rational design, chemical synthesis and cellular evaluation of novel 1,3-diynyl derivatives of noscapine as potent tubulin binding anticancer agents". Journal of Molecular Graphics & Modelling. 106: 107933. doi:10.1016/j.jmgm.2021.107933. PMID 33991960 Periksa nilai
|pmid=(bantuan). - ^ Patel AK, Meher RK, Nagireddy PK, Pragyandipta P, Pedapati RK, Kantevari S, Naik PK (April 2021). "9-Arylimino noscapinoids as potent tubulin binding anticancer agent: chemical synthesis and cellular evaluation against breast tumour cells". SAR and QSAR in Environmental Research. 32 (4): 269–291. doi:10.1080/1062936X.2021.1891567. PMID 33687299 Periksa nilai
|pmid=(bantuan). - ^ Mandavi S, Verma SK, Banjare L, Dubey A, Bhatt R, Thareja S, Jain AK (2021). "A Comprehension into Target Binding and Spatial Fingerprints of Noscapinoid Analogues as Inhibitors of Tubulin". Medicinal Chemistry. 17 (6): 611–622. doi:10.2174/1573406416666200117120348. PMID 31951171.
- ^ Rahmanian-Devin P, Baradaran Rahimi V, Jaafari MR, Golmohammadzadeh S, Sanei-Far Z, Askari VR (2021-11-30). "Noscapine, an Emerging Medication for Different Diseases: A Mechanistic Review". Evidence-Based Complementary and Alternative Medicine. 2021: 8402517. doi:10.1155/2021/8402517
 . PMC 8648453
. PMC 8648453  Periksa nilai
Periksa nilai |pmc=(bantuan). PMID 34880922 Periksa nilai|pmid=(bantuan).