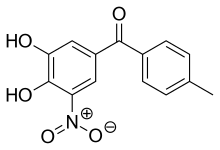
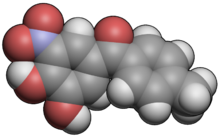
Tolkapon
| |
|---|---|
| |
| Nama sistematis (IUPAC) | |
| (3,4-Dihidroksi-5-nitrofenil)(4-metilfenil)metanona | |
| Data klinis | |
| Nama dagang | Tasmar |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a698036 |
| Data lisensi | EMA:pranala, US Daily Med:pranala |
| Kat. kehamilan | B3(AU) |
| Status hukum | Harus dengan resep dokter (S4) (AU) POM (UK) ℞-only (US) |
| Rute | Oral |
| Data farmakokinetik | |
| Bioavailabilitas | 65% |
| Ikatan protein | >99.9% |
| Metabolisme | Hati (terutama glukuronidasi) |
| Waktu paruh | 2–3 jam |
| Ekskresi | Urin (60%), feses (40%); selalu 0,5% dalam bentuk yang tidak dimetabolisme |
| Pengenal | |
| Nomor CAS | 134308-13-7 |
| Kode ATC | N04BX01 |
| PubChem | CID 4659569 |
| Ligan IUPHAR | 6646 |
| DrugBank | DB00323 |
| ChemSpider | 3848682 |
| UNII | CIF6334OLY |
| KEGG | D00786 |
| ChEMBL | CHEMBL1324 |
| Data kimia | |
| Rumus | C14H11NO5 |
| |
| Data fisik | |
| Titik lebur | 143–146 °C (289–295 °F) |
| Kelarutan dalam air | tidak larut mg/mL (20 °C) |
Tolkapon adalah obat yang digunakan untuk mengobati penyakit Parkinson(PD). Obat ini merupakan penghambat enzim katekol-O-metiltransferase (COMT) tipe nitrokatekol yang selektif, kuat, dan reversibel.[1] Obat ini telah menunjukkan toksisitas hati yang signifikan, yang menyebabkan penangguhan izin edar di sejumlah negara.
Tolkapon tampaknya selektif secara perifer, tetapi masih dapat masuk ke otak dalam jumlah yang signifikan dan telah ditemukan menghambat COMT secara sentral juga.[2][3] Dibandingkan dengan entakapon, penghambat COMT nitrokatekol lainnya, tolkapon memiliki waktu paruh yang lebih panjang (2,9 jam vs. 0,8 jam) dan dapat menembus otak dengan lebih baik, bekerja baik di sistem saraf pusat maupun di sistem saraf tepi.[4] Namun entakapon kurang beracun bagi hati.
Sejarah
[sunting | sunting sumber]Tolkapon diperkenalkan ke pasar Eropa pada bulan Agustus 1997, dan kemudian ke pasar Amerika Serikat pada bulan Maret 1998. Toksisitas hati dilaporkan pada empat orang yang diberi tolkapon, tiga orang meninggal karena komplikasi. Akibatnya, otorisasi pemasaran tolkapon ditangguhkan dari Desember 1998 hingga Agustus 2004 ketika dicabut. Pada bulan November 1998, perusahaan yang memproduksi tolkapon secara sukarela[5] menarik obat tersebut dari pasar. Otorisasi tersebut kemudian diperbarui pada bulan Agustus 2009.[6]
Sebagai akibat dari komplikasi yang dilaporkan, Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) mengeluarkan peringatan kotak hitam untuk tolkapon dan revisi label yang bertujuan untuk mengatur pemantauan mereka yang diresepkan tolkapon untuk penyakit Parkinson pada bulan November 1998.[7] Sejumlah negara lain menarik tolkapon dari pasar; Australia pada bulan Februari 1999, Bulgaria pada bulan April 1999, Islandia pada bulan November 1998, dan Lithuania pada bulan Desember 1998.[5]
Kegunaan medis
[sunting | sunting sumber]Tolkapon digunakan dalam pengobatan penyakit Parkinson sebagai tambahan untuk obat levodopa/karbidopa atau levodopa/benserazida. Levodopa adalah obat awal untuk dopamin, yang mengurangi gejala Parkinson; karbidopa dan benserazid adalah penghambat dekarboksilase asam amino aromatik L (AADC).[8]
Tanpa pemberian tolkapon, efek menguntungkan dari levodopa cenderung lebih cepat hilang, sehingga mengakibatkan fluktuasi motorik.[9]
Kontraindikasi
[sunting | sunting sumber]Menggabungkan tolkapon dengan penghambat oksidase monoamina non-selektif seperti fenelzin atau tranilsipromin merupakan kontraindikasi.[10] Tolkapon juga merupakan kontraindikasi bagi orang dengan penyakit hati atau peningkatan enzim hati.[11]
Efek samping
[sunting | sunting sumber]Tolkapon telah menunjukkan toksisitas hati yang signifikan (hepatotoksisitas)[12] yang membatasi kegunaan obat ini. Entakapon merupakan alternatif, terutama karena obat ini memiliki profil toksisitas yang lebih baik.
Hepatotoksisitas dapat dikaitkan dengan peningkatan kadar transaminase, tetapi penelitian telah menunjukkan bahwa risiko minimal ada pada mereka yang tidak memiliki kondisi hati sebelumnya saat kadar enzim mereka dipantau. Tidak ada mekanisme yang jelas yang terlibat, tetapi telah dihipotesiskan bahwa hal itu ada hubungannya dengan respirasi mitokondria yang abnormal karena pelepasan fosforilasi oksidatif.[13]
Efek samping lainnya adalah peningkatan aktivitas dopaminergik, termasuk gejala pencernaan.[11] Pengobatan dengan tolkapon berisiko menimbulkan atau memperpanjang diskinesia; hal ini dapat diatasi dengan mengurangi dosis levodopa. Hal ini terjadi karena pemberian tolkapon mengakibatkan akumulasi donor metil biologis S-adenosil-L-metionina (SAM) di striatum yang memicu gejala Parkinson.[13]
Gejala pencernaan meliputi mual dan diare; efek samping dopaminergik lebih lanjut meliputi hipotensi ortostatik, mulut kering, berkeringat, dan pusing. Tolkapon menyebabkan diare yang lebih parah daripada entakapon; ini merupakan alasan paling umum untuk penghentian terapi dalam penelitian.[10] Perubahan warna urin berasal dari metabolit tolkapon yang menguning, yang dikeluarkan dalam urin dan tidak berbahaya.[11][13]
Interaksi
[sunting | sunting sumber]Meskipun peningkatan kadar dopamin merupakan interaksi yang diinginkan, tolkapon secara teoritis juga dapat meningkatkan kadar obat lain yang dimetabolisme oleh COMT, seperti penghambat AADC karbidopa dan benserazid; serta metildopa, dobutamin, apomorfin, adrenalin, dan isoprenalin. Dalam penelitian, interaksi ringan dengan benzerazida terlihat, tetapi tidak dengan karbidopa. Interaksi lain dengan kelompok obat ini belum dipelajari. Jenis interaksi teoritis terkait adalah dengan obat yang meningkatkan konsentrasi katekolamina, seperti penghambat oksidase monoamina (MAO) dan penghambat penyerapan kembali noradrenalin; obat-obatan ini juga hanya menunjukkan sedikit efek dalam praktik. Kombinasi dengan penghambat MAO non-selektif mungkin berbahaya.[10][11]
Karena afinitasnya terhadap enzim hati CYP2C9, interaksi dengan obat yang dimetabolisme oleh enzim ini juga mungkin terjadi. Tidak ada interaksi dengan tolbutamid, substrat 2C9, yang diamati dalam penelitian.[11]
Farmakologi
[sunting | sunting sumber]Mekanisme kerja
[sunting | sunting sumber]
Tolkapon secara selektif dan reversibel[10] terikat pada situs katalitik COMT di perifer dan sistem saraf pusat (SSP) dengan afinitas yang lebih besar daripada ketiga katekolamina, termasuk levodopa.[15] Dengan demikian, tolkapon mencegah 3-O-metilasi levodopa oleh COMT di perifer, yang menghasilkan 3-O-metildopa, metabolit utama yang bersaing dengan levodopa untuk melewati sawar darah otak. Lebih banyak levodopa yang diberikan mencapai SSP. Selain itu, levodopa yang telah mencapai SSP, setelah diubah menjadi dopamin, tidak akan terdegradasi secepat ketika tolkapon menghambat aktivitas COMT. Dengan demikian, tolkapon meningkatkan bioavailabilitas dan mengurangi pembersihan levodopa dan selanjutnya dopamin dari SSP.[16]

Kekuatan afinitas pengikatan tolkapon, yang direpresentasikan oleh konstanta penghambatan Ki (2,5 nM), dapat dianggap sebagai konstanta disosiasi untuk kinetika kompleks enzim dan penghambat. Aktivitas katalitik maksimum menunjukkan kemanjuran tolkapon (Vmax = 58,4 pmol/min·mg).[17]
Farmakokinetik
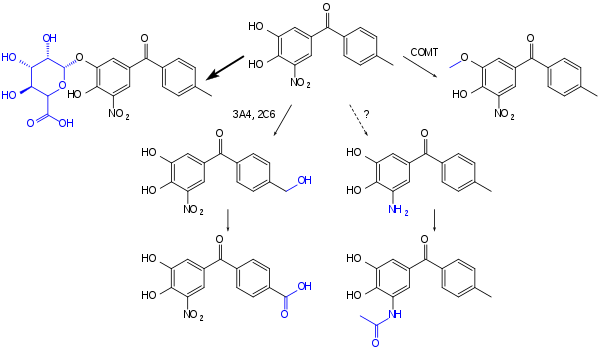
[sunting | sunting sumber]Tolkapon cepat diserap dari usus hingga sekitar 85%. Ia memiliki bioavailabilitas absolut sebesar 65%, yang hanya sedikit menurun jika dikonsumsi bersama makanan. Zat tersebut mencapai konsentrasi plasma darah tertinggi setelah sekitar dua jam. Ketika berada di aliran darah, obat ini hampir seluruhnya (>99,9%) terikat pada protein plasma, terutama albumin. Langkah inaktivasi utama adalah glukuronidasi; proses lainnya adalah metilasi oleh COMT, hidroksilasi oleh CYP3A4 dan CYP2A6 dengan oksidasi berikutnya menjadi asam karboksilat, dan mungkin jalur minor dengan reduksi menjadi amina dengan asetilasi berikutnya.[10][11]
Waktu paruh tolkapon adalah dua hingga tiga jam, volume distribusi (Vd)nya adalah 0,3 L/kg (21 L pada orang dengan berat rata-rata 70 kg).[9] 60% metabolit diekskresikan melalui urin dan 40% melalui feses. Hanya 0,5% obat yang diekskresikan dalam bentuk tidak berubah melalui urin.[10][11]
Koefisien partisi mengukur kemampuan molekul untuk melewati sawar dara otak. LogPIdce= 0,2, –1,4, –0,4 untuk tolkapon, nitekapon, dan entakapon. Koefisien partisi dalam kasus ini diukur dalam larutan 1,2-dikloroetana/H2O yang menyebabkan molekul berada dalam bentuk terionisasi. Tidak ada penjelasan saat ini tentang bagaimana molekul bermuatan ini menembus sawar darah otak.[18]
Tolkapon dikatakan memasuki sistem saraf pusat hanya minimal dan karenanya tampaknya selektif secara perifer.[2] Namun, tolkapon lebih lipofilik daripada penghambat COMT lainnya seperti entakapon dan mungkin lebih mungkin melewati sawar darah-otak (BBB). Sebuah studi pencitraan pada manusia menemukan bahwa tolkapon juga menghambat COMT di otak hingga tingkat yang signifikan.[3]
Kimia
[sunting | sunting sumber]Penelitian
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ Antonini A, Abbruzzese G, Barone P, Bonuccelli U, Lopiano L, Onofrj M, Zappia M, Quattrone A (February 2008). "COMT inhibition with tolcapone in the treatment algorithm of patients with Parkinson's disease (PD): relevance for motor and non-motor features". Neuropsychiatric Disease and Treatment. 4 (1): 1–9. doi:10.2147/NDT.S2404
 . PMC 2515921
. PMC 2515921  . PMID 18728767.
. PMID 18728767.
- ^ a b Keating GM, Lyseng-Williamson KA (2005). "Tolcapone: a review of its use in the management of Parkinson's disease". CNS Drugs. 19 (2): 165–184. doi:10.2165/00023210-200519020-00006. PMID 15697329.
The efficacy of tolcapone as an adjunct to levodopa in patients with Parkinson's disease has primarily been attributed to its ability to inhibit peripheral it is thought that tolcapone enters the CNS to a minimal extent only.[16] However, results [17] of a study in patients with Parkinson's disease, as well as results of animal studies,[18-21] suggest that tolcapone also has central activity.
- ^ a b Fabbri M, Ferreira JJ, Lees A, Stocchi F, Poewe W, Tolosa E, Rascol O (October 2018). "Opicapone for the treatment of Parkinson's disease: A review of a new licensed medicine". Mov Disord. 33 (10): 1528–1539. doi:10.1002/mds.27475. PMID 30264443.
The possible central effect of tolcapone, which is more lipophilic than entacapone and may be more likely to cross the blood-brain barrier (BBB), has been under debate for many years.26 An (18)F-dopa positron emission tomography study showed its effect as a central COMT inhibitior.27 However, this effect was not translated into clinical benefit in L-dopa-naive patients, in whom tolcapone alone or added to selegiline was compared with placebo.28 Tolcapone is more efficacious than entacapone, as it reduces total OFF time by an average of 98 minutes daily.
- ^ Forsberg M, Lehtonen M, Heikkinen M, Savolainen J, Järvinen T, Männistö PT (February 2003). "Pharmacokinetics and pharmacodynamics of entacapone and tolcapone after acute and repeated administration: a comparative study in the rat". The Journal of Pharmacology and Experimental Therapeutics. 304 (2): 498–506. doi:10.1124/jpet.102.042846. PMID 12538800.
- ^ a b "2001 Pharmaceuticals: Restrictions in Use and Availability". World Health Organization. Diarsipkan dari versi asli tanggal 12 June 2011. Diakses tanggal 31 October 2012.
- ^ "Tasmar tolcapone EPAR summary for the public" (PDF). European Medicine Agency. Diarsipkan dari versi asli (PDF) tanggal 22 May 2013. Diakses tanggal 31 October 2012.
- ^ Press Office, U.S. Department of Health and Human Services. "FDA Talk Paper". New Warnings for Parkinson's Drug, Tasmar. Food and Drug Administration.
- ^ Dingemanse J, Jorga K, Zürcher G, Schmitt M, Sedek G, Da Prada M, Van Brummelen P (September 1995). "Pharmacokinetic-pharmacodynamic interaction between the COMT inhibitor tolcapone and single-dose levodopa". British Journal of Clinical Pharmacology. 40 (3): 253–62. doi:10.1111/j.1365-2125.1995.tb05781.x. PMC 1365105
 . PMID 8527287.
. PMID 8527287.
- ^ a b Jorga KM, Fotteler B, Heizmann P, Zürcher G (July 1998). "Pharmacokinetics and pharmacodynamics after oral and intravenous administration of tolcapone, a novel adjunct to Parkinson's disease therapy". European Journal of Clinical Pharmacology. 54 (5): 443–7. doi:10.1007/s002280050490. PMID 9754991.
- ^ a b c d e f Dinnendahl V, Fricke U, ed. (1998). Arzneistoff-Profile (dalam bahasa German). 10 (edisi ke-13). Eschborn, Germany: Govi Pharmazeutischer Verlag. ISBN 978-3-7741-9846-3.
- ^ a b c d e f g h "Tasmar: EPAR – Product Information" (PDF). European Medicines Agency. 3 August 2016. Diarsipkan dari versi asli (PDF) tanggal 15 April 2017. Diakses tanggal 15 April 2017.
- ^ Olanow CW, Watkins PB (2007). "Tolcapone: an efficacy and safety review (2007)". Clinical Neuropharmacology. 30 (5): 287–94. doi:10.1097/wnf.0b013e318038d2b6. PMID 17909307.
- ^ a b c Truong DD (2009). "Tolcapone: review of its pharmacology and use as adjunctive therapy in patients with Parkinson's disease". Clinical Interventions in Aging. 4: 109–13. doi:10.2147/CIA.S3787
 . PMC 2685232
. PMC 2685232  . PMID 19503773.
. PMID 19503773.
- ^ Ellermann M, Lerner C, Burgy G, Ehler A, Bissantz C, Jakob-Roetne R, Paulini R, Allemann O, Tissot H, Grünstein D, Stihle M, Diederich F, Rudolph MG (March 2012). "Catechol-O-methyltransferase in complex with substituted 3'-deoxyribose bisubstrate inhibitors". Acta Crystallographica. Section D, Biological Crystallography. 68 (Pt 3): 253–60. doi:10.1107/S0907444912001138. PMID 22349227.
- ^ Deleu D, Northway MG, Hanssens Y (2002). "Clinical pharmacokinetic and pharmacodynamic properties of drugs used in the treatment of Parkinson's disease". Clinical Pharmacokinetics. 41 (4): 261–309. doi:10.2165/00003088-200241040-00003. PMID 11978145.
- ^ Jorga K, Fotteler B, Heizmann P, Gasser R (October 1999). "Metabolism and excretion of tolcapone, a novel inhibitor of catechol-O-methyltransferase". British Journal of Clinical Pharmacology. 48 (4): 513–20. doi:10.1046/j.1365-2125.1999.00036.x. PMC 2014389
 . PMID 10583021.
. PMID 10583021.
- ^ Forsberg MM, Huotari M, Savolainen J, Männistö PT (April 2005). "The role of physicochemical properties of entacapone and tolcapone on their efficacy during local intrastriatal administration". European Journal of Pharmaceutical Sciences. 24 (5): 503–11. doi:10.1016/j.ejps.2005.01.005. PMID 15784340.
- ^ Novaroli L, Bouchard Doulakas G, Reist M, Rolando B, Fruttero R, Gasco A, Carrupt PA (2006). "The Lipophilicity Behavior of Three Catechol-O-methyltransferase (COMT) Inhibitors and Simple Analogues". Helvetica Chimica Acta. 89 (1): 144–152. doi:10.1002/hlca.200690007.
Pranala luar
[sunting | sunting sumber]- "Tolcapone". Drug Information Portal. U.S. National Library of Medicine.