Dibenzenecromo
| Dibenzenecromo | |
|---|---|
| Nomi alternativi | |
| bis(benzene)cromo(0) | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C12H12Cr |
| Massa molecolare (u) | 208,22 |
| Aspetto | cristalli marrone scuro |
| Numero CAS | |
| Numero EINECS | 215-042-7 |
| PubChem | 11984611 |
| SMILES | [CH-]1[CH-][CH-][CH-][CH-][CH-]1.C1=CC=CC=C1.[Cr] |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | insolubile |
| Temperatura di fusione | 285 °C (558 K) |
| Temperatura di ebollizione | 300 °C (573 K) decomposizione |
| Indicazioni di sicurezza | |
| Punto di fiamma | 82 °C (355 K) |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 228 |
| Consigli P | 210 [1] |
Il dibenzenecromo è il composto metallorganico di formula Cr(η6-C6H6)2. Il composto ha giocato un ruolo importante nello sviluppo dei composti a sandwich nella chimica metallorganica ed è l'esempio più semplice di complesso contenente due areni neutri come leganti.
Proprietà e struttura
[modifica | modifica wikitesto]Cr(η6-C6H6)2 è un composto molecolare. È un solido cristallino marrone scuro, molto sensibile all'aria; la sua preparazione e manipolazione richiede l'utilizzo di glove box o vetreria Schlenk. In assenza di aria il composto è invece notevolmente stabile e si decompone solo a circa 300 °C. Il cromo raggiunge una configurazione elettronica con 18 elettroni nello strato più esterno, e il composto è diamagnetico. Il momento dipolare è zero. Studi di diffrazione a raggi X mostrano la struttura illustrata a fianco, con i due anelli benzenici paralleli ed eclissati. La simmetria della molecola risulta D6h.
Sintesi
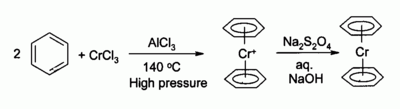
[modifica | modifica wikitesto]Fu preparato per la prima volta da Walter Hafner e Ernst Otto Fischer nel 1955,[2][3] facendo reagire CrCl3, alluminio e benzene in presenza di AlCl3. Questo cosiddetto metodo riduttivo di Friedel-Crafts fu introdotto da Fischer con i suoi studenti.[4][5] Si otteneva un composto giallo, [Cr(C6H6)2]+, che era poi ridotto con ditionito di sodio per arrivare al complesso neutro. In forma schematica le reazioni sono:
- CrCl3 + ⅔ Al + ⅓ AlCl3 + 2 C6H6 → [Cr(C6H6)2]AlCl4 + ⅔ AlCl3
- [Cr(C6H6)2]AlCl4 + ½ Na2S2O4 → [Cr(C6H6)2] + NaAlCl4 + SO2
Composti strettamente correlati a [Cr(C6H6)2]+ erano stati preparati da Franz Hein molti anni prima del lavoro di Fischer, facendo reagire bromuro di fenilmagnesio e CrCl3.[6] La reazione di Hein porta a complessi a sandwich cationici contenenti bifenile e terfenile, che lasciarono sconcertati i chimici fino alla scoperta di Fischer e Hafner.[7] Dunque Hein aveva scoperto senza saperlo i complessi a sandwich mezzo secolo prima del lavoro sul ferrocene. Fischer e Seus prepararono poco dopo il complesso di Hein [Cr(C6H5-C6H5)2]+.[8][9] Le ricerche in questo campo procedevano velocissime: nello stesso numero del Chemische Berichte viene descritto anche il complesso di Mo(0).[10]
Reattività
[modifica | modifica wikitesto]Il dibenzenenecromo reagisce con acidi carbossilici per formare carbossilati di cromo(II), come l'acetato di cromo(II), che possiedono strutture interessanti. Per ossidazione si forma [Cr(C6H6)2]+. Per carbonilazione si ottiene il benzenetricarbonilcromo, [Cr(C6H6)(CO)3]. Il dibenzenenecromo trova impieghi limitati in chimica organica.[11]
Note
[modifica | modifica wikitesto]- ^ Sigma Aldrich; rev. del 27.07.2010
- ^ E. O. Fischer e W. Haffner, Z. Naturforsch., 10b, 1955, p. 665.
- ^ E. O. Fischer e W. Haffner, Über Aromatenkomplexe von Metallen. III. Zur Darstellung des Di-benzol-chroms, in Z. anorg. allg. Chem., vol. 286, n. 3-4, 1956, pp. 146-148, DOI:10.1002/zaac.19562860306. URL consultato il 26 gennaio 2011.
- ^ R. B. King, Organometallic syntheses. Volume 1. Transition-metal compounds, New York, Academic Press, 1965, ISBN 0-444-42607-8.
- ^ C. Elschenbroich e A. Salzer, Organometallics: a concise introduction, 2ª ed., Weinheim, Wiley-VCH, 1992, ISBN 3-527-28165-7.
- ^ D. Seyferth, Bis(benzene)chromium. 1. Franz Hein at the University of Leipzig and Harold Zeiss and Minoru Tsutsui at Yale, in Organometallics, vol. 21, 2002, pp. 1520–1530, DOI:10.1021/om0201056. URL consultato il 30 gennaio 2011.
- ^ D. Seyferth, Bis(benzene)chromium. 2. Its discovery by E. O. Fischer and W. Hafner and subsequent work by the research groups of E. O. Fischer, H. H. Zeiss, F. Hein, C. Elschenbroich, and others, in Organometallics, vol. 21, 2002, pp. 2800–2820, DOI:10.1021/om020362a. URL consultato il 30 gennaio 2011.
- ^ E. O. Fischer e D. Seus, Zur Frage der Struktur der Chrom-phenyl-Verbindungen. Über Aromatenkomplexe von Metallen VI, in Chem. Ber., vol. 89, n. 8, 1956, pp. 1809–1815, DOI:10.1002/cber.19560890803. URL consultato il 30 gennaio 2011.
- ^ F. Hein, Zur Frage der Struktur der Chrom-phenyl-Verbindungen. Bemerkungen zur Abhandlung von E. O. Fischer und D. Seus, in Chem. Ber., vol. 89, n. 8, 1956, pp. 1816–1821, DOI:10.1002/cber.19560890804. URL consultato il 30 gennaio 2011.
- ^ E. O. Fischer e H.-O Stahl, Di-benzol-molybdän (0). Über Aromatenkomplexe von Metallen V, in Chem. Ber., vol. 89, n. 8, pp. 1805-1808, DOI:10.1002/cber.19560890802. URL consultato il 30 gennaio 2011.
- ^ J. W. Herndon, Dibenzenechromium, in L. Paquette (a cura di), Encyclopedia of Reagents for Organic Synthesis, New York, John Wiley & Sons, 2004, DOI:10.1002/047084289.
Bibliografia
[modifica | modifica wikitesto]- N. N. Greenwood, A. Earnshaw, Chemistry of the elements, 2ª ed., Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4.
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su Dibenzenecromo
Wikimedia Commons contiene immagini o altri file su Dibenzenecromo