Prismano
| Prismano | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| Tetraciclo[2.2.0.02,6.03,5]esano | |
| Nomi alternativi | |
| [3]prismano triprismano benzene di Ladenburg | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H6 |
| Massa molecolare (u) | 78,1134 |
| Aspetto | liquido incolore, esplosivo |
| Numero CAS | |
| PubChem | 12305738 |
| SMILES | C12C3C1C4C2C34 |
| Indicazioni di sicurezza | |
Il prismano,[1] nome sistematico [3]prismano o triprismano,[2] è un idrocarburo tetraciclico alifatico di formula (CH)6. Deve il suo nome al fatto che i 6 atomi di carbonio dello scheletro sono disposti ai vertici di un prisma triangolare; in quanto tale rappresenta il più semplice dei prismani,[3][4] una classe di idrocarburi facente parte della classe più ampia dei poliedrani.[5] La disposizione geometrica risultante ha simmetria molecolare D3h.[6]
Albert Ladenburg propose erroneamente questa struttura per il benzene.[7] Il composto fu sintetizzato in laboratorio solo nel 1973.[8]
Proprietà[modifica | modifica wikitesto]
Il prismano è un isomero del benzene (D6h) avente però una stabilità molto minore e una reattività molto maggiore e nettamente differente da quest'ultimo. Del benzene rappresenta anche un isomero di valenza, in quanto può essere convertito in esso direttamente, ad esempio tramite reazioni pericicliche di fotolisi.[9]
Gli angoli CCC di 60° nelle facce triangolari e 90° in quelle quadrate, sono molto distanti dall'angolo tetraedrico (109,5°), cioè quello ideale per il carbonio saturo e questo fa sì che la molecola sia in forte tensione (~ 90 kcal/mol)[10] e quindi alquanto instabile, sebbene il suo derivato esametilsostituito (CMe)6, che è stato anch'esso ottenuto nel 1966, prima del prismano stesso, sia più stabile.[11]
A temperatura ambiente si presenta come un liquido incolore incline ad esplodere.[8]
Sintesi[modifica | modifica wikitesto]
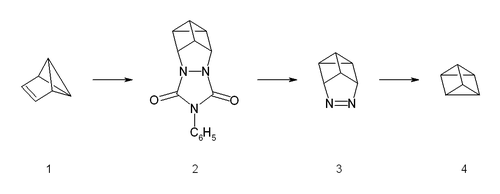
La sintesi parte dal benzvalene (1) e dal 4-feniltriazolidone, che è uno tra i più forti dienofili.[12] La reazione è del tipo Diels-Alder, ma stadi, che comporta la formazione di un carbocatione come intermedio. L'addotto (2) è poi idrolizzato e successivamente trasformato in un sale di rame(II). Dopo neutralizzazione con una base forte, l'azocomposto (3) può essere cristallizzato con una resa del 65%. L'ultimo passaggio prevede una fotolisi dell'azo composto. Questa fotolisi porta alla formazione di un biradicale che decomponendosi forma il prismano (4) e azoto, con una resa inferiore al 10%. Il prismano viene poi isolato tramite gascromatografia preparativa.[8]
Note[modifica | modifica wikitesto]
- ^ Raimondo Germani, Molecole dalla forma curiosa (PDF), 2018. URL consultato il 18 aprile 2022 (archiviato il 19 aprile 2022).
- ^ (EN) Harry P. Schultz, Topological Organic Chemistry. Polyhedranes and Prismanes, in The Journal of Organic Chemistry, vol. 30, n. 5, 1965-05, pp. 1361–1364, DOI:10.1021/jo01016a005. URL consultato il 18 aprile 2022 (archiviato il 12 gennaio 2021).
- ^ Il prismano successivo, il [4]prismano, è rappresentato dal cubano.
- ^ (EN) T. N. Gribanova, R. M. Minyaev e V. I. Minkin, Quantum-chemical investigation of structure and stability of [n]-prismanes and [n]-asteranes, in Russian Journal of Organic Chemistry, vol. 43, n. 8, 1º agosto 2007, pp. 1144–1150, DOI:10.1134/S107042800708009X. URL consultato il 1º settembre 2023.
- ^ (EN) Harry P. Schultz, Topological Organic Chemistry. Polyhedranes and Prismanes, in The Journal of Organic Chemistry, vol. 30, n. 5, 1965-05, pp. 1361–1364, DOI:10.1021/jo01016a005. URL consultato il 1º settembre 2023.
- ^ Experimental data for C6H6 (Prismane), su Computational Chemistry Comparison and Benchmark DataBase.
- ^ Ladenburg A., ., in Chemische Berichte, vol. 2, 1869, p. 140.
- ^ a b c Katz T. J., Acton N., Synthesis of Prismane, in Journal of the American Chemical Society, vol. 95, 1973, pp. 2738–2739, DOI:10.1021/ja00789a084.
- ^ The International Union of Pure and Applied Chemistry (IUPAC), IUPAC - valence isomer (V06590), su goldbook.iupac.org. URL consultato il 1º settembre 2023.
- ^ (EN) R. B. Woodward e Roald Hoffmann, The Conservation of Orbital Symmetry, in Angewandte Chemie International Edition in English, vol. 8, n. 11, 1969-11, pp. 781–853, DOI:10.1002/anie.196907811. URL consultato il 1º settembre 2023.
- ^ (EN) David M. Lemal e Jerrold P. Lokensgard, Hexamethylprismane, in Journal of the American Chemical Society, vol. 88, n. 24, 1966-12, pp. 5934–5935, DOI:10.1021/ja00976a046. URL consultato il 1º settembre 2023.
- ^ (EN) I. K. Korobitsyna, A. V. Khalikova e L. L. Rodina, 4-Phenyl-1,2,4-triazoline-3,5-dione in organic synthesis (review), in Chemistry of Heterocyclic Compounds, vol. 19, n. 2, 1º febbraio 1983, pp. 117–136, DOI:10.1007/BF00506417. URL consultato il 1º settembre 2023.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su prismano
Wikimedia Commons contiene immagini o altri file su prismano