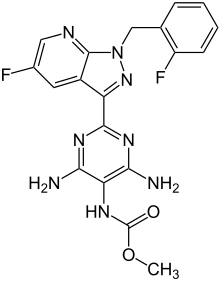
ベルイシグアト
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Verquvo |
| ライセンス | US Daily Med:リンク |
| 胎児危険度分類 | |
| 法的規制 | |
| データベースID | |
| CAS番号 | 1350653-20-1 |
| ATCコード | C01DX22 (WHO) |
| PubChem | CID: 54674461 |
| DrugBank | DB15456 |
| ChemSpider | 32700337 |
| UNII | LV66ADM269 |
| KEGG | D11051 |
| ChEBI | CHEBI:142432 |
| ChEMBL | CHEMBL4066936 |
| 化学的データ | |
| 化学式 | C19H16F2N8O2 |
| 分子量 | 426.39 g·mol−1 |
| |
| |
ベルイシグアト[3](Vericiguat)は、心血管死や心不全のリスクを低減するために使用される医薬品である。経口で服用される[1][2]。
一般的な副作用には、低血圧や赤血球数の低下(貧血)がある[2]。
ベルイシグアトは、可溶性グアニル酸シクラーゼ(sGC)を刺激する薬剤である[1]。米国では2021年1月に医療用医薬品として承認された[2][4]。日本では、2021年6月に承認された[5]。
効能・効果
[編集]- 慢性心不全[6] - ただし、慢性心不全の標準的な治療を受けている患者に限る。
ベルイシグアトは、米国では駆出率が45%未満の症候性慢性心不全を有する成人において、心血管死および心不全による入院、または外来での利尿剤の点滴が必要となった場合の入院のリスクを低減することを効能としている[1][2]。
副作用
[編集]重大な副作用として、低血圧(7.4%)が挙げられている[6]。
動物実験により、大量投与で胎児への影響が見られたことから、妊婦へは投与しないことが望ましい[6][2]。
作用機序
[編集]血管平滑筋はNO-sGC-cGMP経路で弛緩するが、慢性心不全では内皮の機能不全や一酸化窒素(NO)の産生低下により、可溶性グアニル酸シクラーゼ(sGC)への刺激が不充分となっている。ベルイシグアトは、sGCを直接刺激する作用と、内因性NOに対するsGCの感受性を高める作用を併せ持ち、両機序により環状グアノシン一リン酸(cGMP)の産生を高め、血管平滑筋を弛緩させる[5]。
承認
[編集]米国食品医薬品局(FDA)は、心不全が悪化した23歳から98歳までの5,050人を対象とした臨床試験(NCT02861534)のエビデンスに基づき、ベルイシグアトを承認した[2]。本試験は、欧州、アジア、北米、南米の42か国、694施設で実施された[2]。本試験では、悪化した心不全の症状を持つ参加者が登録され、参加者は、ベルイシグアトまたはプラセボを1日1回投与する群に無作為に割り付けられた[2]。
日本では、上記の国際共同臨床試験のほか、国内第I相試験、国外第Ib相試験、国際共同第II相試験(欧州、米国、日本ほか計24か国)の結果を医薬品医療機器総合機構が評価して承認した[7]:13。
関連項目
[編集]- リオシグアト - 最初に実用化されたsGC刺激薬(肺高血圧症治療薬)
参考資料
[編集]- ^ a b c d e “Verquvo- vericiguat tablet, film coated”. DailyMed. 9 February 2021閲覧。
- ^ a b c d e f g h i “Drug Trials Snapshot: Verquvo”. U.S. Food and Drug Administration (FDA) (8 February 2021). 8 February 2021閲覧。
 この記述には、アメリカ合衆国内でパブリックドメインとなっている記述を含む。
この記述には、アメリカ合衆国内でパブリックドメインとなっている記述を含む。
- ^ “KEGG DRUG: ベルイシグアト”. www.genome.jp. 2021年9月6日閲覧。
- ^ “Verquvo: FDA-Approved Drugs”. U.S. Food and Drug Administration (FDA). 19 January 2021閲覧。
- ^ a b 日経メディカル. “慢性心不全に対する初のsGC刺激薬が登場”. 日経メディカル. 2021年9月6日閲覧。
- ^ a b c “ベリキューボ錠2.5mg/ベリキューボ錠5mg/ベリキューボ錠10mg 添付文書”. www.info.pmda.go.jp. 2021年9月6日閲覧。
- ^ “ベリキューボ錠2.5mg/ベリキューボ錠5mg/ベリキューボ錠10mg インタビューフォーム”. www.info.pmda.go.jp. 2021年9月6日閲覧。
関連文献
[編集]- “Vericiguat in Patients with Heart Failure and Reduced Ejection Fraction”. N Engl J Med 382 (20): 1883–1893. (May 2020). doi:10.1056/NEJMoa1915928. PMID 32222134.
外部リンク
[編集]- “Vericiguat”. Drug Information Portal. U.S. National Library of Medicine. 2021年9月6日閲覧。
- 臨床試験番号 NCT02861534 研究名 "A Study of Vericiguat in Participants With Heart Failure With Reduced Ejection Fraction (HFrEF) (MK-1242-001) (VICTORIA)" - ClinicalTrials.gov