TFIIH
| general transcription factor IIH, polypeptide 1, 62kDa | |
|---|---|
| 識別子 | |
| 略号 | GTF2H1 |
| 他の略号 | BTF2 |
| Entrez | 2965 |
| HUGO | 4655 |
| OMIM | 189972 |
| RefSeq | NM_005316 |
| UniProt | P32780 |
| 他のデータ | |
| 遺伝子座 | Chr. 11 p15.1-p14 |
| general transcription factor IIH, polypeptide 2, 44kDa | |
|---|---|
| 識別子 | |
| 略号 | GTF2H2 |
| 他の略号 | BTF2, TFIIH, BTF2P44, T-BTF2P44 |
| Entrez | 2966 |
| HUGO | 4656 |
| OMIM | 601748 |
| RefSeq | NM_001515 |
| UniProt | Q13888 |
| 他のデータ | |
| 遺伝子座 | Chr. 5 q12.2-13.3 |
| general transcription factor IIH, polypeptide 3, 34kDa | |
|---|---|
| 識別子 | |
| 略号 | GTF2H3 |
| 他の略号 | BTF2, TFIIH |
| Entrez | 2967 |
| HUGO | 4657 |
| OMIM | 601750 |
| RefSeq | NM_001516 |
| UniProt | Q13889 |
| 他のデータ | |
| 遺伝子座 | Chr. 12 q24.31 |
TFIIH(transcription factor II H)は、さまざまな遺伝子の転写やヌクレオチド除去修復(NER)経路に関与するタンパク質複合体である。1989年にin vitro転写に不可欠な転写因子として特性解析がなされたことで、TFIIHの存在は明らかとなった。この因子は酵母からも単離され、最終的に1992年にTFIIHと命名された[1][2]。
歴史
[編集]TFIIHは、同定以前にはいくつかの名称で呼ばれていた。この因子は1989年にラットの肝臓から初めて単離された際にはfactor δ、またHeLa細胞から単離された際にはBTF2(basic transcription factor 2)、酵母から単離された際にはfactor Bと呼ばれた[3]。最終的に1992年にTFIIHとして知られるようになった[4]。
構造
[編集]TFIIHは10個のサブユニットから構成され、そのうちの7つがコア複合体を構成し、3つは解離可能なCAK(CDK activating kinase)モジュールを構成する[5]。コア複合体はERCC2/XPD、ERCC3/XPB、GTF2H1/p62、GTF2H4/p52、GTF2H2/p44、GTF2H3/p34、GTF2H5/TTDA/p8から構成され、CAKはCDK7、MAT1、サイクリンHからなる[6]。CAKはERCC2/XPDを介してコア複合体と連結されている[7]。ERCC2/XPDとERCC3/XPBはヘリカーゼそしてATPアーゼとしての活性を持ち、転写バブルの形成を補助する。試験管内では、DNA鋳型が変性していない場合やスーパーコイルを形成している場合にのみこれらのサブユニットが必要である。CDK7とサイクリンHはRNAポリメラーゼIIのC末端ドメインのセリン残基をリン酸化し、また細胞周期に関与する他のタンパク質のリン酸化も行っている可能性がある。
機能
[編集]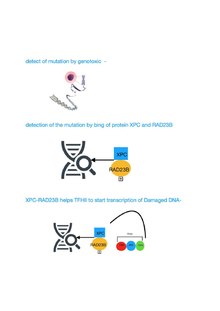
TFIIHの一般的機能は、タンパク質コーディング遺伝子の転写開始、そしてヌクレオチド除去修復(NER)である[8]。
TFIIHはRNAポリメラーゼIIを遺伝子のプロモーターへリクルートする基本転写因子の1つであり、ヘリカーゼとしてDNAを巻き戻す機能を果たす。また、NERの全ゲノム修復(global genome repair、GGR)経路または転写共役修復(transcription-coupled repair、TCR)経路のいずれかによってDNA損傷が認識された後のDNAの巻き戻しも担う[9][10]。TFIIHは損傷の認識後にDNAの二重らせん構造を開くことでNERに関与する。NERは、かさ高い化学損傷や紫外線損傷など、正常な塩基対をゆがめるさまざまな損傷を除去する多段階の経路である。TFIIHの構成要素を含む、NER経路を触媒するタンパク質をコードする遺伝子の欠陥は、早老の症状を引き起こすことが多い[11][12](老化のDNA損傷仮説も参照)。
疾患
[編集]ERCC3(XPB)、ERCC2(XPD)、GTF2H5(TTDA)遺伝子の変異は、硫黄欠乏性毛髪発育異常症の原因となる。この疾患は、光感受性、魚鱗癬、脆い髪や爪、知的障害、生殖能力の低下または低身長によって特徴づけられる[11]。
TFIIHのサブユニットをコードする遺伝子の多型は、皮膚、乳房、肺など多くの組織におけるがん感受性の増大と関係している。XPDやXPBなどのサブユニットの変異は、色素性乾皮症(XP)またはXP合併型のコケイン症候群(XP/CS)など[13]、さまざまな疾患の原因となる。さらに、ウイルスにコードされるタンパク質にはTFIIHを標的とするものもある[14]。
阻害剤
[編集]グルコーストランスポーターの発現が増加している低酸素状態のがん細胞に対し、基本転写因子TFIIHのXPBサブユニットの阻害を介して哺乳類の転写を阻害する強力な生物活性を有するトリプトリドなどの天然物をグルコース抱合体として標的投与する方法が報告されている[15]。
出典
[編集]- ^ “Factors involved in specific transcription by mammalian RNA polymerase II. Identification and characterization of factor IIH”. The Journal of Biological Chemistry 267 (4): 2786–93. (February 1992). doi:10.1016/S0021-9258(18)45947-9. PMID 1733973.
- ^ “Mechanism of ATP-dependent promoter melting by transcription factor IIH”. Science 288 (5470): 1418–22. (May 2000). Bibcode: 2000Sci...288.1418K. doi:10.1126/science.288.5470.1418. PMID 10827951.
- ^ Kolesnikova, Olga; Radu, Laura; Poterszman, Arnaud (2019). “TFIIH: A multi-subunit complex at the cross-roads of transcription and DNA repair”. Advances in Protein Chemistry and Structural Biology 115: 21–67. doi:10.1016/bs.apcsb.2019.01.003. ISSN 1876-1631. PMID 30798933.
- ^ “The essential and multifunctional TFIIH complex”. Protein Science 27 (6): 1018–1037. (June 2018). doi:10.1002/pro.3424. PMC 5980561. PMID 29664212.
- ^ “Dual role of TFIIH in DNA excision repair and in transcription by RNA polymerase II”. Nature 368 (6473): 769–72. (April 1994). Bibcode: 1994Natur.368..769D. doi:10.1038/368769a0. PMID 8152490.
- ^ “Dual role of TFIIH in DNA excision repair and in transcription by RNA polymerase II”. Nature 368 (6473): 769–72. (April 1994). Bibcode: 1994Natur.368..769D. doi:10.1038/368769a0. PMID 8152490.
- ^ “Transcription of eukaryotic protein-coding genes”. Annual Review of Genetics 34: 77–137. (2000). doi:10.1146/annurev.genet.34.1.77. PMID 11092823.
- ^ “TFIIH: when transcription met DNA repair”. Nature Reviews. Molecular Cell Biology 13 (6): 343–54. (May 2012). doi:10.1038/nrm3350. PMID 22572993.
- ^ “Rapid switching of TFIIH between RNA polymerase I and II transcription and DNA repair in vivo”. Molecular Cell 10 (5): 1163–74. (November 2002). doi:10.1016/s1097-2765(02)00709-8. PMID 12453423.
- ^ “TFIIH is an elongation factor of RNA polymerase I”. Nucleic Acids Research 40 (2): 650–9. (January 2012). doi:10.1093/nar/gkr746. PMC 3258137. PMID 21965540.
- ^ a b “TTDA: big impact of a small protein”. Experimental Cell Research 329 (1): 61–8. (November 2014). doi:10.1016/j.yexcr.2014.07.008. PMID 25016283.
- ^ “Genome Instability in Development and Aging: Insights from Nucleotide Excision Repair in Humans, Mice, and Worms”. Biomolecules 5 (3): 1855–69. (August 2015). doi:10.3390/biom5031855. PMC 4598778. PMID 26287260.
- ^ “Phenotypic heterogeneity in the XPB DNA helicase gene (ERCC3): xeroderma pigmentosum without and with Cockayne syndrome”. Human Mutation 27 (11): 1092–103. (November 2006). doi:10.1002/humu.20392. PMID 16947863.
- ^ “TFIIH transcription factor, a target for the Rift Valley hemorrhagic fever virus”. Cell 116 (4): 541–50. (February 2004). doi:10.1016/s0092-8674(04)00132-1. PMID 14980221.
- ^ “A Glucose-Triptolide Conjugate Selectively Targets Cancer Cells under Hypoxia”. iScience 23 (9): 101536. (2020). Bibcode: 2020iSci...23j1536D. doi:10.1016/j.isci.2020.101536. PMC 7509213. PMID 33083765.