ステビオール配糖体
この項目「ステビオール配糖体」は翻訳されたばかりのものです。不自然あるいは曖昧な表現などが含まれる可能性があり、このままでは読みづらいかもしれません。(原文:en: Steviol glycoside) 修正、加筆に協力し、現在の表現をより自然な表現にして下さる方を求めています。ノートページや履歴も参照してください。(2022年9月) |
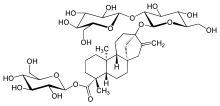
ステビオール配糖体(ステビオールはいとうたい、英: Steviol glycoside)は、南米原産のキク科植物、ステビア(Stevia rebaudiana)の葉の甘味の原因となる化合物群であり、ステビア甘味料の主成分 (または前駆体) である。近縁種のS. phlebophyllaにも含まれるほか(ただしステビア属他の種には含まれない)、およびバラ科の植物Rubus chingiiにもみられる[1]。
ステビア由来のステビオール配糖体は、スクロースの30倍から320倍の甘味度を示すという報告があるが[2]、文献により数値には相違がみられる[3]。熱およびpHに対し安定であり、発酵しない[2]。
ヒトはステビアを代謝できないため、ステビオール配糖体を摂取しても血糖反応は誘発されない[4][5]。ステビオール配糖体の一日摂取許容量(ADI) は、ステビオール当量として体重比4 mg/kgと定められている。この値は、ラットを用いた研究で100倍の投与量でも影響がみられなかったことに基く[6]。
化学構造
[編集]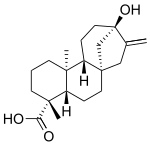
ステビオール配糖体は、ステビオール分子のカルボキシル基の水素原子がグルコース分子に置換されエステル、およびヒドロキシ基の水素原子がグルコースやラムノースと置換されアセタールを形成した配糖体である。
S. rebaudianaの葉に含まれるステビオール配糖体の構成物質と乾燥重量比率を以下に示す。
- ステビオシド(5–10%)
- ズルコシド A (0.5–1%)
- レバウジオシドA (2–4%)
- レバウジオシドB
- レバウジオシドC (1–2%)
- レバウジオシドD
- レバウジオシドE
- レバウジオシドF
- ルブソシド
- ステビオールビオシド
下から3種の化合物は微量しか存在せず、レバウジオシドBは分離時の副産物であるとの主張がある[2]。一例として、植物由来の抽出物を用いた市販のステビオール配糖体混合物は、ステビオシドがおよそ80%、レバウジオシドAが8%、レバウジオシドCが0.6%含まれていたことが報告されている[3]。
中国原産の植物Rubus chingiiには、ステビアにはみられないとされるステビオール配糖体、ルブソシドが含まれる[1]。しかし、2021年7月13日付のEUによるステビア規制令によると、ルブソシドは、ステビア葉抽出物由来のステビア甘味料の11主要成分の1つに挙げられる [7]。
ステビオシドおよびレバウジオシドAは、1931年にフランスの化学者 Bridel と Lavelle により初めて分離された[8]。両化合物のグリカンはグルコースのみからなる。ステビオシドではヒドロキシル基に2分子のグルコースが結合するのに対し、レバウジオシドAでは3分子が結合し、3分子のうち中央のグルコースが直接ステビオール骨格と結合する。
初期の官能試験によれば、レバウジオシドAはの甘味度はスクロースの150倍から320倍、ステビオシドでは10倍から270倍、レバウジオシドCでは40倍から60倍、ズルコシドAでは30倍とされた[2]。しかし、最近の評価では、レバウジオシドAで約240倍、ステビオシドで約140倍とされる[1]。また、レバウジオシド A は、苦味と後味が最も弱い[2]。甘味度は濃度によって変化し、自然比率のステビオール配糖体混合物は、3%スクロース溶液と比べて150倍、10%スクロース溶液と比べ100倍甘い[3]。
生合成
[編集]Stevia rebaudianaにおいては、ステビオール配糖体の生合成は緑色組織でのみ行われる。ステビオールがまず色素体にて産生され、小胞体でグルコシル化され、細胞質でUDP-グルコシルトランスフェラーゼの触媒作用によりグリコシル化される。レバウジオシドAはステビオシドから合成される。

ステビオール配糖体に分類される分子はいくつかあるが、どれも合成経路は同様である[9]。ステビオール配糖体の合成は、上図に示すDXP経路およびMEP経路によるイソプレン骨格の合成から始まる[10][11]。この経路の出発物質は、一次代謝に由来するピルビン酸およびグリセルアルデヒド-3-リン酸である。
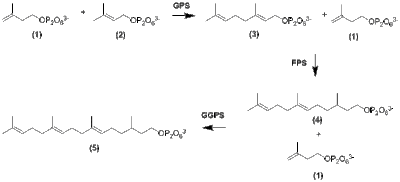
上記経路によりIPPおよびDMAPPが合成された後、上図の経路によりジテルペンの一種ゲラニルゲラニル二リン酸 (GGPP) がSN1反応機構による頭尾付加によって合成される。まず、IPPおよびDMAPPからゲラニルピロリン酸 (GPP) が合成され分子骨格が伸長する。 GPPがさらに同様の反応機構による伸長を受けてファルネシルピロリン酸 (FPP) となり、FPP がさらに伸長してGGPPとなる。
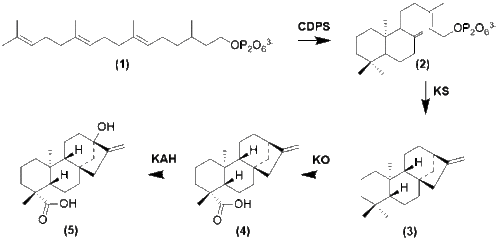
上図のように、GGPPはコパリル二リン酸シンターゼ(CDPS)およびカウレンシンターゼ(KS)によって環化され、(-)-カウレンとなる[12]。次に、多段階の酸化によりステビオールが合成される。

上図に示す例のように、ステビオールは位置選択的な糖置換を受け、ステビオール配糖体となる[13]。グリコシル化の完了したステビオール配糖体は液胞に保存される[1]。
出典
[編集]- ^ a b c d Brandle, J. E.; Telmer, P. G. (2007). “Steviol glycoside biosynthesis”. Phytochemistry 68 (14): 1855–1863. doi:10.1016/j.phytochem.2007.02.010. PMID 17397883. オリジナルの2017-08-10時点におけるアーカイブ。.
- ^ a b c d e Brandle, J. E.; Starratt, A. N.; Gijzen, M. (1998). “Stevia rebaudiana: Its agricultural, biological, and chemical properties”. Canadian Journal of Plant Science 78 (4): 527–536. doi:10.4141/P97-114.
- ^ a b c H.M.A.B. Cardello, M.A.P.A. Da Silva, M.H. Damasio (1999). “Measurement of the relative sweetness of stevia extract, aspartame and cyclamate/saccharin blend as compared to sucrose at different concentrations”. Plant Foods for Human Nutrition 54 (2): 119–129. doi:10.1023/A:1008134420339. PMID 10646559.
- ^ Geuns, JM; Buyse, J; Vankeirsbilck, A; Temme, EH; Compernolle, F; Toppet, S (5 April 2006). “Identification of steviol glucuronide in human urine”. Journal of Agricultural and Food Chemistry 54 (7): 2794–8. doi:10.1021/jf052693e. PMID 16569078.
- ^ “Stevia Leaf to Stevia Sweetener: Exploring Its Science, Benefits, and Future Potential”. Journal of Nutrition 148 (7): 1186S–1205S. (2018). doi:10.1093/jn/nxy102. PMID 29982648.
- ^ EFSA Panel on Food Additives and Nutrient Sources added to food (ANS) (2010). “Scientific Opinion on the safety of steviol glycosides for the proposed uses as a food additive”. EFSA Journal 8 (4): 1537. doi:10.2903/j.efsa.2010.1537.

- ^ COMMISSION REGULATION (EU) 2021/1156 of 13 July 2021
- ^ Bridel, M.; Lavielle, R. (1931). “Sur le principe sucré des feuilles de Kaâ-hê-é (stevia rebaundiana B)”. Comptes rendus de l'Académie des sciences (Parts 192): 1123–1125.
- ^ Huxtable, R.J., 2002. Pharmacology and toxicology of stevioside, rebaudioside A, and steviol. In: Kinghorn, A.D. (Ed.), Stevia: The Genus Stevia. Taylor and Francis, London and New York, pp.160–177.
- ^ Lichtenhalter, H.K., 1999. The 1-deoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants. Annu. Rev. Plant Physiol. PlantMol. Biol. 50, 47–65.
- ^ Totté, N., Charon, L., Rohmer, M., Compernolle, F., Baboeuf, I., Geuns, J.M.C., 2000. Biosynthesis of the diterpenoid steviol, an ent-kaurene derivative from Stevia rebaudiana Bertoni, via the methylerythritol phosphate pathway Tetrahedron Letters 41, 6407–6410
- ^ Richman, A.S., Gijzen, M., Starratt, A.N., Yang, Z., Brandle, J.E., 1999. Diterpene synthesis in Stevia rebaudiana: recruitment and up-regulationof key enzymes from the gibberellin biosynthetic pathway The Plant Journal 19, 411–421.
- ^ Richman, A., Swanson, A., Humphrey, T., Chapman, R., McGarvey, B., Pocs, R., Brandle, J., 2005. Functional genomics uncovers threeglucosyltransferases involved in the synthesis of the major sweetglucosides of Stevia rebaudiana Plant J. 41, 56–67